http://www.chemistrymag.org/cji/2001/034016pc.htm |
Apr. 1,
2001 Vol.3 No.4 P.16 Copyright |
Synthesis and bioactivity of rare earth complexes containing imidazole and acetylglycine
He Shuiyang, Zhang Di, Cao Wenkai, Zhao
Jianshe, Song Disheng
(Department of Chemistry, Northwest University, Xi'an 710069)
Received Sep. 12, 2000; Supported by the National Natural Science Foundation of China(Grant No.29471023)
Abstract New solid
RE(La,Pr,Nd,Sm,Eu,Gd,Er)Perchlorate ternary complexes containing Imidazole and
Acetylglycine have been prepared in methanol .The component of the complexes is determined
using element analysis, chemical analysis. The complex has been characterized by IR, 1HNMR,
UV and TG-DTG. And the structure of the complexes is studied by X-ray powder diffraction.
The bacterriostasis effect of on Verticillium dahliae kleb is studied.
Key words Rare earth complexes Acetylglycine Imidazole Bioactivity
何水样 张迪 曹文凯 赵建设 宋迪生
(西北大学化学系 西安 710069)
2000年9月12日收稿; 国家自然科学基金资助项目(29471023)。
摘要 在合成稀土与乙酰甘氨酸、咪唑混配固态配合物[RE(AGly)2(Im)2(H2O)3](ClO4)3·H2O(RE
=La、Pr、Nd、Sm、Eu、Gd;AGly-乙酰甘氨酸;Im-咪唑)的基础上,又合成了双核稀土配合物[Er2(AGly)4Im(H2O)5](ClO4)2·3H2O。通过化学分析,元素分析确定了配合物的组成;并利用IR、UV、X-射线粉末衍射、1HNMR及摩尔电导率测定等对配合物进行了表征,结合TG-DTG对配合物的热分解机理研究,比较了两类配合物的配位情况;用AMI半经验法对配体进行了结构优化,计算了电荷分布,并推测了配合物可能的结构。生物活性试验结果表明,该类配合物对棉花黄萎病菌有明显的抑菌效果,而对小麦赤霉菌几乎无作用。
关键词 稀土配合物 乙酰甘氨酸 咪唑 生物活性
近十几年来,稀土与氨基酸配合物的研究十分活跃[1-3],稀土与氨基酸及另一配体的多元固态配合物也有报道[4,5]。由于咪唑是一种具有杀菌、抗炎能力的化合物,因此,在60年代就有过渡金属与咪唑及氨基酸衍生物的混配配合物被合成[4,6]。生物体内组氨酸中的咪唑基团可与金属离子相结合,是蛋白质的主要生物活性部位之一。为寻找既保持稀土的助长作用,又提高其杀菌能力的新配合物,我们曾对稀土与甘氨酸(丙氨酸)和咪唑的三元配合物进行了研究[7,8],但有关稀土与乙酰甘氨酸和咪唑的混配固态配合物迄今未见文献报道,为此,本文合成了两种结构的该类配合物,并对其进行了表征及抑菌实验。
1 实验部分
1·1 试剂和仪器
稀土高氯酸盐用其氧化物(>99.95%)和高氯酸(优级纯)制备;乙酰甘氨酸为生化试剂;咪唑和其他试剂为分析纯。
配合物中稀土的质量分数用EDTA容量法滴定;C、H、N
的质量分数用PE2400元素分析仪测定;UV用PE-lambda-17 紫外-可见分光光度计;IR用IR-440
型红外光谱仪;X-衍射用日本理学D/max-ⅡC型衍射仪;1HNMR为FT-AC400核磁共振仪;
TG-DTG采用 DELTA 系列TGA7型热重分析仪;CHEM-3D软件在Pentium II上进行了计算。
1·2 配合物的合成
按物质的量比将高氯酸稀土盐:Agly:Im= 1:2:2
称量,各化合物分别溶于甲醇中。先将高氯酸盐的甲醇溶液在60℃水浴中加热,搅拌下加入AGly甲醇溶液,将未溶的乙酰甘氨酸用少量的甲醇(制铒配合物时用少量水)冲洗入三颈瓶,反应半小时后,再向反应液中加入咪唑的甲醇溶液,反应4小时(制铒配合物时加入少量NaOH,反应6小时),溶液一直澄清。在60℃水浴中浓缩至有晶膜出现,空气中自然冷却,待大量晶体出现(制铒配合物时置于浓硫酸干燥器中,数日后出现粉红色晶膜,一周后出现大量晶体),抽滤,用乙醚-丙酮的混合溶剂充分洗涤。过量的咪唑被乙醚洗掉,过量的稀土和乙酰甘氨酸被丙酮洗掉。晶体置于P2O5
干燥器中恒重。Er配合物的产率为58%, 其余的约为73% 。
1·3 抑菌试验
采用圆滤纸片抑菌圈法,以La[(AGly)2(Im)2(H2O)3](ClO4)3·H2O为代表对棉花黄萎病菌和小麦赤霉菌进行了室内抑菌试验。用不同浓度配合物与无菌水对照,每一浓度重复3次,每皿为一次重复。每皿等距离接种五块,选全部成活的接种培养皿做药效试验。将不同浓度的配合物分别加入直径为1.3cm的灭菌滤纸片上,滤纸片贴到接菌块中央,于25℃温箱培养观察。药后3d和7d分别观察长出菌落情况,并在7d后测量菌落生长直径,根据对照和处理生长菌落数和菌落直径大小分别计算菌落抑制率和菌落生长直径抑制率。
菌落抑制率=[(对照生长菌落数 -
药剂处理生长菌落数)/(对照生长菌落数)]×100%
菌落生长直径抑制率=[(对照菌落生长直径 -
药剂处理菌落生长直径)/(对照菌落生长直径)]×100%
2 结果与讨论
2.1配合物合成方法比较
两类配合物合成方法有所区别。由于用合成La―Gd配合物的方法,未制得Er的配合物,故考虑“软硬酸碱规则”,稀土盐应属硬酸,要形成配合物,必须提高配体硬碱的给电子能力,于是给其中加入少量NaOH以去配体Agly的质子。结果制得了Er的双核配合物。
2.2配合物的组成分析、溶解性
配合物中的稀土与C、H、N含量分析结果列于表1。
表1 配合物的元素分析结果
| 配合物 | RE% |
C% |
H% |
N% |
||||
La配合物 |
15.79 |
15.68 |
19.11 |
19.05 |
3.44 |
3.45 |
9.55 |
9.34 |
Pr配合物 |
15.98 |
15.86 |
19.07 |
18.99 |
3.43 |
3.28 |
9.53 |
9.75 |
Nd配合物 |
16.29 |
16.58 |
19.00 |
19.27 |
3.42 |
3.17 |
9.50 |
9.26 |
Sm配合物 |
16.87 |
16.83 |
18.96 |
19.22 |
3.41 |
3.17 |
9.48 |
9.60 |
Eu配合物 |
17.02 |
17.36 |
18.82 |
19.11 |
3.36 |
3.19 |
9.42 |
9.61 |
Gd配合物 |
17.52 |
17.39 |
18.71 |
18.91 |
3.34 |
3.22 |
9.36 |
9.19 |
Er配合物 |
27.56 |
27.19 |
18.80 |
18.51 |
3.03 |
3.03 |
6.92 |
6.73 |
从表1可以看出,配合物中各成分的实验值与理论值基本相符,说明配合物组成为RE(AGly)2(Im)2(ClO4)3
·4H2O(RE=La、Pr、Nd、Sm、Eu、Gd)及Er2(AGly)4Im(ClO4)2·8H2O。由于配合物是在甲醇介质中合成的(在水中未得到),故选择在甲醇中测定摩尔电导率(浓度约为1.0×10-4mol·dm-3),测得Pr配合物和Sm配合物的摩尔电导率分别为293s·cm2·mol-1,316 s·cm2·mol-1,Er配合物的摩尔电导率为170 s·cm2·mol-1,根据文献[9]甲醇中离子数与摩尔电导率的关系,可确定前者为1: 3型电解质,后者为1:2型电解质,正好解释了铒配合物的外界有两分子高氯酸根。同时,由于合成该配合物过程中加入少量NaOH,使AGly脱去质子,故[Er2(AGly)4Im(H2O)5] (ClO4)2·3H2O为电中性。实验表明所有配合物都溶于水和甲醇,微溶于乙醇、丙酮,不溶于乙醚。
2.3 红外光谱分析
配体咪唑、乙酰甘氨酸以及配合物的红外光谱的数据列于表2。配合物的IR图谱与两个配体的IR图谱相比,某些吸收峰发生了明显的移动,强度也有较大变化,说明稀土高氯酸盐与乙酰甘氨酸和咪唑发生了化学作用。而且从La-Gd各配合物的特征吸收峰近似,说明其成键方式相近。Er配合物的某些特征峰与其他配合物的相比区别稍大,说明Er配合物的成键方式可能有别于其它配合物。
表2 配合物的红外光谱数据/ cm-1
| 指派 | AGly |
Im |
La配合物 |
Pr配合物 |
Nd配合物 |
Sm配合物 |
Eu配合物 |
Gd配合物 |
Dy配合物 |
Er配合物 |
| nasCOO- | 1580 |
1582 |
1583 |
1578 |
1580 |
1580 |
1580 |
1583 |
1600 |
|
| nsCOO- | 1380 |
1400 |
1400 |
1400 |
1400 |
1420 |
1420 |
1420 |
1420 |
|
| dCOO- | 682 |
760 |
760 |
760 |
760 |
760 |
760 |
760 |
_ |
|
| nC=O | 1720 |
1740 |
1733 |
1735 |
1733 |
1735 |
1730 |
1731 |
_ |
|
| nC=N | 1670 |
1622 |
1624 |
1620 |
1624 |
1620 |
1618 |
1620 |
1605 |
|
| nC=C | 1450 |
1440 |
1430 |
1420 |
1435 |
1438 |
1440 |
1440 |
1430 |
|
| n-NH- | 3115 |
3160 |
3160 |
3150 |
3150 |
3145 |
3150 |
3150 |
_ |
|
| nCl-O | 1085 |
1087 |
1080 |
1080 |
1080 |
1085 |
1081 |
1081 |
||
625 |
625 |
625 |
625 |
625 |
625 |
625 |
625 |
|||
| nOH | 3400 |
3400 |
3400 |
3400 |
3380 |
3400 |
3400 |
3400 |
||
525 |
525 |
525 |
525 |
525 |
525 |
525 |
525 |
|||
Δ nas-s |
200 |
182 |
183 |
178 |
180 |
160 |
160 |
163 |
180 |
红外光谱的指派是根据文献[10]进行。从表2可见,在配合物中,COOˉ基团的对称、不对称伸缩振动带及面内歪曲振动均发生了明显紫移,而且,配合物的Δ
n= nasCOO--nsCOO-均比自由乙酰甘氨酸的Δn=200cm-1小,说明配合物中的羧基是以双齿螯合或桥式配位的,且配合物的对称性并不太好[11]。(乙酰甘氨酸在自由状态下以内盐形式呈现NH2+的特征峰在配合物中被3400cm-1附近水的宽峰峰掩盖,只有COOˉ的特征峰在配合物中都保留下来。)La-Gd配合物中酰基氧的νc=o虽紫移了17-20cm-1,但根据立体效应不可能与羧基氧配位于同一金属离子。所以这可能与和其他原子形成氢键有关。各配合物中,咪唑的nC=N和nC=C伸缩振动在配合物中均发生了红移,与文献[4]相比,说明咪唑的3位N原子参与了配位。配合物在1145~1080 cm-1出现了三条很强的吸收带,在940 cm-1出现了一条弱尖吸收带,在625 cm-1出现一吸收带,分别为离子型化合物中ClO4-的n3、n1、n4振动带,说明了ClO4-未参与配位,而n1 吸收带的出现还表明ClO4-是以扭曲的四面体形式存在的 [12]。525 cm-1 处出现了OH的面内摇摆振动峰,说明配合物中有水分子参与了配位[13]。这一点也被配合物的TG-DTG曲线中脱水温度所证实。2.4 紫外光谱分析
以水作溶剂,浓度约在1.0×10-4mol/L,测定了高氯酸盐、乙酰甘氨酸、咪唑及三元配合物的紫外光谱 。发现他们在可见光区(400~900nm)均无吸收,在190~300nm有不同的吸收,其结果列于表3。
表3 配体及配合物的紫外分析结果
| 样品 | La(ClO4)3 |
AGly |
Im |
La配合物 |
Pr配合物 |
Nd配合物 |
Eu配合物 |
Gd配合物 |
Er配合物 |
| lmax/nm | 194.4 |
<190.0 |
208.0 |
200.0 |
203.0 |
198.0 |
204.6 |
203.8 |
215.0 |
从表3可见,各配合物的最大吸收峰的波长与盐、乙酰甘氨酸和咪唑均不同,La-Gd的配合物的最大吸收峰的波长较相近,而Er配合物的最大吸收峰的波长却在215nm处,与它们相差较远。这一方面说明RE3+与两种配体都有配位作用,另一方面说明Er与配体的配位形式异于其它配合物。在Er配合物中随着共轭系统的增大,π电子云束缚更小,引起π→π*跃迁所需能量更小,吸收峰位置就向长波方向移动,故Er配合物的最大吸收峰位置在215nm处。
2.5 X-射线粉末衍射
表4列出了La、Pr、Nd及Er配合物和Im、AGly、Nd(ClO4)3·8H2O的X-射线粉末衍射数据。由此可见,配合物与构成它们的咪唑、乙酰甘氨酸、高氯酸盐的衍射数据均有明显不同,说明他们是不同的物相。而La,Pr,Nd三种配合物的特征值相近,说明其结构相似。Er配合物的特征吸收峰与其它配合物明显不同,说明其结构有异。
表4 X-射线粉末衍射特征值
| Nd盐 | d/nm |
0.704 | 0.606 | 0.428 | 0.302 |
0.246 | 0.232 |
I/I0/% |
60 | 60 |
100 | 60 | 60 |
30 | |
AGly |
d/nm |
0.744 |
0.576 | 0.497 |
0.372 | 0.323 | 0.225 |
I/I0/% |
40 |
50 |
60 |
35 |
100 | 25 | |
Im |
d/nm |
0.4371 | 0.4283 | 0.3630 | 0.3440 |
0.3115 | 0.2910 |
I/I0/% |
37 |
84 | 6 | 100 |
8 | 28 | |
La配合物 |
d/nm |
1.1296 | 0.9689 | 0.5355 | 0.4008 | 0.3633 | 0.2850 |
I/I0/% |
18 | 19 | 25 | 75 |
100 | 13 | |
Pr配合物 |
d/nm |
1.2511 | 1.0179 | 0.5434 | 0.4048 |
0.3663 | 0.2863 |
I/I0/% |
45 | 28 | 28 | 26 |
100 | 30 | |
Nd配合物 |
d/nm |
1.2167 |
0.9950 |
0.5371 |
0.4008 |
0.3630 |
0.2845 |
I/I0/% |
34 |
28 |
34 |
43 |
100 |
28 |
|
Er配合物 |
d/nm |
1.3155 |
1.1291 |
0.6342 |
0.4567 |
0.3709 |
0.2843 |
I/I/% |
26 |
26 |
45 |
100 |
30 |
18 |
根据Nd、Er配合物及两种配体(AGly、Im)的1HNMR谱,将其特征化学位移δ值列于表5。
表5 配体及配合物的特征化学位移δ/10-6
| 化合物 | a |
b |
c |
d |
e |
AGly |
1.88 |
3.78 |
|||
Im |
7.09 |
7.69 |
|||
Nd配合物 |
2.04(0.16) |
4.26(0.48) |
7.39(0.30) |
8.59(0.90) |
4.80 |
N Er配合物 |
2.18(0.30) |
3.94(0.16) |
7.52(0.43) |
8.62(0.93) |
4.76 |
* AGly和Im的数据是查于Satler标准图谱。
对配体中的氢标识为: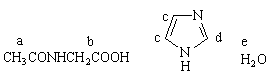
从Nd配合物的1HNMR图谱中可发现5个化学位移值:2.04、4.26、4.80、7.39、8.59,与Slater标准图谱比较:乙酰甘氨酸的特征化学位移分别向低场移动
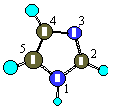 Im
Im |
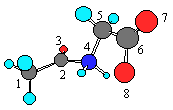 AGly AGly |
| 图1 配体的结构图 |
用AMI半经验法,对配体AGly和Im进行结构优化(图1),计算密立根电荷分布结果如表6:
表6 配体AGly和Im的非氢原子电子密度、键角和键长
|
咪唑 电子密度 键角 键长(Å) |
乙酰甘氨酸 |
||||||||||
N1 |
-0.0408 |
C5N1C2 |
107.0 |
N1C2 |
1.380 |
C1 |
0.2318 |
C1C2O3 |
127.58° |
C1C2 |
1.4902 |
C2 |
0.1523 |
N1C2N3 |
104.0 |
C2N3 |
1.377 |
C2 |
0.3035 |
C1C2N4 |
116.67° |
C2O3 |
1.2276 |
N3 |
-0.1786 |
C2N3C4 |
111.2 |
N3C4 |
1.360 |
O3 |
-0.2687 |
O3C2N4 |
115.76° |
C2N4 |
1.4966 |
C4 |
O.0339 |
N3C4C5 |
105.0 |
C4C5 |
1.325 |
N4 |
0.3531 |
C2N4C5 |
112.47° |
N4C5 |
1.4891 |
C5 |
0.033 |
C4C5N1 |
112.0 |
C5N1 |
1.356 |
C5 |
-.00070 |
C5C6O7 |
115.23° |
C5C6 |
1.5900 |
C6 |
0.4296 |
C5C6O8 |
114.69° |
C6O7 |
1.2402 |
||||||
O7 |
-0.4619 |
O7C6O8 |
130.00° |
C6O8 |
1.2630 |
||||||
O8 |
-0.5804 |
O3O7 |
5.5122 |
||||||||
O7O8 |
4.5671 |
||||||||||
在Im中,3位N原子的电荷密度最大,说明3位N原子配位能力最强。AGly中酰胺的羰基氧(O3)和羧基中的氧(O7、O8)电荷密度较大,O7、O8又比O3电荷密度大得多,故配位能力O7、O8更强。由表5可见,O7与O3、O8与O3间的距离大,根据立体效应,O3与O7、O8二者同时配位于同一金属离子的可能性较小。因此,仅O7、O8可同时螯合配位于一个金属离子,也可分别配位于两个金属离子,形成以羧基为桥的双核配合物。这一点与IR所示一致。
2.8 配合物的热分解机理
La-Gd各配合物的TG-DTG图谱相似。图2为Pr配合物的TG-DTG曲线(N2气氛,升温速率10.0℃/min),由曲线读出的各分解阶段及其分解温度范围和相应的TG残留率如下所示(括号内为理论值):
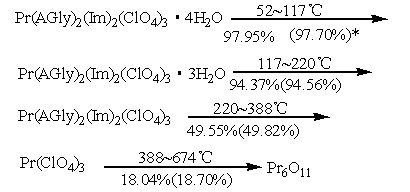
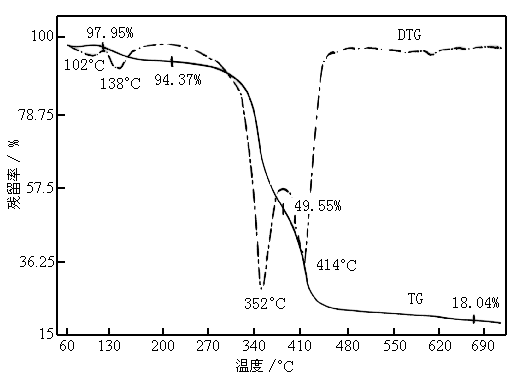 |
图2 Pr配合物的TG-DTG图谱 |
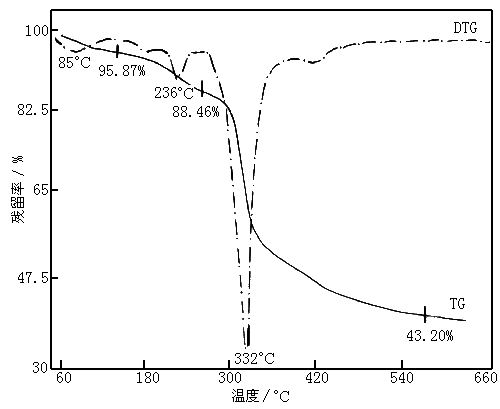 |
图3 Er配合物的TG-DTG图谱 |
图3为Er配合物的TG-DTG曲线,分解机理如下所示(括号内为理论值)。可以看出,Er配合物第一阶段失去3分子水,第二阶段失去5分子的水,根据脱水的温度,可认为第二阶段失去的5分子水为配位水,第三阶段是配体的分解、炭化、氧化,在我们所采用的温度范围595℃转化为碱式氯酸盐。其结构为 :[Er2(AGly)4Im(H2O)5](ClO4)2·3H2O。
(Pr、Er配合物热分解的最终产物均经IR、X-射线粉末衍射验证。)
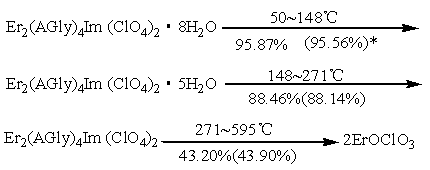
2.9 配合物的抑菌效果
[La(AGly)2(Im)2 (H2O)3](ClO4)3·H2O对棉花黄萎病菌的抑制效果见表7。
表7 配合物对棉花黄萎病菌抑菌效果
| 稀释浓度/% | 药后3天长出菌落数 | 药后7天长出菌落数 | 药后7天菌落直径 | ||||||||||||||
1 |
2 |
3 |
平均 | 抑制率% | 菌丝生长 | 1 | 2 | 3 | 平均 | 抑制率% | 菌丝生长 | 1 | 2 | 3 | 平均 | 抑制率/% |
|
6.4 |
0 |
0 |
0 |
0 |
100 | 无 |
5 | 5 | 5 | 5 | 0 |
稀疏 | 1.3 | 1.1 | 1.2 | 1.2 | 61.3 |
3.2 |
5 |
5 |
5 |
5 |
0 |
稀疏 |
5 |
5 |
5 |
5 |
0 |
较疏 |
1.8 |
1.9 |
1.8 |
1.8 |
41.9 |
1.6 |
5 |
5 |
5 |
5 |
0 |
较疏 |
5 |
5 |
5 |
5 |
0 |
较密 |
2.3 |
2.1 |
2.2 |
2.2 |
29.0 |
0.8 |
5 |
5 |
5 |
5 |
0 |
茂密 |
5 |
5 |
5 |
5 |
0 |
茂密 |
3.0 |
2.9 |
3.0 |
3.0 |
3.2 |
ck |
5 |
5 |
5 |
5 |
- |
茂密 |
5 |
5 |
5 |
5 |
- |
茂密 |
3.2 |
3.0 |
3.1 |
3.1 |
- |
由表7可见,以配合物6.4%的浓度给药,3d后抑菌率可达100%,无菌丝生长;7d后,虽有菌丝生长 ,但很稀疏,按菌落直径计算抑制率为61.3%。随培养时间的延长,药剂对菌落生长抑制率有所降低。与我们以往合成的如RE(Ala)3Im(ClO4)3·nH2O、RE(Ala)3(BeIm)(ClO4)3·H2O、RE(Ala)2(Im)2 (NO3)3·4H2O等相比[La(AGly)2(Im)2 (H2O)3](ClO4)3·H2O对该菌的抑制效果最佳,这对今后在农业上的应用提供了很有意义的信息。对小麦赤霉菌的作用,效果不明显。
REFERENCES[1] Huang Chunhui. Coordination Chemistry of Rare Earthes (Xitu Peiwei Huaxue). Beijing: Science Press (Kexue Chubanshe), 1997: 79.
[2] Li Zhenxiang, Ni Jiazuan , Li Lemin. Journal of Rare Earthes (Zhongguo Xitu Xuebao), 1990, 8 (1): 1.
[3] Yang Pin. Chemistry (Huaxue Tongbao), 1985, (7): 31.
[4] Rao G N, Li N C . Canadian Journal of Chemistry, 1966, 44: 1637.
[5] Gan Xinmin, Tan minyu, Tang Ning et al. Journal of Inorganic Chemistry (Wuji Huaxue Xuebao), 1991, 7 (1): 42.
[6] Driver R, Waiker W R . Aust. J. Chem., 1968, 21: 671.
[7] Liu Xiangrong, He Shuiyang, Song Disheng. Journal of Northwest University (Natural Science Edition) (Xibei Daxue Xuebao ), 1998, 28 (6): 497.
[8] He Shuiyang, Hu Ting, Li Huanyong et al.. Chemistry ( Huaxue Tongbao), 1999, (8): 34.
[9] Geary W. J. Coordination Chem. Rev, 1971, 7: 81.
[10] Zhong Benyixiong (Huang Deru translate). Infrared and Laman Spectra of Inorganic and Coordination Compounds (Wuji He Peiwei Huahewu De Hongwai He Laman Guangpu). Beijing: Chemical Industry Press (Huaxue Gongye Chubanshe), 1986.
[11] Deacon G B, Phillips R J . Coordination Chem. Rev., 1980, 33: 227.
[12] Kazao N. Infrared spectra of Inorganic and Coordination Compounds. New York: John Wiley & sons,1963, 11.
[13] Ma Aizeng, Li Laiming, Lin Yonghua et al. Journal of Inorganic Chemistry (Wuji Huaxue Xuebao), 1993, 9 (4): 401.