http://www.chemistrymag.org/cji/2001/03b057nc.htm |
Nov. 1,
2001 Vol.3 No.11 P.57 Copyright |
Synthesis of three 2-alkyl(aryl)-1, 3-oxathiolane compounds
Yang Yingqing, Zheng Fuping, Sun Baoguo, Ding Fuxin#, Liu Yuping,Ren Yi
(School of Chemical Engineering, Beijing Technology and Business University, 100037
Beijing;#Department of Chemical Engineering, Tsinghua University, 100084
Beijing)
Abstract 2-Acryl-1,3-oxathiolane、2-(2-furfuryl)-1,3-oxathiolane
and 2-phenyl-1,3-oxathiolane were synthesized by the reaction of 2-mercaptan ethanol with
crotonaldehyde、furfural and benzaldehyde
respectively in the presence of p-toluene sulfonic acid, where benzene was used as
azeotropic dehydration agent. The yields were 80%,89%
and 84% in turn. Structures of the compounds were identified by the data of IR spectrum、GC-MS spectrum and 1H NMR spectrum. The
synthesis scheme was convenient and high yields were available.
Keywords 2-acryl-1,3-oxathiolane; 2-(2-furfuryl)-1,3-oxathiolane;
2-phenyl-1,3-oxathiolane; 2-mercaptan ethanol; aldehyde
三种
2-烷基(芳基)-1,3-氧硫杂环戊烷类化合物的合成 , 郑福平, 孙宝国, 丁富新#, 刘玉平,任毅(北京工商大学化工学院, 北京 100037; #清华大学化工系,北京 100084)
2001年9月4日收稿;国家自然科学基金资助项目(No29872004).
摘要
以对甲苯磺酸为催化剂,巯基乙醇分别与巴豆醛、糠醛和苯甲醛(摩尔比
1:1.1)在苯中共沸脱水,合成三种目标产物2-丙烯基-1,3-氧硫杂环戊烷、2-(2-呋喃基)-1,3-氧硫杂环戊烷和2-苯基-1,3-氧硫杂环戊烷。其产率分别为80%、89%和84%。经红外光谱、色-质联机和核磁共振谱分析,确证了产物结构。此方法简便易行,产率较高。
关键词 2-丙烯基-1,3-氧硫杂环戊烷; 2-(2-呋喃基)-1,3-氧硫杂环戊烷;
2-苯基-1,3-氧硫杂环戊烷; 巯基乙醇; 醛
1-烷基-1-烷氧基-1-烷硫基甲烷类化合物具有特殊的化学结构,在同一个碳原子上有一个烷氧基和一个烷硫基,它在有机合成中是一种重要的化合物[1]。就结构而言,1,3-氧硫杂环戊(己)烷类化合物也可归为1-烷基-1-烷氧基-1-烷硫基甲烷类化合物。1,3-氧硫杂环戊(己)烷类香料化合物已在食品、口香糖及医药等领域有广泛应用[2,3
]。其中2-甲基-4-丙基-1,3-氧硫杂环己烷已在西番莲果的香味组份中检测出,其具有强烈的、天然的水果香气,并稍带青叶香气和焦味[4,5],美国食用香料及萃取物制造者协会(FEMA)批准使用号为3578。研究这类化合物的合成对香料、食品和医药等相关行业的发展有着非常重要的意义。
文献报道的合成方法有:以三异丙基硅三氟甲烷基磺酸盐为催化剂,醛(酮)与2-巯基醇直接反应生成1,3-氧硫杂环戊(己)烷[7],这种方法所用的催化剂难于得到且价格较高,用这种方法合成的2-苯基-1,3-氧硫杂环戊烷,产率只有55%;以高岭土为催化剂,醛(酮)与2-巯基醇直接反应生成1,3-氧硫杂环戊(己)烷[8],产物难以与高岭土分离;以对甲苯磺酸为催化剂,二氯甲烷、环己烷为溶剂,巯基醇与醛(酮)直接反应生成1,3-氧硫杂环戊(己)烷[2-4,6,7,9-12]。这些方法中有的用二氯甲烷、环己烷共沸带水,有的用分子筛除水,这些方法共同的不足在于除水过程处理得不好,产率只有60%~80%。
作者采用一种操作简便的方法:即以回流温度较高、带水效果好的苯为溶剂,以对甲苯磺酸为催化剂,巯基乙醇与丙醛(摩尔比
1:1.1)直接反应,用分水器除水,合成三种目标产物:2-丙烯基-1,3-氧硫杂环戊烷、2-(2-呋喃基)-1,3-氧硫杂环戊烷和2-苯基-1,3-氧硫杂环戊烷。用此方法能得到80%以上的产率。
1 实验
1.1 反应式
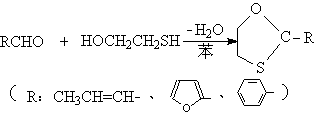
1.2 试剂与仪器
试剂:巯基乙醇(>99%)、巴豆醛(>99%)、糠醛(>99%)、苯甲醛(CP)、对甲苯磺酸(AR)、苯(AR)、二乙胺(CP)。
仪器:Vector22傅立叶变换红外光谱仪(液膜法)、DMX-300型核磁共振仪(溶剂CDCl3
,内标TMS)、岛津GC-17A/QP-5000MS色-质联用仪、岛津GC-9A型气相色谱仪。
1.3 三种目标产物的合成
1.3.1 2-丙烯基-1,3-氧硫杂环戊烷(a)
在250ml三口烧瓶上装置带有冷凝管的分水器,依次加入100ml苯、7.8g(0.1mol)巯基乙醇、7.7g(0.11mol)丙醛和0.2g对甲苯磺酸。加热回流分出水约2ml(需2小时左右)。将反应液冷却至室温,用二乙胺将反应液pH值调至7-8。减压蒸馏,在72-74℃/2100Pa温度下收集无色透明油状液体11.0g,即为目标产物a。其具有浓郁的烤肉香气和青叶香气,产率80%(按巯基乙醇计算),质量分数94%(GC法确定)。IR,υmax(cm-1):2940.4、2868.6(m,υCH3);
1672.7(w,δC=C) ; 1448.7、1342.9(m, δCH3 ); 1056.2(vs,
υC-O-C ); 962.3、720.3(m-s, γ-0-CH-S-)。 MS(EI),m/z(%):130(M+);115(M-CH3
) ;89(M-CH=CHCH3 );60(SCH2CH2, 100 );45(CH3CH=OH)
;41(CH=CHCH3)。1H NMR,δ:1.7197-1.7408 (d,3H,CH3,J=6.3Hz)
3.0608-3.0955(t,2H,OCH2,J=10.4Hz);3.7694-4.3808(dd,2H,SCH2,J=23.8、18.5Hz);5.4466-5.4729(q,1H,=CHCH3,J=7.9Hz);5.5645-5.6407(t,1H,CH=,J=22.9Hz);5.7910-5.8634(d,1H,SCHO,J=21.7Hz)。
1.3.2 2-(2-呋喃基)-1,3-氧硫杂环戊烷(b)
以糠醛9.6g (0.11mol)代替巴豆醛,其它操作步骤与1.3.1类似,在124-125℃/3700Pa温度下收集无色透明油状液体14.5g,即为目标产物b,其具有浓郁的炖肉香气及咖啡香气,产率89%
(按巯基乙醇计算),质量分数96%(GC法确定)。IR,υmax(cm-1):2941.7、2873.7(m,
υCH3 ); 1438.6、1330.1(m, δCH3 ); 1055.6(vs,
υC-O-C ); 967.6、743.6(m-s, γ-0-CH-S-); 884.0(m, γCH);
598.5(w, υS-C )。MS(EI),m/z(%):156(M+);89(M-![]() ) +;67(
) +;67(![]() );60(SCH2CH2,
100 ) ;45(CH3CH=OH) 。1H NMR,δ:3.11145-3.30166
(dd,2H,OCH2,J=20.9、16.0Hz); 4.02760-4.35977(dd,2H,SCH2,
J=21.9、20.2Hz);6.133329(s,1H,OCHS); 6.36035-6.36603 (d,1H, J=1.7Hz);
6.47401-6.53671(t,1H, J=18.8Hz);7.41593-7.45068(d,1H, J=10.4Hz)。
);60(SCH2CH2,
100 ) ;45(CH3CH=OH) 。1H NMR,δ:3.11145-3.30166
(dd,2H,OCH2,J=20.9、16.0Hz); 4.02760-4.35977(dd,2H,SCH2,
J=21.9、20.2Hz);6.133329(s,1H,OCHS); 6.36035-6.36603 (d,1H, J=1.7Hz);
6.47401-6.53671(t,1H, J=18.8Hz);7.41593-7.45068(d,1H, J=10.4Hz)。
1.3.3 2-苯基-1,3-氧硫杂环戊烷(c)
以苯甲醛10.6g (0.11mol) 代替巴豆醛,其它操作步骤与1.3.1类似,在143℃-145℃/3000Pa温度下收集无色透明油状液体14.8g,即为目标产物c,其具有浓郁的烤肉香气及苦杏仁香气,产率84%
(按巯基乙醇计算),质量分数94%(GC法确定)。IR,υmax(cm-1):υmax(cm-1):2942.1、2873.7(m,
υCH);1438.6(m, δCH2); 1330.1(m, δCH3 ); 1055.6(vs,
υC-O-C ); 973.6 (m, γ-0-CH-S-); 705.0(s,υCH)。MS,(EI)m/z(%):166(M+);89(
M-![]() ) ;77(
) ;77(![]() ) ; 60(SCH2CH2,
100 ) ;45(CH3CH=OH)。1H NMR,δ:3.20631 -3.33257(dd,2H,OCH2,
J=13.0、9.6Hz); 3.92591-4.57605(dd,2H,SCH2, J=24.0、18.4 Hz);
6.0743(s,1H,OCHS); 7.2692-7.5721 (m,5H,Ph-H)。
) ; 60(SCH2CH2,
100 ) ;45(CH3CH=OH)。1H NMR,δ:3.20631 -3.33257(dd,2H,OCH2,
J=13.0、9.6Hz); 3.92591-4.57605(dd,2H,SCH2, J=24.0、18.4 Hz);
6.0743(s,1H,OCHS); 7.2692-7.5721 (m,5H,Ph-H)。
2 分析与结论
反应机理如下:
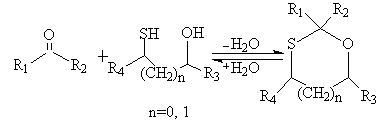
该过程可以看作是醇对羰基的可逆加成反应,通过分水器不断地共沸带水,使反应向着有利于生成噁噻烷(即1,3-氧硫杂环化合物)的方向进行[13]。 所以对于本反应来说,选择较为有效的脱水方式是一个的关键环节。本方法采用苯为溶剂,因其有很好的共沸带水效果,提高了产率,并且缩短了反应时间。作者以苯为溶剂,巯基乙醇分别与巴豆醛、糠醛和苯甲醛反应合成2-丙烯基-1,3-氧硫杂环戊烷、2-(2-呋喃基)-1,3-氧硫杂环戊烷和2-苯基-1,3-氧硫杂环戊烷,得到高达80%以上的产率。此方法操作简便。
REFERENCES
[1] Sun B G, Fu X, Liu Y P et al. Chemistry Online, 2000, (3): c00029.
[2] Wilson Richard A, John V Pascale, Manfred Hugo. U. S. Patent, 1977, 4 042 601 .
[3] Wilson Richard A, Pascale John V, Manfred Hugo. U. S. Patent, 1977, 4 031 257 .
[4] Parliament Thomas H. U.S. Patent, 1985, 4 496 600 .
[5] Li H, Li P W, Yu Z H. Transl. Food Flavors Chemistry―Heterocyclic
Flavors. Beijing: Chinese Light Industry Press, 1992: 55, 218.
[6] Firmenich S L. Helvetica Chimica Acta., 1976, 59 (5): 168.
[7] Ludik Streinz, Bohumir Koutek, David Saman. Collect. Czech. Chem. Commu., 1997, 62:
665.
[8] Ponde Datta E, Deshpand Vishnu H, Bulbule Vivek J et al. J. Org. Chem., 1998, 63:
1058.
[9] Mosandl A, Heusinger G. Liebigs Ann. Chem., 1985, 1185.
[10] Paavo Pasanen, Kalevi Pihlaja. Acta. Chem. Scand., 1971, 25 (5): 1908.
[11] Paavo Pasanen and Kalevi Pihlaja. Acta. Chem. Scand., 1970, 24 (6): 2257.
[12] Luminita Muntean, Ion Grosu, Sorin Mager. Studia Univ. Babes-Bolyai Chemia., 1995, 40
(1-2): 189.
[13] Xing Q Y, Xu R Q, Zhou Z. Basal Organic Chemistry. Beijing: Higher Education Press,
1980, 357.