http://www.chemistrymag.org/cji/2001/03c060nc.htm |
Dec. 1,
2001 Vol.3 No.12 P.60 Copyright |
Tang Yuchao, Hu Chun, Wang Yizhong
(Research Center for Eco-Environmental Sciences, State Key Laboratory of Environmental Aquatic Chemistry, Chinese Academy of Sciences, Beijing, 100085, China.)
Abstract Influences of seven common inorganic cations on the photoactivity of TiO2/SiO2 have been investgated in the photodegradation of dyes. The lowest concentration of inorganic cations resulting in the deactivation of TiO2/SiO2 photoactivity was measured. Four cations are found to inhibit photocatalysis at some or all of the concentrations tested, although only Mn2+ has some detrimental effect on catalysts and cannot be revived fully. The deactivated catalysts can be regenerated simply with rinsing of H2O except for that Mn2+ and Fe3+ can be regenerated with rinsing of HCl. The mechanisms of the deactivation of the catalysts were also discussed.
Keywords photocatalysis, inorganic cations, TiO2, catalyst deactivation, dyes
无机阳离子对
TiO2/SiO2光催化剂降解染料化合物活性的影响唐玉朝
胡 春 王怡中(中国科学院生态环境研究中心,环境水化学国家重点实验室,北京,100085)
摘要
以酸性红B、阳离子蓝X-GRL和活性艳红K-2G为模型化合物考察了7种最常见的无机阳离子在不同浓度下对TiO2/SiO2复合光催化剂活性的影响。结果发现Mn2+强烈地导致失活,Cu2+、Ni2+、Fe3+影响次之,Ca2+、Mg2+对催化剂活性影响不明显,Al3+有明显的促进作用。Cu2+、Ni2+失活的催化剂通过简单的水冲洗即可恢复活性,Mn2+和Fe3+造成失活的需用HCl冲洗才能恢复活性。催化剂的失活机制也作了探讨。关键词 光催化 无机阳离子 TiO2 催化剂失活 染料
光催化方法处理环境污染物是一种新兴的污染治理技术,近年来受到广泛关注
[1-2],随着光催化技术的日趋成熟,作为一种有着诸多优点的污染控制技术其实用化是必然的结果。然而在实际工业废水中通常会含有多种有机、无机离子,这些离子很容易造成催化剂活性降低。预防催化剂失活的措施如果以离子交换或其它方法去除溶液中的离子会造成运行成本过高,因而探索催化剂的再生方法就显得十分必要。但是迄今为止这些方面的研究工作尚很少,所以研究TiO2催化剂在光催化反应过程中催化剂失活与中毒以及催化剂再生工艺是一项十分有意义而紧迫的工作。本文考察了7种常见的无机阳离子在溶液中对TiO2/SiO2复合催化剂光催化降解染料化合物的活性影响。考虑到一些阳离子只能存在于较强的酸性条件下,以及Cu2+、Ni2+、Fe3+离子在水溶液中自身有颜色而影响染料的比色,故实验采用三种不同的染料,即酸性红B、阳离子蓝X-GRL和活性艳红K-2G,Mn2+、Al3+、Ca2+和Mg2+用酸性红B,Cu2+和Ni2+采用阳离子蓝X-GRL,而Fe3+和Al3+采用活性艳红K-2G。三种染料分别为酸性染料、阳离子染料和活性染料,具有一定的代表性。 1 实验部分1.1 实验材料
TiO2/SiO2复合催化剂的制备:将干燥的多孔硅胶(青岛海洋化工厂生产)浸渍在钛酸四丁酯Ti(Obu)4与环己烷的混合溶液(V(Ti(Obu)4/V(C6H12) = 4)中反应15 h;样品在313 K下蒸发掉环己烷溶液后,在393 K下干燥6 h;最后在空气中经过下列三步煅烧:473 K焙烧1 h,623 K焙烧1 h,723 K焙烧4 h。通过在空气中的焙烧,Ti(Obu)4被氧化为TiO2。催化剂经过筛后取80-160目之间部分,用去离子水冲洗1 h后晾干备用,催化剂性能参见文献[3]。反应所用试剂均为分析纯,未经进一步纯化,水为去离子水。
1.2 光催化反应实验
1.2.1 Mn2+、Mg2+、Ca2+、Cu2+、Ni2+对光催化活反应影响的实验
MnCl2、MgCl2、CaCl2、CuCl2、NiCl2的实验过程如下:在直径为90 mm的浅池反应器中加入30 ml染料溶液,加入适量TiO2/SiO2复合催化剂,反应液的混合由摇床震荡完成,添加适当浓度的无机盐溶液,吸附反应30 min后打开主波长为365 nm功率为15 W的黑光灯(北京空后保温材料厂),反应1 h。控制溶液pH值在一定范围内。取样离心10 min,以752紫外可见分光光度仪测定溶液的色度变化考察其反应速率。 以吸附30 min时的溶液浓度为起始浓度,光反应1 h后的浓度与起始浓度的差值为ΔC,根据反应时间计算反应速率常数v = ΔC/Δt,用反应速率的快慢评价离子对催化剂活性影响的大小。
1.2.2 Fe3+、Al3+的光催化反应影响实验
在NDC光化学反应器(南京大学环境科学系研制,参见文献[4])中,加入250 ml、60 mg/L的活性艳红K-2G溶液及适当浓度被评价离子的盐溶液,加入0.25 g催化剂,控制溶液的pH在一定范围,通入空气340 ml/min以保证充分搅拌。30 min后打开300 W主波长为365 nm的高压汞灯(北京电光源研究所),通入冷凝水冷却反应器。每隔10 min取样一次,样品离心10 min,以752紫外可见分光光度仪测定溶液的色度变化考察其反应速率。以上述同样的方法计算反应速率常数v,用反应速率的快慢评价离子对催化剂活性影响的大小。
催化剂经反应后,分别以去离子水冲洗10 min,室温下晾干,重复上述实验检测其活性,对水冲洗活性恢复低的Fe3+、Mn2+再用0.10 M的HCl冲洗10 min,然后以去离子水冲洗10 min,室温晾干后再次测定其活性。 2 实验结果
2.1 Mn2+对光催化降解酸性红B反应速率的影响
Mn2+对光催化降解反应速率的影响见图1。实验MnCl2的浓度范围为10-1000 mmol/L,反应起始pH = 4.15-5.64。在实验的浓度范围内,溶液中锰的主要存在形式为Mn2+和MnCl+,而MnOH+的量很小,随着加入的MnCl2浓度的增加,Mn2+的所占比重越少,而Mn(Cl)+的比重越多。由图1可以看出锰离子对催化剂降解速率的影响,当加入10 mmol/L时降解速率迅速降低,10-100 mmol/L时反应速率变化不明显,超过100 mmol/L时反应速率持续降低。水反冲洗后,活性仅恢复了39.3%,用HCl反冲洗后,活性恢复了76.6%。
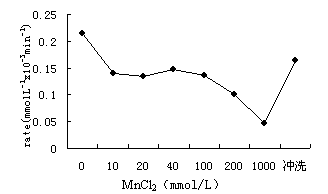
图1 Mn2+对光催化降解酸性红B的影响
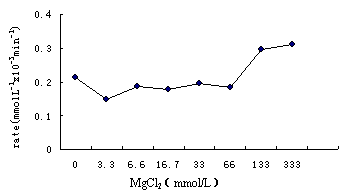
图2 Mg2+对光催化降解酸性红B的影响
2.2 Mg2+对光催化降解酸性红B反应速率的影响
Mg2+对光催化反应速率的影响见图2。实验中MgCl2浓度范围为3.3-333 mmol/L,反应初始pH值用HCl调节为5.36-6.14,溶液中镁绝大多数以Mg2+形式存在,Mg(OH)+非常少。由图2可看出,在较低浓度时反应速率略有下降,但随着镁离子浓度的增加,总体速率呈现增加趋势。
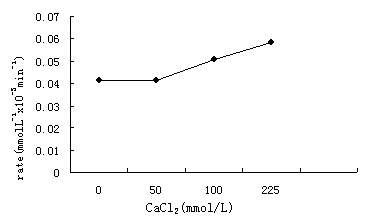
图3 Ca2+对光催化降解酸性红B反应速率的影响
2.3 Ca2+对光催化降解酸性红B反应速率的影响
Ca2+对光催化反应速率的影响见图3。实验取 CaCl2浓度范围为为50-225 mmol/L,反应溶液pH值用HCl调节为5.81-5.97。溶液中钙的主要存在形式为Ca2+,而Ca(OH)2、Ca(OH)+分别是10-13和10-7数量级。由图3可以看出,在低浓度时,反应速率几乎没有变化,较高浓度时速率略有增加。
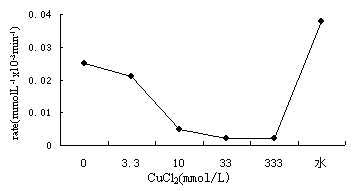
图4 Cu2+对光催化降解阳离子蓝X-GRL的影响
2.4 Cu2+对光催化降解阳离子蓝X-GRL反应速率的影响
Cu2+对光催化降解阳离子蓝X-GRL反应速率的影响见图4。实验CuCl2浓度范围为值是3.3-333 mmol/L。反应pH = 2.51-5.56。在实验的pH范围内,溶液中铜的主要存在形式为Cu2+和Cu(Cl)+,此外还有少量的Cu(OH)+,随着浓度的增加,Cu(Cl)+所占比重有所增加。由图可知,随着铜浓度的增加,光降解速率下降,将失活的催化剂用去离子水冲洗后活性恢复到154%。
2.5 Ni2+对光催化降解阳离子蓝X-GRL反应速率的影响
Ni2+对光催化降解阳离子蓝X-GRL反应速率的影响见图5。实验中NiCl2的浓度范围为3.3-333 mmol/L,反应初始pH = 4.38 -5.46,溶液中镍的主要存在形式为Ni2+,Ni(OH)+很少。由图5可知,当加入3.3 mmol/L时光降解速率上升,但随着镍离子浓度的增加,光降解速率又下降,水反冲洗后,活性恢复到146%。
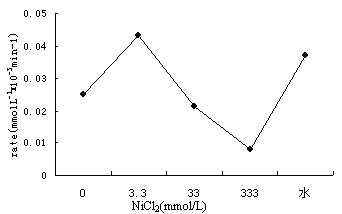
图5 Ni2+对光催化降解阳离子蓝X-GRL的影响
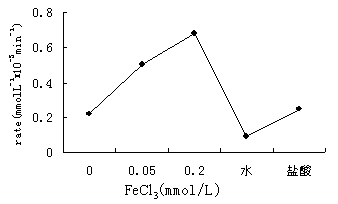
图6 Fe3+对光催化降解活性艳红K-2G的影响
2.6 Fe3+对光催化降解活性艳红K-2G反应速率的影响
Fe3+对光催化降解活性艳红K-2G反应速率的影响见图6。实验FeCl3的浓度为0.05和0.2
mmol/L,反应溶液的pH = 2.73-2.82。在实验的pH条件下,溶液中铁的主要存在形式为Fe3+和Fe(OH)2+,铁的其它羟基配合物或多核羟基配合物所占比重很小,Cl-与铁形成的配合物比重也很小。实验结果如6所示,从图中可以看出,随着铁浓度的增加光降解速率也加快,表面上看这似乎是铁促进了反应的进行。但考虑到即使不加催化剂,铁也有光降解作用[5],这很可能掩盖了Fe3+对催化剂的中毒作用,因此又将失活的催化剂进行水冲洗,发现水反冲洗后的催化剂活性仅为原催化剂的41.3%,这说明铁离子的确是使催化剂失活而不是促进作用,而且经水冲洗活性不能恢复。催化剂经HCl反冲洗后,活性恢复为原来的111%,说明铁在参与光催化反应过程中会有一部分沉积在催化剂表面,对催化剂的活性起了抑制的作用,经HCl冲洗后可被部分激活。
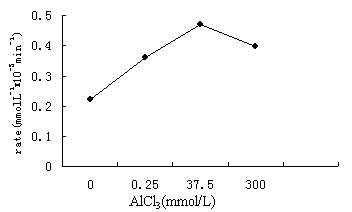
图7 Al3+对光催化降解活性艳红K-2G的影响
2.7 Al3+对光催化降解活性艳红K-2G反应速率的影响
Al3+对光催化降解活性艳红K-2G反应速率的影响见图7。实验AlCl3浓度范围为0.25-300
mmol/L,溶液pH = 2.77-2.82。在实验的pH条件下,溶液中铝的主要存在形式为Al3+,此外有少量的Al(OH)2+。如图7所示,随着铝离子浓度增加,光降解速率明显增加,高浓度时有所降低,但仍比空白值高。
考虑到铝盐本身是很好的混凝剂,可以使水中的颗粒物絮凝从而降低水中有机物的浓度,为了了解它的这种作用有多大,同时做了一组比较实验。实验取37.5
mmol/L的Al3+,不添加催化剂,其它条件同上,结果发现单独铝盐存在时其反应速率仅为0.079
μmol/min,而同浓度Al3+存在时光催化反应速率为0.470 μmol/min,二者之差远大于光催化反应空白值0.219
μmol/min,由此说明Al3+的确促进了光催化反应的进行。
3.1 失活机制的探讨
3.1.1俘获机制
铜离子对光催化降解速率的抑制是因为Cu2+可以捕获电子,而生成的Cu0很不稳定,还可以与价带空穴h+vb或HO·自由基反应[6]:
Cu2+ + 2e- → Cu0
Cu0 + 2h+vb → Cu2+
通过以上两个反应,e-cb,h+vb和HO·自由基这些活性氧化基团会相应减少,因此光降解速率会降低。Ni2+对催化剂活性的影响与Cu2+类似,是通过捕获电子空穴而造成活性降低。在低浓度下观察到Ni2+促进了反应的进行,是因为在较低浓度时Ni2+与电子的作用实际上起了抑制电子-空穴复合的作用。如张颖[7]等发现许多过渡金属离子在低浓度时都会促进光催化反应的进行。在本实验中,Cu2+和Ni2+经过水冲洗后活性可恢复,可见Cu2+和Ni2+没有在催化剂表面产生强吸附,导致催化剂活性降低的主要机制是俘获机制。
3.1.2 表面沉积机制
Mn2+能够导致催化剂中毒,Mn2+能够以离子或金属氧化物的形式沉积在催化剂表面或渗透入催化剂表层[8],在此过程中TiO2表面活性位会受到破坏。催化剂再生后活性恢复的较少,经HCl反冲洗的催化剂为灰色,说明在催化剂表面仍有残留有锰的氧化物(MnOOH或MnO2),锰氧化物对催化剂活性的影响是因为其沉积在催化剂表面时阻塞活性位。Fe3+对催化剂活性的影响与Mn2+类似,主要是通过形成氧化物沉积在催化剂表面,Fe3+对失活的催化剂经过HCl冲洗后活性恢复到111%,可见酸冲洗过程中有活性位被激活。
3.2 Ca2+、Mg2+与Al3+与活性的关系
Ca2+与Mg2+一样,都属于碱土金属离子,电子层饱和而且不具有变价,在溶液中不具备与电子或空穴发生作用的能力。Ca2+与Mg2+也不容易形成金属或金属(氢)氧化物沉积在催化剂表面而影响其活性,同时也没有观察到它们能够吸附在催化剂表面,所以Ca2+与Mg2+对光催化剂的活性影响很小。
Al3+对光催化反应的促进是因为Al3+能作为有效的电子受体,它可以减少了TiO2表面电子-空穴对的复合,从而使TiO2表面产生更多的HO·[9]。 4 结论
实验评价了7种金属阳离子对TiO2/SiO2催化剂光催化降解三种染料化合物活性的影响。结果发现Mn2+对催化剂活性影响最大,造成催化剂部分中毒,经过HCl冲洗活性也仅恢复76.6%。Fe3+通过沉积在催化剂表面占据其活性位而影响活性,水冲洗活性不能完全恢复,但HCl冲洗后活性达111%,可见有活性位被活化。Cu2+和Ni2+使虽然反应速率下降,但它们是通过俘获电子及空穴而导致活性下降,对催化剂本身并没有显著影响。Ca2+和Mg2+均不对催化剂活性产生影响,而Al3+却能够明显促进光催化反应的进行。 REFERENCES
[1] Masakazu Anpo. Pure. Appl. Chem., 2000, 72 (7): 1265- 1270.
[2] Hoffmann M R, Martin S T, Choi W et al. Chem. Rev., 1995, 95: 69-96.
[3] Hu Chun, Wang Yizhong, Tang Hongxiao. Appl. Catal. B: Environ., 2001, 30 (3/4): 277-285.
[4] Tian C R, Wang Y Z, Hu C. Environmental Chemistry (Huanjing Huaxue), 2001, 20 (1): 18-22.
[5] Brand N, Mailhol G, Bolte M. Chemosphere, 2000, 40:395-401.
[6] Zhu Hua, Zhang Manping, Xia Zongfeng et al. Wat. Res., 1995, 29 (12): 2681-2688.
[7] Zhang Ying, Li Z H, Yang L X et al. Research of Environmental Science (Huanjing Kexue Yanjiu), 2000, 13: 40-42.
[8] Robert A Burns, John C Crittenden, David W Hand et al. Journal of Environmental Engineering, 1999, 1: 77-86.
[9] Pan H X, Fu J M, Sheng G Y et al. Research of Environmental Science (Huanjing Kexue Yanjiu), 2000, 13: 300-306.