http://www.chemistrymag.org/cji/2003/053019rc.htm |
Mar. 1, 2003 Vol.5 No.3 P.19 Copyright |
Liu Jindong, Wang Wenji
(Institute of Chemistry & Chemical Engineering , Fuzhou University 350002 )
Abstract Basic and
applying research works on mineral fast ion conductor which lasting more than ten years by
our group are reviewed .Nasicon type FIC was prepared by high temperature solid phase
reaction , used clay mineral as starting material . Three factors affect conductivity :
polarization effect , comparative size between passage and migrating ion , and filling
amount of dopant ion . Reformed montmorillonite ( thereafter refered to as mont. ) was
produced by ion exchange method and molecular substition method. XRD data proves that the
lattice of reformed mont. remain the same as natural mont. Thermal analysis data and
conductivity data show : It is water which is absorbed in surface of mont. that enhanced
migration rate of conducting ion , not water resided between two layer of mont. . Practice
of solid magnesium cell using mont. as electrolyte show : it can serves as power source
for microelectronic device .
Keywords nasicon, montmorillonite, solid state cell
刘景东
王文继(福州大学化学化工学院 350002)
2002
年11月4日收稿;福建省教育厅资助课题(编号JB00103)摘要 本文综述本课题组十余年矿物快离子导体基础、应用研究成果。特别是蒙脱石固体电解质方面的研究成果。
关键词 快离子导体 蒙脱石 固态电池
钠快离子导体Nasicon自1976年被开发以来,人们发现它是一个离子电导率较高的快离子导体,适用于高温钠硫电池。本课题组依据Nasicon的合成原理,通过与Si4+、Zr4+离子半径相近的元素离子进行Si-O四面体取代、Zr-O八面体取代,得到一系列Nasicon型的快离子导体[1-9]。但是Nasicon具有如下缺点:含有ZrO2杂相,合成温度仍偏高;抗钠腐蚀性差。我们发现,使用粘土矿物作起始原料,也可以获得Nasicon型快离子导体 。现对取得的一系列研究成果予以综述。 2 最新研究成果
2.1 改性为Nasicon型快离子导体
人们改造天然矿物加以利用,主要从改型与改性两方面着手。改型就是保护矿物的基本结构不变,只改变其中某些可替代部分。改性则是改变矿物的原有结构,以期建立新的结构。
高岭石结构式Al4[Si4O10](OH)8,属三斜晶系,空间群C1,单网层结构。八面体的“水铝石”型层联系一个四面体Si4O10层的结构,Al3+只充填八面体空隙的2/3,层间无传导离子,不具有离子导电性。
叶腊石Al2[Si4O10](OH)2是一种八面体的“水铝石”型层联系2个四面体Si4O10层的结构。由于[Si4O10]中没有Si被Al代替,结构单元层内电性中和,层间没有其他离子充填,所以不具有传输离子,也就不具有离子导电性。
合成方法是将粘土矿物、钠盐以一定摩尔比研磨混合,经高温固相反应制成。原先没有离子导电性的高岭石和叶腊石经过这样处理后室温电导率达到10-5 S·cm-1数量级,电子电导率∶离子电导率<0.01,晶相结构大多属Nasicon的
经过长期研究,我们发现影响电导率的三个因素:
a. 极化效应:Nasicon直接用Li+交换后,电导率下降。虽然r(Li+)<r(Na+),但Li+极化力大于Na+的极化力,Li+与骨架作用的离子性减小,共价性增大,故电导率下降。Nasicon经两价离子交换后,电导率下降,这是因为Nasicon骨架是阴离子性质,Na+占据能量相近但结晶学不等同的两个位置,而这两个位置又没有占满,故Na+可在这两个位置上迁移,具有快离子导电特性;当Na+被高价金属离子Men+取代后,金属离子与骨架之间库仑引力增大,故电导率下降。
b. 离子通道大小与传输离子的匹配。研究认为,传导离子在离子通道中传输时,存在骨架收缩、离子迁移的协同运动,如虽然Li+离子半径小于Na+半径,但不与Nasicon离子通道相匹配,故经Li+交换的Nasicon电导率下降。
c. 离子的填充数量。制成的粘土矿物快离子导体只有在掺入的杂质离子数量较小时,一般为x≤0.5,具有较好的离子导电性。
与Nasicon相比,Nasicon型快离子导体具有合成温度低(约1000℃),无140-210℃的二级相变,耐水、CO2腐蚀性提高等优点。但缺点也是明显存在的,那就是室温电导率都低于Nasicon,活化能都高于Nasicon。由于锂快离子导体在锂电池应用中的重要性,我们也用粘土矿物作起始原料,通过添加锂盐,制成Lisicon型快离子导体。部分Nasicon型钠快离子导体、锂快离子导体研究数据如表1。
表
1 部分粘土矿物快离子导体的导电特性Table 1. Ionic conductivity characters of some clay minerals fast ion conductor
起始 |
最终产物化学式 |
晶相 |
最佳室温电导率 (S.cm-1) |
电导激活能 (kJ.mol-1) |
文献 |
高岭石 |
Na1+2x+yAlxYbyZr2-x-ySixP3-xO12 |
|
6.92×10-5 |
43.3 |
11 |
叶腊石 |
Li1+3xAlxTi2-xSi2xP3-xO12 |
|
2.02×10-4 | 29.36 |
12 |
叶腊石 |
Li1+3xAlxGe2-xSi2xP3-xO12 |
|
5.30×10-5 | 29.1 |
14 |
高岭石 |
Li1+2x+yAlxYbyZr2-x-ySixP3-xO12 |
|
2.93×10-5 | 49.8 |
10,15 |
1)y=0.5 0.1
≤x≤0.4 2)0<x<0.25 3)0≤x≤0.3 4)y=0.5 0.1≤x≤0.3 2.2 改型蒙脱石(Montmorillonite)为层状快离子导体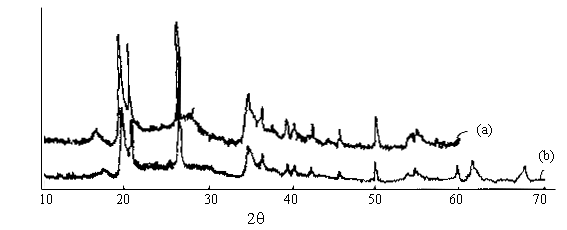
图1 蒙脱石和分子取代法改性的蒙脱石粉末X射线衍射图
Fig.1 Powder X ray diffraction of natural Mont. (a ) and reformed Mont. ( b)
蒙脱石为层状结构,结构式为:(0.5Ca.Na)0.33[(Al.Mg.Fe)2(OH)2(Si2Al)2O10].nH2O,它具有单斜对称结构,空间群为C2/m,晶层沿a.b轴延展,在c轴方向迭置,c轴由于含水分子层高度不同,间距可由0.96到2.14nm。由于四面体中Si和八面体中Al部分被低价离子同型置换,致使晶层带电。由于静电吸引作用,层间吸附一些阳离子和极性水分子。阳离子同水分子结合形成水合离子在层间作准液态运动,因此表现出一定的离子导电性。如Ca基蒙脱石室温电导率为6.57×10-5S.cm-1。
合成方法包括离子交换法和分子取代法。离子交换法:将蒙脱石倾入沸腾的金属盐溶液,充分搅拌,静置、冷却数小时后,倾去废液,换上新液;如此反复三次,用蒸馏水洗涤,50℃烘干。分子取代法:无水MgCl2与蒙脱石按一定重量比称取,使总重量为10g,研磨混匀,置于-5℃环境中进行干湿循环处理15-20次,再于50℃烘干。
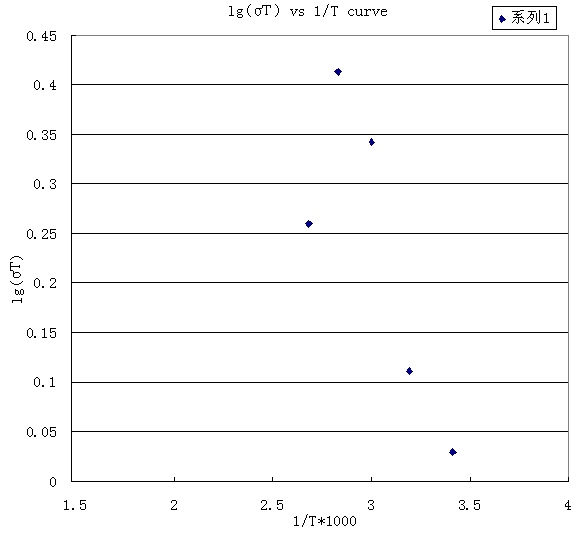
图2 改型蒙脱石log(sT)-1/T曲线
Fig.2 log(sT) vs 1/T curve of reformed mont.
图1的XRD粉末衍射表明,结合在蒙脱石层间的水分子已不具有独立的相,而完全属于蒙脱石母体的相。IR分析表明离子交换、分子取代只是改变层间阳离子和层间分子的性质,没有改变层状蒙脱石母体结构。热分析表明,蒙脱石表面吸附水在高于室温就开始失去,层间结合水在100∽200℃失去,结构水(Al-O(OH))八面体中的-OH在400∽500℃失去。交流电导率数据如表2,电导率随温度变化曲线如图2。离子交换样品电导率最大值出现在60℃,分子取代样品电导率最大值出现在80℃。
表2 部分改型蒙脱石样品的导电特性
Table 2
Conductivity characters of some reformed Mont. samples
样品 |
交流电导 (S.cm-1) |
直流电导 (S.cm-1) |
活化能 (kJ.mol-1) |
文献 |
Mg-Mont. |
7.16 ×10-4 |
1.2 ×10-5 |
19.98 |
* |
MgCl225%-Mont. |
3.65× 10-3 |
5.0×10-5 | 14.79 |
* |
NH4-Mont. |
8.54× 10-4 |
18.39 |
* |
|
H-Mont. |
4.56× 10-4 |
17.93 |
* |
*数据来源:陈静西 福州大学硕士研究生学位论文
σ=Σσk=ΣCkqkμk
σk为k 种离子的电导率,Ck: k种离子的浓度, qk:
k 种离子的电荷,μk: k
种离子的淌度。淌度的大小对电导率的影响很大,在每种体系中都有起主要作用的离子。据此分析,蒙脱石表面的吸附水对离子淌度影响最大,而不是层间水,因为在层间水尚未失去时,电导率就已达到最大值。
2.3 器件方面的应用研究
主要为室温全固态电池的研究。曾组装室温一次镁电池[13]:
Mg│MgCl225%-Mont.│复合正极
MgCl225%-Mont.:经过重量分数为25%MgCl2分子取代后的蒙脱石样品,作为固体电解质。Mg片、Mg粉为负极,正极复合材料由V2O5、乙炔黑和MgCl225%-Mont.按一定重量比均匀混合而成。
负极:xMg=xMg2++2xe
正极:xMg2++2xe+V2O5=MgxV2O5
电池反应:xMg+V2O5=MgxV2O5
在负载为50.7kΩ下放电293小时,平均放电电压1.12V,平均放电容量8.2mAh,电池比能量48.29Wh/kg,表现出良好的电池性能。该电池适用于微功率输出电池。但负载降低时,电池内部极化加重,电池性能下降。怎样降低电极、固体电解质界面阻抗,弄清界面传输的离子特性,提高固体电解质的电化学稳定性,是进一步研究的重要课题。
对于需要微安级放电电流的微功率电子器件是理想电源,我们选择普通液晶显示电子表作为放电负载,这类电子表的耗电情况如下:电压1.8∽1.0V,电流1.6∽0.6μA,平均电流约1.2μA。研究发现放电96天后,输出电压仍维持1.4V。
本课题组曾尝试组装室温二次锂离子电池,发现蒙脱石可能适合于作电池的电极材料。主要是锂离子嵌入和脱出的性能不是很好,致使随循环次数上升,界面阻抗增大,充放电容量降低。深入研究可以从改变改型蒙脱石的锂盐负离子半径的大小入手,以期扩大蒙脱石的层间距,使锂离子容易嵌入和脱出。
(1)发展蒙脱石固体电解质的研究
已研究的矿物固体电解质中,只有改型蒙脱石固体电解质具有较高的室温电导率∽10-3S.cm-1,用蒙脱石固体电解质研制室温固态电池是很有希望的。利用蒙脱石层间间距大,可作为聚合反应的场所,引入聚合物,利用聚合物易成膜的特性,制成电解质隔膜,相信能提高固态电池的性能。
(2)发展蒙脱石锂离子固态电池研究
在蒙脱石电解质中,水在离子导电中起的作用是很大的,但水会对金属锂起腐蚀作用,怎样提高电池反应对腐蚀反应的比例,制成实用的室温固态锂离子电池,是今后课题的重要方向。 REFERENCES
[1] Wang W J, Wang S B, Lu Z L. College Journal of Fuzhou university(natural science) (Fuzhou daxue xuebao), 1986, 14 (4): 84.
[2] Wang W J, Zhang D L, Zhao J Z. College Journal of Fuzhou university(natural science) (Fuzhou daxue xuebao), 1991, 19 (1): 54
[3] Wang W J, Zhang Z B, Ou X Y et al. Solid State Ionics, 1988, (28-30) : 442.
[4] Wang W J, Wang S B, Rao L et al. Solid State Ionics, 1988, (28-30) : 424.
[5] Wang W J, Wang S B, Liu Y B et al. Inorganic Chemistry (Wuji Huaxue), 1987, 3,(2): 12.
[6] Wang W J,Ou X Y , Zhao J Z. Academic Journal on Inorganic Material (Wuji cailiao xuebao) 1989, 4 (2): 151.
[7] Wang S B, Wang W J , Lu Z L. Academic Journal on Inorganic Chemistry (Wuji huaxue xuebao), 1991, 7 (3): 271.
[8] Wang W J ,Wang S B, Liu Y B et al. Inorganic Chemistry (Wuji huaxue), 1986, 4 (2): 1.
[9] Wang W J , Zhang D L ,Zhao J Z, Funtional Material (Gongnen cailiao), 1995, 26 (3): 255.
[10] Cai Z L ,Wang W J. College Journal of Fuzhou university (natural science) (Fuzhou daxue xuebao), 1997, 25 (5): 88.
[11] Zhang Y R, Wang W J. Functional Material (Gongnen cailiao), 2001, 32 (5): 510.
[12] Huang G, Wang W J. Functional Material (Gongnen cailiao), 2001, 32 (5): 508.
[13] Zhang Z B,Wang W J, Li X Y,et al Functional Material (Gongnen cailiao) 1993, 24 (1): 38.
[14] Wang W J, Chen J X, Zhao J Z. Solid State Ionics: Materials and Application edited by B.V.R.Chowdari et al. World Sciecntific, 1992 : 369.
[15] Zhang Y R, Wang W J. Solid State Ionics:Maerials and Application (Edited by B.V.R.Chowdari et al). World Scientific, 2000: 63.