http://www.chemistrymag.org/cji/2003/054032nc.htm |
Apr.1, 2003 Vol.5 No.4 P.32 Copyright |
Liquid-liquid equilibria for ternary mixtures of water, decane and 2-isopropoxyethanol
Yao
Chen*, Renqiang Li and Kazihiro Tamura
(*Department of Chemistry, Jinan University, Guangzhou 510632, China;
Department of Biotechnology, Jinan University, Guangzhou 510632, China; Department of
Chemistry and Chemical Engineering, Kanazawa University, 2-40-20 Kanazawa, Ishikawa
920-8667, Japan)
Abstract The experimental liquid-liquid
equilibria results for the mixtures of 2-isopropoxyethanol, water and decane were measured
at 298.15K The experimental results are further compared with those calculated by an
extended UNIQUAC model. The experimental results are well agreement with the calculated
results.
Key words Extended UNIQUAC model, Surfactant, Ternary liquid-liquid equilibria
2����������Ҵ���ˮ������Ԫ������ҺҺƽ��
*������ǿ�����ͺ�(*���ϴ�ѧ��ѧϵ������ 510632�����ϴ�ѧ���﹤��ϵ������ 510632�������ѧ��ѧ�����ʻ�ѧ��ѧ�ƣ��ձ����� С��Ұ2-40-20 9208667)
2003��1��8���ո�; ��������ѧ�ع���Ա������������2002-247��������Ŀ��
ժҪ
�ⶨ�˿�����������Լ���2����������Ҵ��������ˮ��25oCʱ��ҺҺ��ƽ�����ݣ���������ѧģ�� Extended UNIQUAC ģ����������Щʵ�����ݣ�Extended UNIQUAC ģ�ͳɹ���������2����������Ҵ��������ˮ��ҺҺ����ƽ�⣬ȷ������2����������Ҵ��������ˮ���Һ������ѧ���ʣ�ʵ�����ͼ������ľ��������Ϊ1.01���ؼ��� Extended UNIQUAC ģ�� ������Լ� ҺҺƽ��
���ſƼ��Ľ�������������Դ��������ҲԽ��Խ����Դ�����ѳ�Ϊ���ǹ�ע�Ľ��㡣ʯ����Ŀǰ����Ҫ����Դ������Һ��ʯ���⣬��ɰ������Ҳ����Ϊʯ����Դ���������ҷ�ɢ������ɰ�Ҳ��У�ֻ��ͨ�������ķ������ɣ����п������黯�ķ�ʽ����ȡ��Ϊ���˽��黯��ԭ��������ϵ�ı仯��̬�����о���ͬʱ������ˮ����ˮ������ˮ��Һ�п����γɽᾧ�����������γ��黯Һ�Ľ�����Լ�2����������Ҵ��������黯ʵ�飬Ŀ�����ڿ���ˮ���ͼ�2����������Ҵ�����ģ�������黯ʱ���������ϵ�еĴ���״��������ֵ�Ũ�ȹ�ϵ���˽�������Ϊ��������Һģ��
extended UNIQUAC[1]ģ�͵ļ�������ʵ�������бȽϡ� 1 ʵ��1.1 ʵ���Լ�
���顢 2����������Ҵ��Լ�ˮ�����ձ��ⴿҩ��ҵ��ʽ�����ṩ������ɫ�����������ٷ��ʷֱ�Ϊ99.4% ��99.6%��99.7%�����ǻ��ⶨ�˴������25oCʱ���ܶȣ��������ֵ������ֵ[2]���бȽϣ�����1��
��1 �����298 Kʱ���ܶ�
��� |
�ܶ�[��/����3] |
|
ʵ��ֵ |
����ֵ |
|
ˮ |
0.99704 |
0.99705 |
���� |
0.72636 |
0.72635 |
2����������Ҵ� |
0.89934 |
�� |
1.2 ʵ��װ�ü��ⶨ����
����ֵ�ҺҺƽ�������¶�Ϊ��298.15��0.01��K��ѹ��Ϊ��ѹ�½���,
ʵ��װ����ͼ1��ʾ����ϸ�����μ�����[3]��
ƽ�ⲣ��ƿ�������ڶ��κ���ˮ���У�ƿ��װ��50ml������ֵĻ��Һ��ƿ�����ø���ĵ����ܷ��Է�ֹ��ʪ�����Һ�����ȵؽ���5h������5h���Ա�ȷ���ﵽ���õ�����룬Ȼ������ע�����ֱ�Ӹ�����ȡ����ͨ������ɫ���飨�ձ�����GC-8A���ⶨ��Ʒ����ֵĺ�����
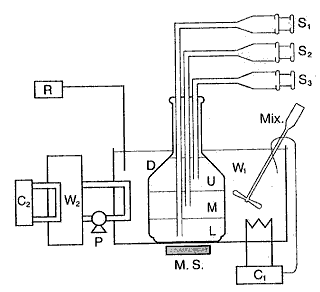
U: ���� S1 S2: ��ע���� P: ���� R: ��¼��
W1 W2: ����ˮԡ�� C1 C2: �ȿ�����
M.S: ���������� D: ƽ�ײ���ƿ
ͼ1 ҺҺƽ���ʵ��װ��ͼ
���о�����Nagata ��extended UNIQUAC ģ��������ʵ�����ݡ���ģ���У�ʣ��Gibbs������gE�Զ���ֻ������Ա�ʾΪ��
���i�Ļ��ϵ����i��Gibbs������gE�Ĺ�ϵΪ��
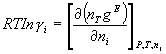 ��2��
��2��ni�����i��Ħ������nT���ܵ�Ħ�������ɷ��̣�2���������صõ����1�Ļ��ϵ�����ı���ʽΪ��
 ��3��
��3��ʽ����λ��ZΪ 10, ����������� �����������������Ķ�Ԫ����ò�����ji�ֱ�������£�
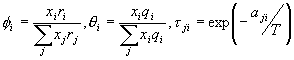 ����
��4��
����
��4��
3 ʵ�����ͷ���
ҺҺƽ���ʵ��������2��ʵ�����������ͼ2��ͼ����ʾ��Ϊ���������ࣩ��
I��Ϊ��ȫ��ϻ���1������II��ΪҺҺ2������III��Ϊ�黯�㡣
��2 ���¶�298K.15ʱ��2����������Ҵ���1�������飨2����ˮ��3����Ԫ��ϵ������Ħ������
���� |
���� |
���� |
||||||
x1 |
x2 |
x3 |
x1 |
x2 |
x3 |
x1 |
x2 |
x3 |
0.0006 |
0.9988 |
0.0007 |
0.2503 |
0.0501 |
0.6996 |
0.0177 |
0.0000 |
0.9823 |
0.0195 |
0.9797 |
0.0008 |
�� | �� | �� | 0.3046 |
0.0000 |
0.6954 |
0.0191 |
0.9803 |
0.0007 |
�� | �� | �� | 0.4212 |
0.0000 |
0.5788 |
0.0380 |
0.9606 |
0.0014 |
�� | �� | �� | 0.5648 |
0.0000 |
0.4352 |
0.0393 |
0.9577 |
0.0030 |
�� | �� | �� | 0.6514 |
0.0103 |
0.3383 |
0.0519 |
0.9476 |
0.0005 |
�� | �� | �� | 0.7285 |
0.0227 |
0.2487 |
0.0506 |
0.9472 |
0.0022 |
�� | �� | �� | 0.7583 |
0.0411 |
0.2006 |
0.1099 |
0.8858 |
0.0043 |
�� | �� | �� | 0.7785 |
0.0725 |
0.1490 |
0.1118 |
0.8861 |
0.0021 |
�� | �� | �� | 0.7767 |
0.1264 |
0.0969 |
0.2844 |
0.7020 |
0.0136 |
�� | �� | �� | 0.5605 |
0.3992 |
0.0403 |
���̣�5���ͣ�6�����ڶ�Ԫ��Һƽ��ļ��㣬��ȫ���ܵĶ�Ԫ��ֵ�����ò����Ĺ��������������ԭ��
[4]�����������Һ��������Զ�����������ͨ���ع�������Һƽ��ʵ���������á�![]() ��5��
��5��
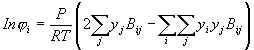 (6)
(6)
���У��ݶ�ϵ�������ɷ��̣�6�������㣬����ֵ�����ѹPS����
Antoine���̼������á�������Rackett����[5]���ڼ��㴿Һ���Ħ�����V L���ڶ�Virial ϵ��Bͨ��Hayden-Oconnell[6]�����ơ�����ַ��ӵ�������������r��q��ȡ��Prausnitz etal[4]����extended UNAQUAC ģ���У�ˮ�������2����������Ҵ���q �ֱ�Ϊ0.96��1.43��0.92������ѧ���̣�7���ͣ�8���������ع�ҺҺƽ�⣬���ֻ��ܵĶ�Ԫ�������õIJ�����ͨ���������̣�7���ͣ�8����á�
���У���Ϊ���ϵ����I��II��IIIָ���ࡣ
��3������extended UNAQUAC ģ�͵Ļع�������Ԫ����ò�������ϸ���㷽���μ�����[7]����Щ��Ԫ����ò���������������ֵ�ҺҺ��ƽ�⡣
��3 ��298.15Kʱ��
Extended UNAQUAC ģ�͵Ļع�����ϵ |
��Ԫ����ò���aji |
|
2����������Ҵ� + ���� |
291.58 |
183.95 |
2����������Ҵ� + ˮ |
1540.30 |
- 980.79 |
���� + ˮ |
2522.20 |
2599.00 |
����ֵ�ҺҺ����ƽ�����������ͼ2����ʵ������ʾ����ͼ2������ʵ������Բ���ʾʵ��㣩��
extended UNAQUAC ģ�͵ļ�������Ƚ��������Զ�����extended UNIQUAC ģ�͵���������ʵ�������Ǻϣ����������extended UNIQUAC ģ��ȷ����������Ԫ��ϵ2����������Ҵ��������ˮ��ҺҺƽ�⣬�Ӷ�Ҳ˵����ʵ����ȷ�ȸߡ���ͼ2���Կ�����ˮ���͡�������Լ��������ȫ�������Ͷ���������Լ��������������ȫ�������Ƚ�С����������������ϴ�������Ϊ1- ������- 2- ����������ˮ�е��ܽ�ȶ���С���¡��˽����ǵ��ܽ�Ⱥ����������������ʯ�ͻ�ѧ��ҵ���������������̵���ƣ���Ϊʯ�Ϳ����ṩ�вο���ֵ�Ļ������ݡ�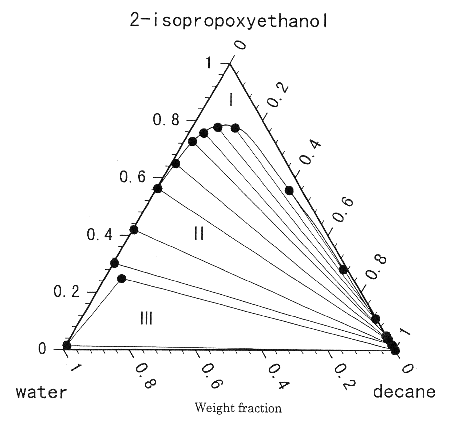
ʵ��tie-line�ߣ�����;Extended-UNIQUAC model�������ߣ�����
ͼ2 ��Ԫ��ϵ2����������Ҵ��������ˮ������ƽ��
REFERENCES
[1] Nagata I. Fluid Phase Equilibria, 1990, 54: 191-206.
[2] Riddick J A, Bunger W B, Sakano T K. Organic Solvents, 4th edn, New York: Wiley
Interscience, 1986.
[3] Chen Y, Tamura K, Yamada T. J. Chem. Thermodyn., 2000, 32: 1597-1605.
[4] Spencer C F, Danner R P. J. Chem. Eng. Data, 1972, 17: 236-241.
[5] Hayden J G, O'connell J P. Ind. Eng. Chem. Process Des. Dev., 1975, 14: 209-216.
[6] Prausnitz J M, Anderson T F, Grense E A, et al. Prentice-Hall: Englewood Cliffs, NJ,
1980.
[7] Tamura K, Chen Y, Tada K, et al. Fluid Phase Equilibria, 2000, 171: 115-126.