http://www.chemistrymag.org/cji/2003/056045nc.htm |
Jun. 1, 2003 Vol.5 No.6 P.45 Copyright |
Zhang Nan, Zhang Xiaoli, Zhao Yunfang
(School of Chemistry and Chemical Engineering, Shandong University, Jinan, 250100,
Shandong, China)
Keywords lomefloxacin(LMF), lomefloxacin- Mg(II)complex, DNA, voltammetry
����ɳ�ǣ�þ�������DNA���õķ�����Ϊ�о�
���
������ ���Ʒ�(ɽ����ѧ�� ��ѧ�뻯��ѧԺ�� ���ϣ� 250100)
2003
��2��1���ո�ժҪ
ͨ������Ԫ��ϵ(����ɳ�ǣ�þ��DNA)�ķ�����Ϊ���о������������������ɳ�ǣ�þ(LMF-Mg(II))�ⶨ������·����� ��NH3 -NH4Cl ������Һ(pH=9.10)�У�LMF-Mg(II)��DNA���ò���һ��������IJ������������ʵĻ�ԭ�壬���λΪ -1.63V (vs.SCE)����������DNA��Ũ�ȳ����ȣ�ctDNA��fsDNA�����Է�Χ�ֱ�Ϊ 5.00´ 10-6��2.20´ 10-5g/mL��1.67´ 10-7��3.67´ 10-7g/mL�� ����ֱ�Ϊ3.30´ 10-6g/mL ��1.00´10-7g/mL ����Ա�ƫ��RSD=3.4% (n = 5)���ؼ��� ����ɳ�ǣ�����ɳ�ǣ�þ�����������
�������Ǻ���
(DNA)��һ�����Ҫ���������ʣ����������Ŵ���Ϣ�����壬��DNA���о���������ѧ�����м�����Ҫ�����ݡ�DNA�ĵ绯ѧ�о��������ں���IJⶨ�������ں���Ľṹ������������ΪDNA����������С�������ʵȵ�������ṩ���ݡ����ں���ĵ绯ѧ�źź�����ֱ�Ӳ���Ч���ϲѡ������������õĵ����ָʾ����Ϊ�ȵ㡣Ŀǰ����������(MX)[1]��TMAP[2]��CuTMAP[3]��ŵ��ù��[4]����ŵù��[5]�������ѱ�֤ʵ��DNA����Ƕ���������ɷǵ�������ʡ����Ļ��ڿ����ؽ��������LMF-Mg(II)��DNA���������µĵ�������ʵ������о�����Ԫ��ϵLMF-Mg(II)-DNA�ķ�����Ϊ���ݴ˽�����һ�ֲⶨ������·�����LMF-Mg(II)��DNA����õ��о����Խ�һ���˽��ŵͪ��ҩ������û����Ͷ����Լ���һ��ҩ�����ƺϳ��кܴ�����塣1 ʵ�鲿��
1��1 ��ѧ�Լ�������
1��2 ʵ�鷽��
ȡһ�����0.08 mol/L��NH3-NH4Cl������Һ(pH=9.10)�ڵ����У�ͨN2����15���Ӻ����μ�������ɳ�DZ���Һ, MgSO4��Һ��DNA��Һ��Ԥ����(ta)60s����ֹ(tr) 30s���缫���(A)Ϊ0.0234�M2��������λEa= -1.20V����-1.20 ~ -1.80V��Χ�ڽ���ɨ�裬��¼�������ǰ��ķ������ߡ�
2 ���������
LMF ��- 1.53V(vs.SCE)����һ�������ķ�(a)������Mg(��)�ļ��룬�� -1.55V(vs.SCE)������һ��������LMF-Mg(II)�����ķ�(b)��DNA�ļ���ʹ�˷彵�ͣ�ͬʱ��- 1.63V������һ���µIJ�����Ļ�ԭ��(c)��c����DNA��Ũ�ȱ仯�����Թ�ϵ�����Ա���ѡ��c����Ϊ�о�����
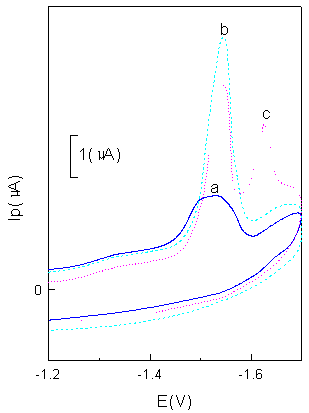
ͼ1 ��ϵ��ѭ������ͼ
0.08mol/L NH3-NH4Cl (pH = 9.10), ta=60s,
tr=30s ,v=100mV/s, A = 0.0234�M2��
LMF (a)��5.00´ 10-6mol/L LMF
LMF-Mg(II) (b)�� (a) +1.25´ 10-5mol/L Mg(II)
LMF-Mg(II)-ctDNA (c): (b)+ 6.00´ 10-6g/mL[ctDNA]. 2��2 ��ѷ�Ӧ������ѡ��
NH3 -NH4Cl����ҺŨ��Ϊ0.08 mol/L��pH=9.10,��Mg(II)Ũ����LMFŨ�ȱ�Ϊ2.5:1��Ea = -1.20Vʱ����(c)��Գƣ�Ip�ϴ�LMF-Mg(II)��DNA 4���Ӻ�Ӧ��ȫ����1Сʱ�ڵ���Ip���ֲ��䡣���⣬���Ÿ���ʱ���������Ip���������������ļ�����ʵ����ѡ����ʱ���Ϊ60s��
2��3 �������ʵ�Ӱ��
�����ʵ�������£��̶� ctDNA��Ũ��Ϊ6.70´ 10-6g/mL���Ը����ᡢ������ȶ��ְ�����ͽ��������ӽ����˸���ʵ�飬����Co2+, Ni2+�нϴ���ţ�����Co2+, Ni2+Ũ��һ��ʱ���ñ����뷨�ⶨ��Ʒʱ��Ӱ��ⶨ�����
3 ����Ӧ��
�����ʵ�������£�ctDNA��fsDNA�����Է�Χ�ֱ�Ϊ5.00´ 10-6-2.20´ 10-5g/mL��1.67´ 10-7-3.67´ 10-7g/mL ������ֱ�Ϊ3.30´ 10-6g/mL ��1.00´ 10-7g/mL, ���Իع鷽�̷ֱ�Ϊ Ip = - 4.532+0.867 C(Ip,mA; C,10-6g/mL) �� Ip= -8.838+0.060 C (Ip, mA; C, 10-6 g/mL), ���ϵ���ֱ�Ϊ0.9989��0.9956���ñ����뷨�ⶨ�ϳ���Ʒ(��Ʒ��MnSO41.00´ 10-6 mol/L , pb(NO3)2 1.00´ 10-5 mol/L, ctDNA(6.70´ 10-6g/mL)��������Ϊ96% -108% , ��Ա�ƫ��RSD=3.4% (n = 5)�� REFERENCES
[1] Liu S H, He P G, Fang Y Z. Chinese Journal of Analytical Chemistry (Fenxi Huaxue) , 1996, 24 (11): 1301.
[2] Qu F, Li N Q, Jiang Y Y. Anal. Chim. Acta.( Fenxi Huaxue Xuebao), 1997, 344 (1/2): 97.
[3] Qu F, Li N Q, Jiang Y Y. Microchemical. Journal (Weiliang Huaxue), 1998, 58 (1): 39.
[4] Ibrahim M S. Anal. Chim. Acta. (Fenxi Huaxue Xuebao), 2001, 443 (1/2): 63.
[5] Chu X, Shen G L, Jiang J H et al. Anal. Chim. Acta (Fenxi Huaxue Xuebao), 1998, 373 (1): 29.
����