http://www.chemistrymag.org/cji/2003/056044nc.htm |
Jun. 1, 2003 Vol.5 No.6 P.44 Copyright |
Shen Jingru, Sun Xiaomei, Lei Zhuolin, Zhu
Yong, Ding Zhigang
(College of Chemistry and Life Science, South-Central University for Ethnic Communities,
Wuhan 430074)
Abstract Catalytic determination of
glucose with mimic glucose oxidase was constructed by the reaction of b-cyclodextrin,
maleic anhydride, chloroactic acid with iron trichloride in hydrogen peroxide. The method
is simple and convenient, and sensitivity and reappearance are ideal. The linear range is
30-197mg·mL-1,
while the detection limit is 4 mg·mL-1, the RSD is 0.98% (n=8). The recovery of
sample is 95.8%-103.1%.
Keywords Glucose, b-Cyclodextrin
derivant, Mimic glucose oxidase, Catalysize to analyse
沈静茹 孙小梅 雷灼霖 朱 用 丁志刚
(中南民族大学化学与生命科学学院,武汉,430074)
2003年4月30日收稿;湖北省自然科学基金资助项目(95160)
摘要 报道了用双[-6-氧-(3-脱氧柠檬酸酯)]-
b-环糊精同三氯化铁构筑模拟葡萄糖氧化酶 (GOD),对葡萄糖进行催化氧化,据此,建立了模拟酶催化法测定葡萄糖的新方法。该法的线性范围为30-197mg·mL-1, 检测下限为4 mg·mL-1, 精密度试验RSD为 0.98% (n=8)。方法用于葡萄糖针剂中葡萄糖含量的测定,回收率为95.8%-103.1%。关键词 葡萄糖, b-环糊精衍生物, 模拟葡萄糖氧化酶, 催化分析
葡萄糖是临床化学中检测的重要指标,目前普遍采用的方法主要有化学发光法[1]、分光光度法[2]、电化学法[3]等。虽然检测手段不同,但几乎都是采用一个相同的反应机理,即葡萄糖在氧化酶的作用下与氧反应转变为葡萄糖酸和H2O2,通过测定O2浓度的降低或H2O2浓度的升高而间接测定[4]。酶试剂较贵,对酸、碱、热不稳定, 反应条件苛刻, 容易失活变性,因此,模拟天然酶的研究是一个很有意义的课题。现在有用金属卟啉化合物[5]或氯化血红素[6]模拟辣根过氧化物酶与葡萄糖氧化反应偶联测定葡萄糖的,尚需与葡萄糖氧化酶偶联才能测定。
我们利用双[-6氧-(3-脱氧柠檬酸酯)]-b-环糊精 (CD) 与三氯化铁形成的配合物模拟GOD,采用邻甲苯胺法[7]测定葡萄糖。该法测定葡萄糖无需特殊条件,灵敏度、重现性较好,线性范围较宽,回收率结果理想,且模拟酶制备简便,费用低廉,易储存,不易失活变性,是一种较理想的新型葡萄糖测定方法。模拟酶制备反应式如下:
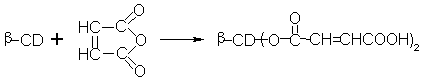
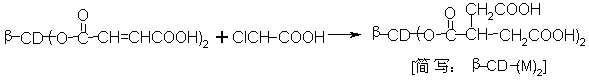
1 实验部分
1.1 仪器与试剂
UV-240 紫外-可见分光光度计,日本岛津;752型紫外光栅分光光度计,上海精密科学仪器有限公司分析仪器总厂;pHS-3C数字酸度计,杭州万达仪器仪表厂;TG-332A微量分析天平,上海分析仪器厂。
葡萄糖标准溶液;0.100 mol·L-1和2.000×10-3
mol·L-1;配合物
1.2 模拟酶b-CD-(M)2·Fe3+·H2O2的制备
取0.1000g配合物b-CD-(M)2·Fe3+溶于9.20 mL二次水中,不断搅拌下加入0.80 mL 30% H2O2,复合30min后制得模拟酶溶液,浓度为6.556 × 10-3 mol·L-1备用。
1.3 模拟酶的催化反应
取6.556×10-3 mol·L-1 模拟酶溶液4.00 mL于一小烧杯中,加2.00 mL水,在不断搅拌下加入0.100 mol·L-1的葡萄糖溶液7.00 mL,将反应温度控制在80℃,并开始计时取样,每隔10 min 用微量取样器抽提50mL反应液,加50mL (0.400 mol·L-1) 邻甲苯胺溶液,混匀,放入80℃的水浴中保温一定时间后,用二次水定容至5.00 mL,以不加底物葡萄糖的溶液为参比,在波长365nm处测定A值。对照实验Ⅰ:用相同量的配合物代替模拟酶;对照实验Ⅱ:用相同量的H2O2 代替模拟酶;对照实验Ⅲ:用相同量的FeCl3与H2O2复合物代替模拟酶。结果见图1。
1.4 测定葡萄糖方法
分别取一定体积2.000× 10-3 mol·L-1葡萄糖标准溶液和一定体积的6.556× 10-3 mol·L-1模拟酶溶液,加入一定体积二次水于恒温 (80℃) 水浴中保温一定时间后,取出冷却至室温,加入一定体积的4.00× 10-4 mol·L-1邻甲苯胺的DMF溶液,放置一定时间后,用水定容至5.00 mL,以不加底物葡萄糖的溶液作对应空白,在365nm 波长处测定吸光度A。 2 结果与讨论
2.1 模拟酶催化法的确定
图1结果表明,随着模拟酶催化葡萄糖反应的进行,吸光度A365值逐渐增加,40min催化反应基本进行完全后出现平台,且模拟酶的催化速率比配合物b-CD-(M)2·Fe3+、FeCl3+H2O2、H2O2快得多。由此建立了用模拟酶催化法测定葡萄糖的新方法。
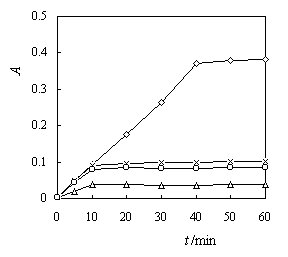
图1 模拟酶催化葡萄糖的动力学曲线
Fig. 1 Catalytic kinetics of mimic glucose oxidase.
System: C模拟酶 = 2.000 × 10-3 mol·L-1; C邻甲苯胺 = 0.200 mol·L-1; t = 80℃
b-CD-(M)2·Fe3+·H2O2 (□); b-CD-(M)2·Fe3+ (△); H2O2 (×); FeCl3+H2O2 (○)
2.2 模拟酶浓度的影响
在具塞刻度试管中加入2.000× 10-3 mol·L-1葡萄糖标准溶液3.00
mL和2.00 mL二次水,6.556×10-3 mol·L-1模拟酶分别取50,100,120,150,200,250,300
2.3 邻甲苯胺显色剂用量的影响
在具塞刻度试管中加入2.000×10-3 mol·L-1葡萄糖标准溶液3.00 mL和2.00 mL二次水,6.556×10-3 mol·L-1模拟酶取100 mL,置于80℃水浴中,50min后取出,冷却后分别取4.00×10-4 mol·L-1邻甲苯胺的DMF溶液120,160,200,240,280,320,360,400 mL,混匀,放置60 min后,以不加底物葡萄糖的溶液作对应空白,测A365值。结果表明,显色剂用量加大,吸光度也增大,当浓度为2.36 × 10-5 mol·L-1时灵敏度达到最大,随后吸光度基本不变,说明显色剂用量已饱和。
2.4 酸度的影响
在具塞刻度试管中加入2.000× 10-3 mol·L-1葡萄糖标准溶液1.50 mL (3.0×10-6mol),6.556× 10-3 mol·L-1模拟酶100 mL (根据模拟酶与葡萄糖最佳摩尔比的量),分别取pH值为3.6,3.8,4.5,5.4,6.2,7.7,8.2,8.8,9.4,10.0缓冲液3.50 mL,置于80℃水浴中,50min后取出,冷却至室温,加入4.00× 10-4 mol·L-1邻甲苯胺的DMF溶液320 mL,混匀,放置60 min后,以不加底物葡萄糖的溶液作对应空白,测A365值。结果见图2,从图中可看出,在最佳反应酸度pH 8.8时A365值最高,大于或小于此值对测定的灵敏度均有不同程度的影响。在pH3.8-4.5之间灵敏度出现另一小峰,这有可能是酸度对模拟酶结构的稳定性[如Fe3+与b-CD-(M)2的配合]和邻甲苯胺的综合影响所致。
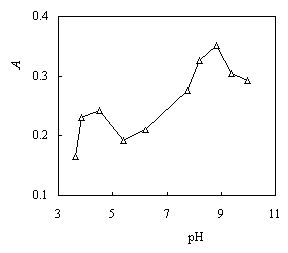
图2 酸度对分析灵敏度的影响
Fig. 2 Effect of pH on analytic sensitivity.
System: C模拟酶 = 1.31×10-4 mol·L-1; C邻甲苯胺 = 2.36×10-5 mol·L-1; t = 80℃
2.5 工作曲线和干扰离子的影响
在选定的最佳条件 (C模拟酶 = 1.31×10-4 mol·L-1,
C邻甲苯胺 = 2.36×10-5 mol·L-1, pH=8.8, t = 80℃)
下进行测定,葡萄糖的浓度在30-197 mg·mL-1之间,线性理想,其线性回归方程为:A=2.4×10-3C–0.0052,线性相关系数
在葡萄糖制剂中,共存的主要是些无机离子,由实验可知,相对葡萄糖量70倍Zn2+、80倍Ba2+、100倍Cl-、K+、Ca2+、Mg2+对测定无干扰,60倍的Al3+对测定干扰严重。
2.6 精密度实验
取一定量被测液,在365nm处测定吸收值,并按回归方程计算。共重复测定8次,结果平均测得量为:(140.6±1.4)mg·mL-1, 相对标准偏差(RSD)0.98%。根据3倍标准偏差计算,最低检测限为4 mg·mL-1。
2.7 样品测定及回收实验
根据工作曲线选定的最佳检测条件,测定5%葡萄糖针剂中葡萄糖含量,按回归方程计算。结果见下表:
表1 试样中葡萄糖的分析结果和回收率
试 样 |
试样含量 |
标样加入量 |
测得总量 |
回收率 |
1 |
59.7 |
22.7 |
83.1 |
103.1 |
2 |
59.7 |
37.8 |
96.7 |
97.9 |
3 |
59.7 |
136.2 |
190.2 |
95.8 |
[1] Zhou Y X, Nagaoka T, Li F et al. Talanta, 1999, 48 (2): 461.
[2] Shi Y, Crouch S R. Anal. Chim. Acta, 1999, 381 (2): 165.
[3] Wang J, Fang L, Lopez D et al. Anal. Lett., 1993, 26 (9): 1819.
[4] Wei SL, Deng G H. Chinese Journal of Analytical Chemistry (Fenxi Huaxue), 2001, 29 (4): 425.
[5] Yao Fengji, Wang L T. Acta Scientiarum Naturalium Universitatis Pekinensis, 1999, 35 (4): 437.
[6] Gao J Z, Yang B. Analytical Laboratory (Fenxi Shiyan Shi), 1998, 17 (6): 35.
[7] Analytical Chemistry Section of Hangzhou University. The Handbook of Analytical Chemistry, 3rd Section, Beijing: Chemical Industry Press, 1983: 562.
[8] Ren W H, Ding Z G, Song F J et al. Chinese Journal of Organic Chemistry (Youji Huaxue), 1998, 18: 66.