http://www.chemistrymag.org/cji/2004/06c092nc.htm |
Dec. 1,
2004 Vol.6 No.12 P.92 Copyright |
(College of Chemistry & Environmental Science, Hebei University, Baoding 071002, China) Abstract The adsorption of Ce(III) on chitosan and crosslinked chitosan was studied in this paper. The effect of various factors such as the time, initial concentration, temperature and pH on the adsorption behavior of Ce(III) were investigated. The results showed that the adsorption of Ce(III) obeyed the Freundlich equation, and the adsorption capacities were improved with the increase of Ce(III) concentration. The optimum conditions of adsorption by chitosan and crosslinked chitosan are: pH in Ce(III) solution was 4.2, time more than 10 h.
Keywords chitosan, crosslinked chitosan, adsorption, Ce(III)
壳聚糖对铈(III)离子的吸附作用
马志广
高俊刚 张雪寒 刘秀英 杜保安
(河北大学化学与环境科学学院 保定
071002)
2004年8月16日收稿
摘要
本文研究了交联壳聚糖及壳聚糖对Ce()的吸附行为,探索吸附时间、金属离子的起始浓度、吸附温度、溶液的pH值等方面对吸附性能的影响。结果表明:壳聚糖交联前后对Ce(III)的吸附均符合Freundlich经验公式;Ce(III)的起始浓度越大,吸附量越高。两种壳聚糖对Ce(III)的最佳吸附条件是溶液的pH值为4.2,吸附时间10
h。
关键词
壳聚糖 交联壳聚糖 吸附 Ce(III)
甲壳素是一类自然界广泛存在的可再生天然资源,壳聚糖(CTS)是甲壳素脱乙酰基的产物,由于CTS分子中有极性基团-NH2等,故它对过渡金属具有很强的螯合能力,所以具有很好的吸附作用,因而在废水处理及金属回收方面得到了广泛的应用。国内外对壳聚糖吸附金属离子方面的研究报道很多[1-3],对稀土金属离子的吸附研究很少[4,5]。将壳聚糖制备成交联壳聚糖(CCTS)微球后,耐酸性增加,且容易与吸附液分离。本文研究CTS及CCTS对Ce(III)的吸附性能,以期为壳聚糖在稀土工业中应用提供理论基础。
1.实验部分
1.1仪器与试剂
pHs-3C型酸度计(上海伟业仪器厂),HZS-D水浴振荡器(哈尔滨东联电子技术开发有限公司)。Ce(NO3)3·6H2O(北京化工厂),壳聚糖
(脱乙酰度>99%,上海伯奥生物科技有限公司,粘度法测定其分子量为4.65×105),其他皆为市售分析纯试剂。
1.2 实验方法
1.2.1交联壳聚糖微球的制备:
参考有关文献[6],稍做改进。称取2.5 g壳聚糖加入25 mL水,搅拌成悬浊液,加入25
mL 6%的乙酸溶液,搅拌至体系透明。在250 mL三颈瓶中加入50 mL的液体石蜡及5滴span80乳化剂快速搅拌0.5
h后慢慢加入CTS溶液,继续搅拌1 h。缓慢滴加5 mL 25%的戊二醛溶液后搅拌20
min。升温到50℃左右,滴加10%NaOH溶液至pH= 9,然后继续升温到70℃,搅拌2
h。趁热过滤,用氯仿洗、乙醇抽提后在80℃烘8 h后得到棕红色CCTS微球。
1.2.2 吸附容量的测定
准确称取一定量的壳聚糖,加入待吸附Ce(III)溶液,置于HZS-D水浴振荡器中恒温振荡,摇速110
r/min。用EDTA络合滴定法测定Ce(III)含量[7](CTS吸附液离心分离后分析),按下式计算壳聚糖对Ce(III)的吸附量:Q
= (C0-C) S/W。
式中C0 、C分别表示Ce(III)的初始浓度和吸附残余浓度(mg/mL),W为吸附剂用量(g),S为吸附溶液的体积(mL)。三次平行实验的测定结果取平均值。
表1 不同时间下Ce(III)的吸附量
Table 1 The adsorption capacities in different
times
时间(h) |
2 |
4 |
6 |
8 |
10 |
12 |
吸附量(mg/g)(CTS) |
20.8 |
26.4 |
32.9 |
39.4 |
44.3 |
45.0 |
吸附量(mg/g)(CCTS) |
14.0 |
24.1 |
29.6 |
35.2 |
40.1 |
40.7 |
2.结果与讨论
2.1 吸附时间对吸附量的影响
壳聚糖0.2 g,Ce(III)初始浓度为1.0 mg/mL,温度25℃,吸附液体积50
mL,改变吸附时间,得到结果见表1。吸附时间不同,吸附量不同。从表3.1可以看出,随着吸附时间的延长,Ce(III)的吸附量也相应的增加,两种壳聚糖对Ce(III)的吸附在10
h左右基本达到饱和。同时可以看到,交联后的壳聚糖对Ce(III)的吸附量比普通壳聚糖有所减小。
2.2 Ce(III)起始浓度对吸附量的影响
壳聚糖0.2 g,温度25℃,吸附液体积为50 mL,吸附时间10 h。Ce(III)的起始浓度不同时,平衡吸附量也会有所不同。随着Ce(III)的起始浓度的增大,平衡吸附量也逐渐增加。
表2 不同起始浓度时Ce(III)的吸附量
Table 2. The absorption capacity in different
initial Ce(III) concentration
Ce(III)起始浓度(mg/mL) |
1 |
2 |
3 |
4 |
5 |
吸附量(mg/g)(CTS) |
44.3 |
75.6 |
101.1 |
125.9 |
153.1 |
吸附量(mg/g)(CCTS) |
40.1 |
65.8 |
87.3 |
105.5 |
123.7 |
如果用吸附量的对数(lnQ)对Ce(III)平衡浓度的对数(lnC)作图(图1)为直线,线性相关系数为:r1=0.9997(CTS),r2=0.9999(CCTS)。这说明壳聚糖交联前后对Ce(III)的吸附都符合Freundlich等温式,壳聚糖对Ce(III)并非仅仅是单分子层吸附。
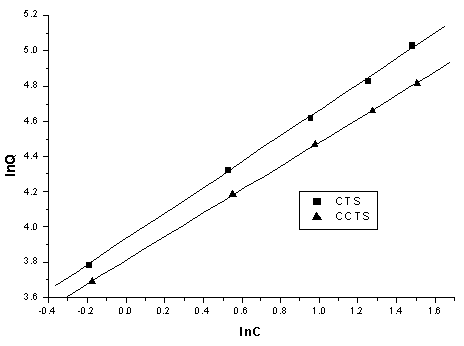
图1 lnQ与lnC关系曲线
Fig. 1 Relationship between lnQ and lnC
2.3温度对吸附量的影响
壳聚糖0.2 g,Ce(III)浓度1 mg/mL,吸附液体积为50 mL,吸附时间10 h,不同温度下Ce(III)的吸附量如表3.3所示。
表3 不同温度下Ce(III)的吸附量
Table 3 The adsorption capacity of CTS
and CCTS at different temperature
温度(℃) |
25 |
30 |
35 |
40 |
45 |
吸附量(mg/g)(CTS) |
44.3 |
43.4 |
45.6 |
47.6 |
48.2 |
吸附量(mg/g)(CCTS) |
40.1 |
41.1 |
40.4 |
37.8 |
40.7 |
从表3可以看出,不同温度下的CCTS对Ce(III)吸附量基本没有变化,CTS对Ce(III)吸附量影响也不显著,这表明温度对Ce(III)的吸附影响不大。
2.4 pH对吸附量的影响
交联壳聚糖0.2 g,Ce(III)浓度1.0 mg/mL,温度25℃,吸附液体积50 mL,吸附时间10
h,溶液的pH不同时,吸附量也会不同,其结果见表3.4
表4 pH值对Ce(III)吸附量的影响
Table 4 The effect of the pH value on the
adsorption capacity of CTS and CCTS to Ce(III)
CTS |
pH |
2.95 |
4.22 |
5.07 |
6.14 |
吸附量(mg/g) |
29.6 |
46.0 |
44.3 |
42.7 |
|
CCTS |
pH |
2.95 |
4.21 |
5.07 |
5.98 |
吸附量(mg/g) |
25.7 |
42.7 |
39.8 |
36.2 |
从表4可以看出,溶液的pH对吸附量有影响。在酸性条件下,吸附量较小。这是因为溶液中的Ce(III)和H+对交联壳聚糖的作用是相互竞争的。当溶液的pH较低时,溶液中的H+浓度很高,H+在竞争中占优势,H+先与交联壳聚糖中的-NH2形成-NH3+,减少了Ce(III)与-NH2络合的机会,所以吸附量比较小;当溶液的pH较高时,H+浓度降低,此时Ce(III)在吸附过程中占优势,优先被壳聚糖吸附,从而吸附量增加。值得一提的是,当溶液的pH值高于Ce(III)的水解pH值时,会产生氢氧化物而不能吸附。考虑到Ce(III)在pH值不到7.00时就已经开始水解,所以控制最大pH在6.00左右。至于对Ce(III)的吸附会在弱酸性条件下4.2左右达到最大值,可能和Ce(III)较易水解的性质有关。
3.结论
无论是否交联,壳聚糖对Ce(III)的吸附都很好地符合Freundlich等温经验式;在实验浓度范围内随着Ce(III)起始浓度增大,吸附量增加;交联壳聚糖比普通壳聚糖吸附量有所降低;温度对吸附量影响不大。交联壳聚糖和普通壳聚糖对浓度1
mg/mL的Ce(III)最佳吸附条件是:溶液的pH为4.2,吸附时间10 h。
REFERENCES
[1] Zhang P, Cai S H, Luo Z C et al. Hydrometallurgy (Shifa Yejin), 1994, 49 (1): 16-20.
[2] Liu Y X, Fan Z R, Sun X H et al. Journal of Shenyang Institute of Chemical Technology
(Shenyang Huagong Xueyuan Xuebao), 2002, 16 (3): 202-205.
[3] Huang W Q,Han L J, Li C X et al. Chinese Journal of reactive polymers, 1998, 8 (1-2):
6-11.
[4] Li J P, Han J H, Song L M et al. Liaoning Chemical Industry (Liaoning Huagong), 2002,
31 (11): 469-471.
[5] Li J P, Song L M. Liaoning Chemical Industry (Liaoning Huagong), 2001, 30 (10):
442-444
[6] Ding M, Shi J J, Huangpu L X, et al. Chemical world (Huaxue Shijie), 1998, 39 (12):
636-640.
[7] The Teaching and Research Section of Analytical Chemistry in Hangzhou University.
Analytical Chemistry Handbook (second edition)(Fenxi
Huaxue Shouce, Di'er Fence) Beijing: Chemical
industry press, 1982.