http://www.chemistrymag.org/cji/2005/07c081nc.htm |
Dec. 2, 2005 Vol.7 No.12 P.81 Copyright |
Zhao Haibo, Xiang Xiaolan, He Jinlan
(Department of Chemistry, Zhanjiang Normal College, Zhanjiang 524048,China)
Abstract In this report, the application of microemulsion electrokinetic chromatography (MEEKC) in the analysis of the enantiomer of the cypermethrin was presented for the first time. By applying chiral reagent, b-CD, the enantiomer of cis-cypermethrin and trans-cypermethrin was baseline resolved in less than 12min and 8min respectively, The separation was carried out in a 50 cm (to the detector)100mm I.D. fused-silica capillary with running voltage 28 kV. Optimum separation conditions were investigated with respect to buffer type and concentration, pH and the composition of microemulsion, the concentration of b-CD and ethanol. This study shows the microemulsions were prepared using relatively lower level SDS (50mmol/L)that could reduce the ionic intension of running buffer, which allowed a higher running voltage(28kV) to be applied, and obtained the higher separation efficiency, and not effected the separation reproducibility. In the experiments, the running buffer was sonicated for10-15 min before use, which could ensure the reproducibility of migration times was in less than 2.5%.
Keywords microemulsion electrokinetic chromatography , cypermethrin , chiral separation
微乳电动毛细管色谱分离氯氰菊酯对映体
赵海波 项小兰 何金兰(湛江师范学院化学系,广东 524048)
2005年11月18日收稿;广东省自然科学基金资助项目(粤科基办[2005]04号)
摘要 首次用b-环糊精添加的微乳电动毛细管色谱,分别在12、8分钟内完成了顺式、反式氯氰菊酯对映体的手性拆分。详细讨论了微乳体系的组成及浓度、b-环糊精浓度及乙醇含量对手性拆分的影响;发现在较低浓度的SDS微乳体系中,不仅能施加高分离电压(28kV),使手性分离快速、高效,而且也能获得高的分析重现性(RSD<2.5%);全文对手性识别机理进行了初步的探讨。关键词 微乳电动毛细管色谱 氯氰菊酯 手性分离
微乳电动毛细管色谱(
Microemulsion electrokinetic chromatography,MEEKC)是近年来得到广泛应用的一种新的毛细管电泳分离技术[1-6]。微乳是由不溶的液体(或称为油滴)形成纳米大小的分散的、均匀的溶液体系。在MEEKC中,油滴被表面活性剂包裹而分散在水的缓冲溶液中,由于表面活性剂和助表面活性剂(一般为短链的醇,如,正丁醇)的存在,使油相和水相之间的表面张力张力趋于0,从而使体系稳定。MEEKC分离是根据溶质的疏水性和电泳淌度两者来分离的,与MECC相似;但在MEEKC中,溶质更容易进入油滴表面,所以,更适于疏水性物质的分离。氯氰菊酯是一类强疏水性的拟除虫菊酯类杀虫剂,其化学名称为(R S)–a–氰基–(3–苯氧苄基)(1R S,3R S; 1R S,3S R)–3–(2,2–二氯乙烯基)–2,2–二甲基环丙烷羧酸酯,分子式为C22H19Cl2NO3;共有8种光学异构体。杀虫活性的强弱与分子构型的手征性有关;其中,顺式氯氰菊酯含有(S)–(1R,3R)和(R)-(1S,3S)两个对映体;反式氯氰菊酯含有(S)-(1R,3S)和(R)–(1S,3R)两个对映体;均为高效体。顺式、反式氯氰菊酯的分子结构见图1。
拆分顺、反氯氰菊酯对映体,用色谱法较多[7,8];用微乳毛细管电泳对上述样品进行手性分离还未见报道。本文采用手性试剂b环糊精(b-CD)添加的微乳电动毛细管色谱,分别在12、8分钟内完成了顺、反氯氰菊酯对映体的手性拆分。全文详细考察微乳组成及手性试剂的浓度对对映体的拆分的影响;并对手性识别机理进行了初步的探讨。
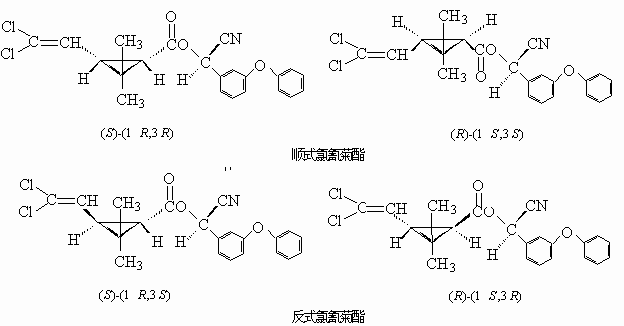
图1 顺式、反式氯氰菊酯的分子结构
Fig.1 The structure of the cypermethrin and its cis-, trans-, isomers 1 实验部分
1.1 仪器和试剂
P/ACETM MDQ毛细管电泳仪(美国Beckman-Coulter公司),紫外(UV-214nm)检测器。未涂层毛细管柱(ID.100 mm,OD.360 mm,总长60.2㎝有效长度50㎝,河北省永年锐丰色谱器件有限公司)。
正庚烷和b-环糊精(天津科密欧化学试剂开发中心);十二烷基硫酸钠(SDS,广州化学试剂玻璃仪器公司);正丁醇(广州新港化工厂);硼砂、磷酸二氢钠、乙醇(汕头光华试剂厂);以上试剂均为分析纯。顺、反氯氰菊酯由中山凯达精细化工厂提供,其纯度分别为95%和93%。实验用水为反渗透去离子水。
1.2 微乳溶液制备及毛细管电泳操作
依次将一定量的SDS、硼砂、磷酸二氢钠、正庚烷、正丁醇混合,超声至溶液透明。
分离电压28kV,进样压力0.4psi,进样时间3s,阴极检测,分离温度20℃。样品用分离缓冲液稀释。所有溶液在进入毛细管仪之前,经0.45mm微孔滤膜过滤。每次电泳前,先用分离缓冲溶液在30psi的压力下冲洗1.5min。
2 结果与讨论
2.1 分离缓冲溶液的组成和pH值的选择
在MEEKC中,高浓度SDS能使微乳稳定,所以缓冲溶液常常使用低离子强度(5~10mmol/L)的硼砂或磷酸盐缓冲溶液及高pH值,使之产生低电流和和适当快速的电渗流(EOF)[1,2]。实验发现氯氰菊酯在pH<6时,EOF速度小,分离时间长,分离峰展宽,分离效率下降;pH>8后,分离重现性差,且有杂峰出现,这可能是菊酯类农药在碱性条件下易分解[9]。所以,菊酯分离pH值在6~7之间比较好。实验中我们发现采用硼砂和磷酸二氢钠的摩尔比为1︰4的混合缓冲溶液,能方便、准确地保证分离体系稳定在pH=6.8,比单独使用硼砂或磷酸盐缓冲溶液的重现性好。为了使分离在高电压下进行,我们采用1mmol/L的硼砂和4mmol/L的磷酸二氢钠组成缓冲溶液。
2.2 SDS浓度对手性分离的影响
SDS是阴离子表面活性剂,其十二烷基渗透进入油滴。SDS的浓度愈高,微滴表面负电荷密度增加,中性溶质容量因子增加,使迁移时间增加[5],如图2所示。从图2可知,SDS浓度达到25mmol/L时,反式氯氰菊酯对映体开始逐渐分离;但是,对顺式氯氰菊酯对映体的分离,SDS浓度至少要50mmol/L。虽然,高含量的表面活性剂能减少微滴表面张力,使微乳体系稳定[4-6],又能改善分离选择性;但是,本研究发现SDS浓度增至70mmol/L时,对映体的分离在30分钟后才完成,且分离峰展宽,分离效率下降。所以,本研究选用SDS浓度为50mmol/L。
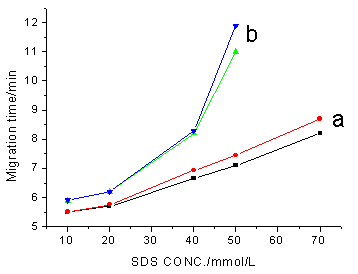
图2 SDS浓度对手性分离的影响
Fig.2 The influence of SDS concentration on the migration time of the enantiomer of the cis-(b), trans- (a) cypermethrin buffer system:in 1mmol/Lborate and 4mmol/L phosphate
a)with 10mmol/L b-CD,17mmol/Lheptane,250mmol/L Butan-1-ol;
b)with 50mmol/L b-CD,34mmol/Lheptane,500mmol/L Butan-1-ol and 15%(v/v)ethanol 2.3 正庚烷浓度对手性分离的影响
正庚烷和辛烷是微乳毛细管电泳中常用的油剂[2,10]。由于正庚烷毒性小,我们选择正庚烷作为油剂。在微乳体系中,油剂作为油相被表面活性剂包裹,形成荷电的油相;溶质在荷电的油相和缓冲水相两者之间的分配而分离;疏水部分进入油相,亲水部分进入缓冲水相。庚烷的浓度增加,氯氰菊酯对映体的迁移时间增加,分离度改善。这是因为样品的容量因子随着正庚烷浓度增加而增加(见图3)。从图3可知,庚烷浓度大于15 mmol/L后,氯氰菊酯对映体的容量因子迅速增加;而且,使顺式、反式氯氰菊酯对映体达到基线分离的最小正庚烷的浓度不一样:存在b-CD和50mmol/LSDS的体系中,17 mmol/L的正庚烷可使反式氯氰菊酯对映体在8分钟内达到基线分离;顺式氯氰菊酯对映体达到基线分离时,正庚烷的浓度至少34mmol/L。可见,没有庚烷存在时,即胶束电动毛细管色谱中,氯氰菊酯对映体达不到基线分离的。
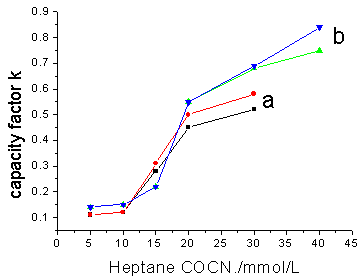
图3 正庚烷浓度与样品的容量因子的关系
Fig.3 Relationship between the retention factor of the cypermethrin and the amount of heptane
Buffer system:in 50mmol/LSDS,1mmol/Lborate and 4mmol/L phosphate,
(a) with 10mmol/L b-CD, 250mmol/L n-butanol (the curve of the enantiomer of trans- cypermethrin);
(b) with 50mmol/L b-CD,500mmol/L n-butanol and 15%(v/v) ethanol (the curve of the enantiomer of cis-cypermethrin) 2.4 正丁醇浓度对手性分离的影响
在微乳体系中,正丁醇作为助剂,使油、水之间的表面张力趋于0,能稳定微乳体系。助剂浓度的变化,对分离选择性没有影响[5]。但是我们发现,随着正丁醇浓度增加,氯氰菊酯对映体的迁移时间增加,分离选择性却明显下降。这可能是随着正丁醇浓度的增加,一部分正丁醇也能进入CD空腔,使待分离组分与CD形成主客体包合物的空间减小,导致手性识别能力下降。可见,助剂浓度对手性拆分的选择性是有影响的。实验发现:使顺、反氯氰菊酯对映体达到基线分离的正丁醇浓度分别为500mmol/L和250mmol/L。
2.5 b-CD浓度对手性分离的影响
b-CD由7个葡萄糖通过a-1,4糖甙键连接而成的筒状化合物,分子的外部呈极性,内腔为非极性,能选择性地与强疏水性化合物形成水溶性较高的主客体包合物,所以,随着b-CD的浓度的增加,与溶质形成的主客体包合配合物的保留时间比未形成主客体包合配合物的溶质要短,分离选择性也应随之提高,实验结果与上述设想完全一致(见图4)。同样,实验发现:使顺、反氯氰菊酯对映体达到基线分离所需要的b-CD浓度分别为50mmol/L和10mmol/L。
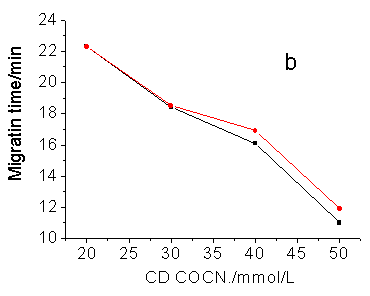
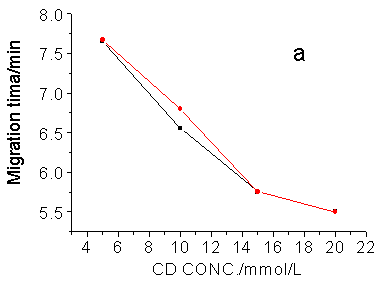
图4 β-CD浓度对手性分离的的影响
在拆分顺式、反式氯氰菊酯对映体的过程中,微乳组成浓度与b-CD的浓度完全不同:在50mmol/LSDS,10mmol/L b-CD,17mmol/L正庚烷,250mmol/L正丁醇和1mmol/L的硼砂、4mmol/L的磷酸二氢钠组成缓冲溶液中,8分钟内反式氯氰菊酯对映体达到基线分离(图5a)。但是,在拆分顺式氯氰菊酯对映体时,缓冲体系中添加乙醇才能在较短的时间内使之达到基线分离,且随着乙醇浓度的增加,组分的保留时间减少,分离度却明显增加(见图5b,4c)。这是因为,有机溶剂可以增加疏水溶质的水溶性,使保留时间减少,提高分辨率[11]。
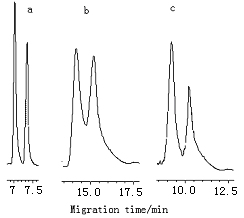
图5 顺、反氯氰菊酯对映体分离
Fig. 5 Separation of the enantiomer of the cis-(b,c), trans-(a), cypermethrin by MEEKC.
Separation conditions:in 50mmol/LSDS,1mmol/Lborate and 4mmol/L phosphate,pH 6.5
a)with 17mmol/Lheptane, 250mmol/L Butan-1-ol and 10 mmol/L b-CD;
b)with 34mmol/Lheptane, 500mmol/L Butan-1-ol 50 mmol/L b-CD and 10%(v/v) ethanol;
c)with 34mmol/Lheptane, 500mmol/L Butan-1-ol and 50 mmol/L b-CD and 15%(v/v) ethanol. 2.7 微乳体系对分离重复性的影响
高含量的表面活性剂减少表面张力,使微乳体系稳定。典型的SDS浓度范围在110mmol/L(3%,w/w)内,其稳定性在几个月内不变。SDS浓度高达6.6%曾经用过[3]。本研究发现高浓度的SDS使微乳体系稳定,但使保留时间增加、分离峰展宽、分离效率下降。本实验采用较低浓度的SDS微乳体系,隔夜后,发现分离重复性下降,但实验发现只要将微乳溶液超声15分钟后再上机,就能保证迁移时间的重现性<2.5%(n=11)。 3 结论
微乳电动毛细管色谱非常适于强疏水性化合物的分离,微乳溶液不仅能使疏水性化合物的容量因子增加,还能够扩大添加剂的使用范围,如本研究中在微乳体系中使b-CD的使用浓度高达50 mmol/L,有利于对映体的分离。另外,本研究采用较低浓度的SDS(50mmol/L)微乳体系,体系的离子强度低,能采用高的分离电压(28kV),可以达到快速、高效的分离目的。 REFERENCES
[1] K D Altria, J. Chromatogr., A 1999, 844:371-377.
[2] H Watarai, K Ogawa, M Abe,et al., Anal. Sci.,1991, (7): 245-252.
[3] L Song, Q Ou, W Yu, et al., J. Chromatogr.,A 1995,699 :371-382.
[4] S Terabe, N Matsubara, Y Ishihama, et al., J. Chromatogr.,1992,608: 23-31.
[5] Y Ishihama, Y Oda, K Uchikawa, et al., Anal.Chem.,1995,67:1588-1595.
[6] M F .Miola, M J Snowden, K D Altria, J. Pharm. Biomed. Anal.,1998, 18:785-792.
[7] 徐秀珠,侯镜德,赵成英. 分析化学,1995, 23(3):310-313.
[8] 王鹏,江树人,周志强. 应用化学,2004,21(1):96-97.
[9] 王箴. 化工辞典,北京:化学工业出版社,2004,p269.
[10] R Szucs, E Van Hove, P Sandra, J. High Resolut. Chromatogr.,1996, 19:189-199.
[11] G. Li, Z. Chen, M. Liu, Z. Hu , Analyst,1998, 123: 1501-1509.