http://www.chemistrymag.org/cji/2009/119042pc.htm |
Sep.1,
2009 Vol.11 No.9 P.42 Copyright |
Chen Guofeng, Dong Xiaoyun, Li Jitai, Bai
Guoyi, Wang Shuxiang
(College of Chemistry and Environmental Science, Hebei University; Hebei Province, Baoding
071002, China)
Abstract A fluorescent probes with
having two dithiocarbamates groups as receptors were designed. The titration experiment
indicated that these probes are highly selective to Hg2+, which shows a
pronounced fluorescence enhancement. It was also found that the response to Hg2+
is a typical PET-suppressed process. The stoichiometry of the probe-metal ion complex was
estimated to be 1:1 by a nonlinear curve fitting of the fluorescence titration.
Keywords fluorescent probe; anthracene; dithiocarbamate;molecular recognition;metal ion.
9,10-二蒽甲基双二乙氨基二硫代甲酸酯的合成及对金属离子的识别作用
陈国锋,董晓云,李记太,白国义,王书香
关键词 荧光分子探针;蒽;二硫代氨基甲酸基;分子识别;金属离子
1 引言
2 实验部分
蒽购自天津市光复精细化工研究所。柱色谱硅胶为青岛海洋化工厂产品 (200-300 mesh),其它合成原料及溶剂均为市售分析纯化学品,光谱测定溶剂均为市售色谱纯溶剂。
核磁共振谱在 Varian Unity-Plus 500MHz 核磁共振仪上测定,TMS 为内标;红外光谱用 BIO-RAD FTS 3000 红外光谱仪测得;紫外光谱用 HP 8453 紫外可见分光光度计测定;荧光光谱在 Varian Cary Eclipse 荧光分光光度计上测定;熔点在 X4 数字显微熔点测定仪上测定 (未做校正)。
2.2 9,10-二氯甲基蒽的制备
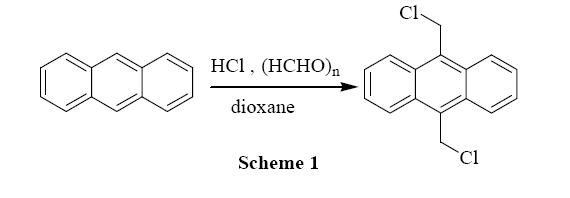
将 120 mL 干燥处理过的 1,4-二氧六环和 20 mL 浓盐酸加入到带有干燥管的 250 mL 三口瓶中,通入新制的干燥氯化氢气体 (浓硫酸滴入氯化钠中制得),待氯化氢气体达到饱和后,加入 15.0 g (84 mmol) 蒽和13.0 g多聚甲醛缓慢搅拌,加热至微沸,继续通入氯化氢气体 2 h。然后停止通入氯化氢气体,缓慢搅拌,保持轻微回流约 3 h后停止加热,继续搅拌 16 h。过滤得到黄绿色固体,用二氧六环多次洗涤,甲苯重结晶得到黄绿色固体 9,10-二氯甲基蒽 13.0 g,产率:56.1%,mp: 257-259℃,[文献值[10]: 258-260℃]。
2.3 9,10-二蒽甲基双二乙氨基二硫代甲酸酯的合成
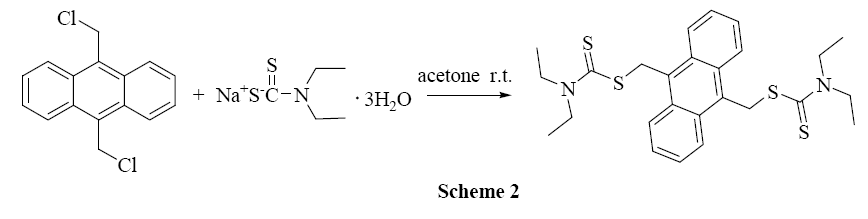
将 9,10-二氯甲基蒽 275 mg (1 mmol),带三个结晶水的二乙氨基二硫代甲酸钠 0.9 g (4 mmol),丙酮 60 mL 加入到 100 mL 的三口圆底烧瓶中,室温搅拌 36 h,TLC 监测底物反应完全,减压蒸除溶剂,往剩余物中加入 50 mL 水,用二氯甲烷萃取,有机相依次用水、饱和食盐水和水洗涤,无水硫酸钠干燥过夜,减压蒸除溶剂,柱色谱分离 (环己烷/二氯甲烷=5:1) 得到黄色固体 0.403 g,收率:80.6%,mp: 165-168℃。
IR (KBr) ν (cm-1) 2974, 2930, 2867, 1675, 1486, 1440, 1416, 1377, 1352, 1266, 1202, 1141; 1H NMR (CDCl3) δ: 8.35 (dd, J1=3.0 Hz, J2=7.0 Hz, 4H), 7.59 (dd, J1=3.0 Hz, J2=7.0 Hz, 4H), 5.46 (s, 4H), 4.12 (q, J=7.0 Hz, 2H), 3.68 (q, J=7.0 Hz, 2H), 1.36 (t, J=7.0 Hz, 3H), 1.21 (t, J=7.0 Hz, 3H);13C NMR (CDCl3) δ: 195.51, 130.63, 127.63, 126.52, 125.32, 49.59, 46.99, 36.46, 12.66, 11.90。
2.4 紫外及荧光光谱的测定
准确称取待测样品,转入50 mL 容量瓶中,用二氯甲烷定容,配制成浓度为1.0×10-3 mol/L 的储备溶液。荧光量子产率测定以蒽 (室温,乙腈中,Ff = 0.36)为参比标准化合物[11]。
移取储备溶液 1 mL 溶于 100 mL 容量瓶中,用 N2 吹干溶剂,用乙腈定容,得浓度为 1.0×10-5 mol/L 的测试溶液。进行金属离子识别筛选。探针的浓度为1.0×10-5 mol/L,分别对 1.0×10-4 mol/L 的 NaClO4、KClO4、Mg(ClO4)2、Ca(ClO4)2、Zn(ClO4)2、Cu(ClO4)2、Co(ClO4)2、Ni(ClO4)2、Fe(ClO4)3、Mn(ClO4)2、Cd(ClO4)2、AgClO4、Hg(ClO4)2 和 Pb(ClO4)2 测定荧光光谱的变化。对筛选出被识别的金属离子,进行浓度滴定,即改变金属离子的浓度,测定相应的荧光光谱和紫外光谱。
3 结果与讨论
在乙腈溶液中,对常见的金属离子 Na+、K+、Mg2+、Ca2+、Zn2+、Cu2+、Co2+、Ni2+、Fe3+、Mn2+、Cd2+、Ag+、Hg2+ 和 Pb2+ 进行了识别试验,研究了主体分子荧光光谱对这些金属离子的响应情况。
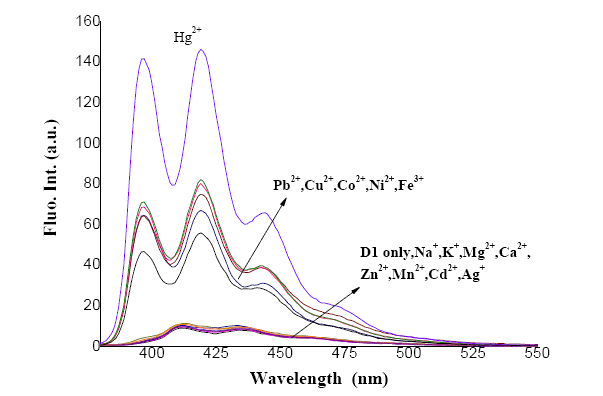
图 1 乙腈溶液中主体分子 (1.0×10-5 M) 的荧光光谱对不同金属离子 (1.0×10-4 M) 的响应
Fig. 1 Fluorescence spectra of host molecule in the presence of 10 equiv. of various metal ions in acetonitrile. [host molecule]=1.0×10-5 M. Excitation wavelength: 365 nm. Bandwidth (Ex): 5 nm. Bandwidth (Em): 5 nm.
如图 1 所示,Na+、K+、Mg2+、Ca2+、Zn2+、Mn2+、Cd2+
和 Ag+ 的加入,对主体分子的荧光光谱基本不产生影响,这可以解释为 DTC 与这类金属离子的配位作用很弱,基本不影响体系的 PET 过程;Cu2+、Co2+、Ni2+、Fe3+ 和 Pb2+
使探针荧光强度增加 (约 7-10 倍);而 Hg2+
的加入使探针的荧光强度增加到原来的 20 倍,发射波长不变。测试结果表明,化合物对 Hg2+ 有较高的选择性,阳离子引起的荧光增强现象归因于主客体之间的相互作用使得体系荧光得以恢复的过程。DTC 既作为电子给体又作为识别基团,使主体分子自身荧光强度下降。Hg2+ 离子加入后,与二乙氨基二硫代甲酸基中的硫原子发生作用,使主体原有的 PET 过程不再发生,从而主体荧光得以恢复,发射强度增加。
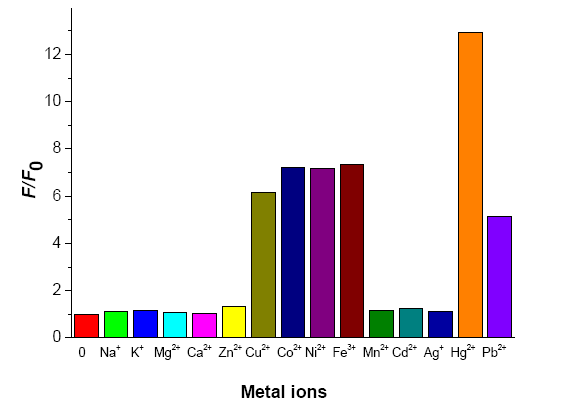
图 2 主体分子 (1.0×10-5 M) 的积分荧光强度对不同金属离子
(1.0×10-4 M) 的响应。柱状图代表加入金属离子后积分荧光强度(F)与加入金属离子前积分荧光强度(F0)的比值(F/F0)。
Fig.2 Integrated
fluorescence response of host molecule (1.0×10-5 M) to various metal ions (1.0×10-4
M). Bars represent the final integrated fluorescence response (F) over the initial
intergtated emission (F0).
相应的荧光强度对比如图
2。由于二硫代氨基甲酸基识别基团与不同金属离子的配位能力,从而使从二硫代氨基甲酸基到蒽的 PET 效应受到不同程度的抑制,探针荧光得到不同程度的增强。二硫代氨基甲酸基与金属离子不同的螯合能力为探针设计中的选择性创造了良好的契机。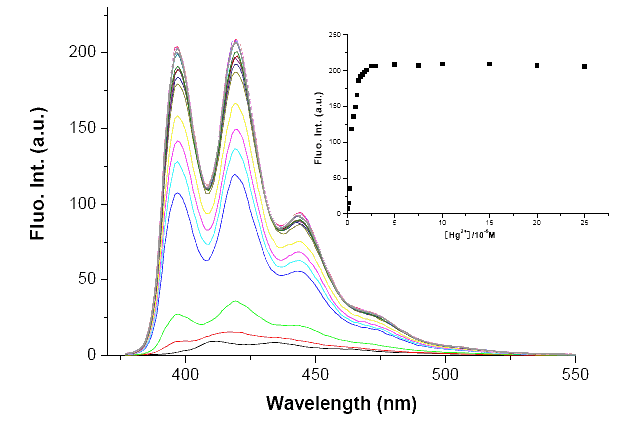
图 3 主体分子 (1.0×10-5 M) 的荧光光谱随 Hg2+ 的浓度的变化,插图是最大发射波长处的荧光强度与 Hg2+ 的浓度的关系
Fig. 3 Fluorescence spectral changes of host molecule (1.0×10-5 M) upon addition of Hg2+ in acetonitrile. Inset: fluorescence intensity at λmax (em) as a function of Hg2+ concentration. Excitation wavelength: 365 nm. Bandwidth (Ex): 5 nm. Bandwidth (Em): 5 nm.
3.2 不同浓度
Hg(Ⅱ) 离子对 D1 荧光光谱的影响在离子筛选试验的基础上,进一步研究了 Hg(Ⅱ) 离子的浓度对主体分子荧光光谱的影响。从图 3 可见,随着 Hg2+ 的加入,主体分子的荧光强度逐渐增大。当加入 1 当量 Hg2+ 后,最大发射波长处荧光发射强度增加到原来的 22 倍。继续增加 Hg2+,荧光强度变化不大。从 419 nm 处荧光强度-Hg2+ 离子浓度变化图显示,主体分子与 Hg2+ 形成 1:1 的配合物,溶液中过量的未结合 Hg2+ 对荧光探针的影响很小。根据 419 nm 处荧光强度-Hg2+ 离子浓度变化图,和公式计算得配合物的稳定常数为1.2×104 M-1,试验结果与典型的 PET 探针性能相符。主体分子对 Hg2+ 的识别作用明显高于 Pb2+、Co2+、Ni2+、Fe3+ 和 Cu2+,是因为前者与 DTC 官能团的配位作用强于后者。
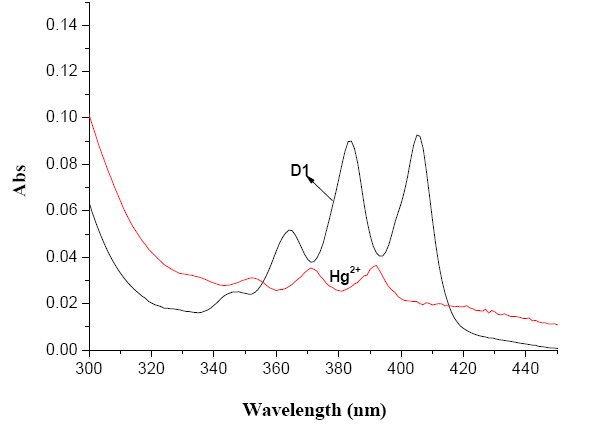
图 4 乙腈溶液中主体分子 (1.0×10-5 M) 的紫外吸收光谱对 Hg2+ (1.0×10-4 M) 的响应
Fig. 4 Absorption spectral changes of host molecule (1.0×10-5 M) upon addition of Hg2+ (1.0×10-4 M) in acetonitrile.
为了更好的解释主体分子
对 Hg2+ 的选择性,我们还测定了主体分子的紫外光谱随着不同金属离子加入后的变化。从图 4 可以看出,加入 Hg2+ 后,蒽的紫外特征吸收发生了明显的降低,并发生蓝移 14 nm。Hg2+ 与主体分子中的 S 原子络合后,降低了 S 原子对蒽环的供电子能力,削弱了荧光团上的电子云密度,增加了电子跃迁所需跨越的能垒,表现在光谱上即吸收波长的蓝移,紫外吸收降低。
根据吸收光谱和荧光光谱的变化,分别计算出原始荧光量子产率和淬灭后的荧光量子产率,主体分子在乙腈中荧光较弱,荧光量子产率值为 0.0023,这很显然归因于光诱电子转移引起的荧光淬灭,加入 Hg2+ 后,PET 效应阻止,荧光量子产率值为 0.12,荧光恢复,荧光量子产率增加。
4 结论
合成了一个以二硫代氨基甲酸基为识别基团含蒽荧光团的分子。通过对不同金属离子的识别试验,该主体分子对 Hg2+ 有较高的选择性,Hg2+ 与二硫代氨基甲酸基配位抑制了 PET 效应,主体分子荧光得以恢复,发射强度增加,并与其形成 1:1 的络合物。
该类探针拓展二硫代氨基甲酸基在分子识别中的应用,在今后的研究工作中,可以将不同的二硫代氨基甲酸基引入体系中,通过改变配位原子的数目和取代基的空间构型来提高响应的选择性。
REFERENCES
[1] He H., Mortellaro M. A., Leiner M. J.
P., et al. Anal. Chem. 2003, 75, 549.
[2] Prodi L., Bargossi C., Montalti M., et al. J. Am.Chem. Soc.2000, 122, 6769.
[3] Tong H., Wang L., Jing X., et al. Macromolecules. 2002, 35, 7169.
[4] Irie M., Fu kaminato T., Sasaki T., et al. Nature. 2002, 420, 759.
[5] Stuhlmann, F.; Jaschke, A. J. Am. Chem. Soc., 2002, 124 (13): 3238.
[6] Lygo, B.; Andrews, A. I. Acc. Chem. Res., 2004, 37 (8): 518.
[7] Ng, S.W.; Kumar Das, V. G.; Tiekink, E. R. T. J. Organomet. Chem., 1991, 403, 111.
[8] Hersh, E. M.; Brewton, G.; Abrams, D. et al., J. Am. Med. Assoc., 1991, 265, 1538.
[9] Cheung, S.-M.; Chan, W.-H. Tetrahedron, 2006, 62 (35): 8379.
[10] Miller, M. W.; Amidon, R. W.; Tawney, P. O. J. Am. Chem. Soc., 1955, 77 (10): 2845.
[11] Martinez-Manez, R.; Sancenon, F. Chem. Rev., 2003, 103 (11): 4419.