http://www.chemistrymag.org/cji/2001/033012pc.htm |
Mar. 1,
2001 Vol.3 No.3 P.12 Copyright |
Jiang Wenhua, Liu Hua, Hu Huijun, Han Shijun
(Chemistry Department of Zhejiang University, Hangzhou, 310027, China)
Received Aug. 13, 2000; Supported by National Natural Science Foundation of China (29736170 and 20076038).
Abstract Based on the
Hadj-Romdhane-Danner mathematical model for solvent diffusing in chromatographic column,
the diffusion coefficients of trace amounts of chloromethane (dichloromethane, chloroform
and carbon tetrachloride) in poly(isobutylene) (PIB) were measured at different
temperatures by packed column inverse gas chromatography. The experimental results
indicate that the diffusion coefficients of the three solvents are related to the
temperature of system and the size of the solvent molecule. It shows that 1) the smaller
the size of the solvent molecule is, the larger the diffusion coefficient is, and 2) the
diffusion coefficient increases with the increase of temperature. Meanwhile, the diffusion
coefficient data measured in this work were investigated by using the Vrentas-Duda
free-volume diffusion coefficient equation. The calculated values of diffusion coefficient
from predictive version of the Vrentas-Duda equation were in good agreement with the
measured data for PIB/carbon tetrachloride system. However, there were large deviations
for PIB/chloroform system due to the neglect of energy effect in the predictive equation.
Keywords chloromethane, poly(isobutylene), diffusion coefficient, inverse gas
chromatography
痕量氯代甲烷在聚异丁烯中的扩散系数研究
蒋文华
刘华 胡惠俊 韩世钧(浙江大学化学系, 杭州, 310027)
2000
年8月13日收稿;国家自然科学基金资助项目(批准号:29736170及20076038)。摘要
采用填充柱反相气相色谱,基于Hadj-Romdhane和Danner所提出的扩散分子在色谱柱中扩散模型,分别测定了不同温度下痕量的三种氯代甲烷溶剂:二氯甲烷、三氯甲烷和四氯甲烷在聚异丁烯膜(PIB)中的扩散系数。实验结果表明溶剂分子在聚异丁烯中的扩散系数与体系温度和溶剂分子的分子大小有关。在相同温度下,溶剂分子越小,扩散系数越大;温度越高,扩散系数越大。同时对所测数据用Vrentas-Duda自由体积扩散系数方程进行了探讨,发现对于PIB/CCl4体系,采用预测型Vrentas-Duda方程计算所得不同温度下的值与实验数据相符,而对于PIB/CHCl3体系计算偏差较大,该偏差产生于预测方程中忽略了能量效应。关键词 氯代甲烷、聚异丁烯、扩散系数、反相气相色谱
小分子在聚合物中的扩散系数是相当重要的物性参数,扩散系数的研究对于更好地研究和利用聚合物材料有着重要的现实意义。测定重量的解吸
/吸收法常被用来测定小分子在聚合物中的扩散系数,但测定所需时间长,而且难于测定含痕量溶剂的高分子浓溶液体系的分子扩散系数。因此在聚合物高浓度区只有少量分子扩散系数数据报道[1],而这个区域的扩散系数数据在聚合物工业尤其是聚合物膜的生产中相当重要。近年来,运用反相气相色谱法研究聚合物高浓度区的分子扩散行为得到很大的发展,因该方法具有简便、迅速的特点且能适用于痕量溶剂的高分子溶液体系。尤其是用于描述填充柱中分子扩散的Hadj-Romdhane-Danner扩散模型的提出,使得痕量溶剂在高分子膜中的扩散系数测定精度得到较大的提高。本文采用此方法测定了不同温度下痕量的三种氯代甲烷在聚异丁烯(PIB)膜中的扩散系数。并采用Vrentas-Duda自由体积扩散方程[2,3]对所测数据进行了讨论。由于担体上所涂高分子膜厚的准确度对扩散系数计算影响很大,故此采用具有较高测定精度Braun和Guillet[4]的方法确定膜厚。
1
实验部分1.1 仪器和装置
采用带有热导检测器的HP1490气相色谱仪(惠普上海分析仪器有限公司)。载气为氢气,由皂膜流量计测定流速,色谱工作站处理流出峰,色谱柱为φ5mm×195cm不锈钢柱。
1.2 试剂和聚合物试样
实验用二氯甲烷(CH2Cl2)、三氯甲烷(CHCl3)、 四氯甲烷(CCl4) 和3-戊酮皆为分析纯试剂,并经精馏后使用,聚异丁烯(PIB)为Adrich试剂(
1.3 色谱柱的准备
采用两种填充柱担体:硅烷化102担体(60-80目,上海试剂一厂)和硅烷化玻璃微珠担体(60-80目,同济大学测试中心)。担体的涂膜是将已溶解好聚异丁烯的苯溶液涂布担体,然后真空干燥,待完全干燥后装入色谱柱。
Table 1. Column characteristics
Support type |
L/cm |
Ws/g (a) |
Wp/g (b) |
102 support |
198 |
5.8067 |
0.3015 |
Glass bead |
198 |
17.4438 |
0.1480 |
(a) weight of support, (b) weight of polymer
1.4 气相色谱实验过程在恒定温度、每一稳定流速下,用10μL的注射器抽取0.4μL小分子试剂,然后在空气中将针抽至6μL。从小流量到大流量依次进样,每一流量重复进样3次。
2 扩散方程及其扩散模型参数的确定
2.1 填充柱中溶剂分子的扩散方程
反相气相色谱法早期所采用的模型是Van
Deemter方程[5,6],但此模型不仅受柱子条件限制,且得出的扩散系数由于包含了小分子在气相中的扩散而其值偏大。而Hadj-Romdhane和Danner[1]提出的模型中同时考虑了小分子在气相和液相的扩散,采用矩分析法处理色谱流出峰,从而修正了流出峰的不规则性,因而能准确地获得小分子在聚合物相中的扩散系数,该模型认为:担体上的膜厚df恒定,在气相和聚合物涂层界面上的热力学平衡为连续,溶质在气相和聚合物相中同时发生扩散,其扩散系数分别为DL和Dp。定义有效塔板高度Heff为![]() (1)
(1)
式中v为载气平均线速度;j、f
分别为James-Martin 和Giddings压缩因子[1];A为多路径因子,A=2b
Dp,b
为填充柱的特征因子;B0为纵向扩散项,B0=2τDm0,τ为扩散不规则因子,取值0.6~1.0[7],Dm0为小分子在色谱柱出口压力下的扩散系数;![]() 为理论塔板高度,μ1、
为理论塔板高度,μ1、![]() 为小分子的平均保留时间和浓度分配变量,其定义式为
为小分子的平均保留时间和浓度分配变量,其定义式为
![]() (2)
(2)
![]() (3)
(3)
这里C(t)为t时刻流出浓度。从而导出小分子在聚合物相中扩散方程为
![]() (4)
(4)
式中Cp、Cg0分别为小分子在聚合物相和气相中的质量传递阻力, 其定义式为
![]() (5)
(5)
![]() (6)
(6)
这里k为容量比,k=Kεp/εg,K 为小分子-聚合物体系的平衡分配常数,εp、εg分别为固定相和流动相的分体积;Rs和Rp分别为担体和高分子膜的半径;kf0为在色谱柱出口压力下流体膜质量传递系数。
采用矩分析处理时间-浓度流出曲线,得到矩方程
![]() (7)
(7)
ta为空气峰流出时间。
2.2
扩散模型参数的确定扩散模型中有六个参量需要确定,即k、B0、A、Cp、Cg0和df。据μ1与ta的关系[式(7)],作线性回归,可得容量比k。采用Fuller-Schettler-Giddings[8]方程可计算不同温度下的Dm0,从而得到B0。A值可由高流速下的色谱数据回归得到,因为在较高的流速下,扩散方程[式(4)]可简化为
据扩散方程[式(4)],以Heff/v对j/f作线性回归,即可得到Cp及Cg0的值。高分子膜厚由Braun和Guillet[4]提出的方法测定:以3-戊酮为探针分子,以涂有高分子膜的玻璃微珠担体为固定相,恒定载气流速50cm/min,在318.2-341.2K温度范围内测定不同温度时探针分子的保留体积,求得本实验中的吸附常数Ka,0和吸附热DH分别为1.26×10-7和-27.78kJ/mol,然后利用小分子在102为担体的填充柱中的保留时间和保留体积数据,求得102柱的特征比表面积Ssp,从而计算得到本实验中102担体上高分子膜厚为4.98×10-5cm。
3
结果与讨论由三种氯代甲烷(CH2Cl2、CHCl3和CCl4)在不同流速和柱温(313.2,323.2,333.2和341.2K)下从涂有PIB膜的102坦体填充柱中流出的色谱数据,分别得到相应的扩散模型参数k、A和B0的值(如表2所示)。 Table 2. Diffusion coefficients of three solvents in PIB at infinite dilution and the corresponding parameters of the diffusion model.
T(K) |
Dp×109(cm2/s) | K |
A (cm) |
B0 (cm/s) |
||||||||
| CH2Cl2 | CHCl3 | CCl4 |
CH2Cl2 | CHCl 3 |
CCl 4 |
CH2Cl2 | CHCl 3 |
CCl 4 |
CH2Cl2 | CHCl 3 |
CCl 4 |
|
313.2 |
3.71 |
0.50 |
0.29 |
1.36 |
3.50 |
6.05 |
5.73 |
10.5 |
23.5 |
1.41 |
1.25 |
1.13 |
323.2 |
7.20 |
0.81 |
0.56 |
1.02 |
2.54 |
4.37 |
3.90 |
6.68 |
15.6 |
1.48 |
1.32 |
1.20 |
333.2 |
8.17 |
1.55 |
0.87 |
0.82 |
1.44 |
3.17 |
2.35 |
4.64 |
10.5 |
1.57 |
1.39 |
1.26 |
341.2 |
10.6 |
2.45 |
1.43 |
1.12 |
2.00 |
2.59 |
1.14 |
2.01 |
6.79 |
1.64 |
1.45 |
1.32 |
图
1给出了CH2Cl2的平均保留时间与空气峰的保留时间的关系,这里认为空气与PIB无相互作用,因此空气峰的保留时间就是载气流出填充柱所需的时间。从图中可以看出在不同的温度下都呈现很好的线性关系,与矩方程[式(7)]相当一致,并由矩方程知,从其斜率可得容量比k的值。在痕量溶剂条件下,式(1)中的理论塔高度可由下式确定式中W1/2为溶剂的半峰宽,tr为溶剂的相对保留时间。结合所得的模型参数A和B0的值,可得到一定温度和流速下的有效塔板高度Heff的值。然后由扩散方程[式(4)]作线性回归,即得扩散方程参数Cp和Cg0的值。图2给出了CH2Cl2/PIB体系在不同温度下扩散方程的回归结果,从其斜率可得参数Cp的值。根据参数Cp的定义[式(5)],由上述得到的模型参数k和膜厚df,可确定痕量溶剂在聚合物中的扩散系数Dp。不同温度下三种氯代甲烷在PIB中扩散系数测定结果列于表2。可以看出,对于同一种溶剂,扩散系数随着温度的升高而增大;在相同的温度下,扩散系数按CH2Cl2、CCl4和CHCl3的顺序递减,这与分子大小顺序相反,因此分子越小扩散越容易。
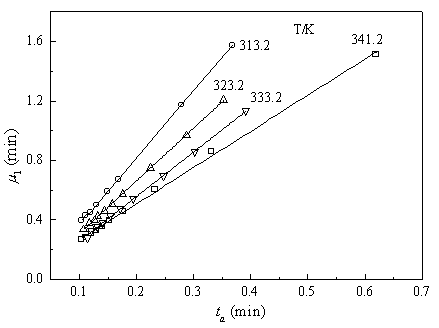
Fig.1 Estimation of the capacity ratio k for PIB-CH2Cl2
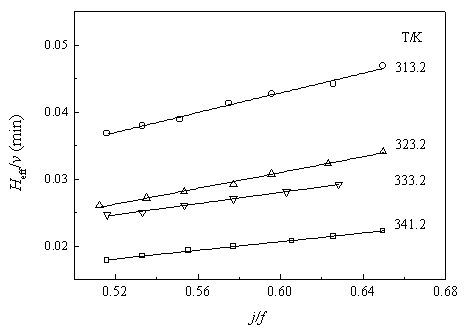
Fig.2 Estimation of Dp for the PIB-CH2Cl2
许多研究者开发了多种理论方程用于描述聚合物
/小分子溶剂体系中溶剂的扩散系数,其中Vrentas-Duda的自由体积扩散系数方程最为成功,它不仅是一个很好的关联方程,而且具有预测能力。下面用该方程对所测定数据进行讨论。在溶剂分子无限稀的情况下,Vrentas-Duda方程可表示为这里
式中
K22=C22 (13)
在纯溶剂条件下,将溶剂分子的Vrentas-Duda扩散系数方程代入Dullien的溶剂粘度-温度关系式可得[10]
式(14)中h1、
式(15)中
V2j=0.0925Tg2+69.47 (16)
由此可估算参数x的值。在预测型的Vrentas-Duda扩散系数方程中,通常忽略能量效应,即假定E*=0。图3给出了不同温度下痕量CHCl3和CCl4在PIB中的稀释扩散系数的预测值与实验值的比较,预测所用自由体积参数列于表3(由于缺乏PIB/CH2Cl2体系的自由体积参数,故该体系未作比较)。
Table 3 Parameters used in diffusion coefficient predictions*
Parameter |
PIB/ CHCl3 | PIB/CCl4 |
1.004 |
1.004 |
|
| K12/g( cm3/g/K) | 2.53×10-4 |
2.53 ×10-4 |
| K22-Tg2(K) | -97.6 |
-97.6 |
| Tg2(K) | 205 |
205 |
| D0( cm2/s) | 5.49×10-4 |
9.77×10-4 |
| x | 0.69 |
0.82 |
| E*(J/mol) | 0 |
0 |
图
3可见PIB/CCl4体系的实验值与预测值吻合较好,相对误差为8.0%,而PIB/CHCl3体系的预测误差相当大,达到227%。究其原因是预测方程中忽略了能量效应。利用表3所列的自由体积参数,可由方程式(10)计算不同温度下的E*,即计算结果如图4所示。显然,对于PIB/CCl4体系不同温度下的E*值落在0.0 J/mol附近,而PIB/CHCl3体系,则在3260 J/mol附近。可见对于前者E*很小,能量效应可忽略,而对于后者E*较大不能忽略。这跟CCl4和CHCl3的分子极性有关,由于PIB和CCl4皆为非极性分子,其分子间的作用力皆为范德华力,因此溶剂CCl4分子间的相互作用能与高分子链段间的相互作用能相差不大,即Ep与Es相近。而CHCl3为极性分子,分子间除范德华力外还有色散力作用,因此PIB/CHCl3体系Ep与Es相差较大,能量效应比较明显。由此可见,预测型的Vrentas-Duda扩散系数方程仅适用于组分分子间相互作用较为相近的体系,对于相互作用相差较大的体系,可利用少量扩散系数的实验数据获取能量参数E*的值,进而预测其它条件下的溶剂分子扩散系数。
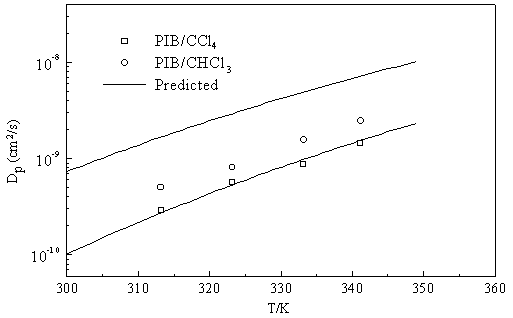
Fig. 3 A comparison of diffusion coefficients between
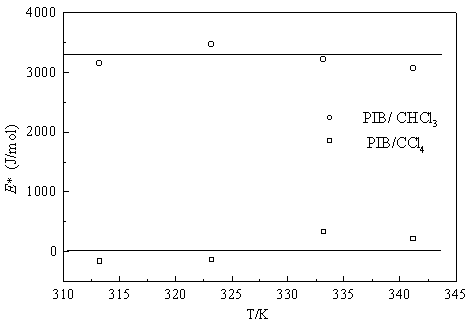
Fig. 4 Calculated values of E* at different predicted values and experimental data. temperatures
4
结论采用填充柱反相气相色谱,基于Hadj-Romdhane-Danner色谱柱扩散模型,测定了痕量CCl4和CHCl3在PIB中的扩散系数。其中PIB/CCl4体系中CCl4在不同温度下的扩散系数实验数据与预测型Vrentas-Duda自由体积扩散系数方程的计算值一致,而PIB/CHCl3体系中CHCl3的扩散系数实验数据与预测值的差别较大,其误差则来自于预测方程中忽略了能量效应,这与实际情况相符。同时也说明了所用实验方法的可靠性和所测实验数据的准确性。 REFERENCES
[1] Hadj-Romdhane H, Danner R P. AIChE J., 1993, 39: 625.
[2] Vrentas J S, Vrentas C M. Macromolecules, 1994, 27: 4684.
[3] Vrentas J S, Duda J L. J. Polym. Sci., Polym. Phy. Ed., 1977, 15: 403.
[4] Braun J M, Guillet J E. Macromolecules, 1975, 8: 882.
[5] Van Deemter J J, Zuiderweg F J, Klinkenberg A. Chem. Eng. Sci., 1956, 5: 271.
[6] Gray D G, Guillet J E. Macromolecules, 1973, 6: 223.
[7] Galin A, Rupprecht M C. Polymer, 1978, 19: 506.
[8] Fuller E N, Schettler P D, Giddings J C. Ind. Eng. Chem., 1966, 58 (5): 19.
[9] Sugden S J. Chem. Soc., 1927: 1786.
[10] Vrentas J S, Vrentas C M. Macromolecules, 1993, 26: 1277.
[11] Hong S U, J. Appl. Polym. Sci., 1996, 61: 833.
[12] Zielinski J M, Duda J L. AIChE J., 1992, 38: 405.