http://www.chemistrymag.org/cji/2001/035019pc.htm |
May 1,
2001 Vol.3 No.5 P.19 Copyright |
Critical concentration of lyotropic liquid crystal for benzyl chitosan
Dong Yanming, Guo Zhenchu#,
Dong Qizhi#, Ruan Yonghong, Wu Yusong
(Department of Materials Science and State Key Laboratory for Physical
Chemistry of Solid Surfaces, Fujian,Xiamen, 361005; #Department of Chemistry, Xiangtan Teachers College, Hunan, Xiangtan, 411100)
Abstract N-benzyl chitosan and N,O-benzyl
chitosan were prepared by different methods respectively. The critical concentration to
form liquid crystal phase in formic acid solution was determined with a polarized optical
microscope. The critical concentration values of both polymers were 11wt%, implying that
critical concentration value of this system was not affected by both degree of
substitution and site of substitution.
Keyword chitosan, benzyl chitosan, lyotropic liquid crystal, critical
concentration.
苄基化壳聚糖溶致液晶的临界浓度
董炎明 郭振楚# 董奇志# 阮永红 吴玉松(厦门大学材料科学系和固体表面物理化学国家重点实验室,福建 厦门 361005; #湘潭师范学院化学系, 湖南 湘潭 411100) 2000年10月25日收稿;国家自然科学基金(批准号29974023)和福建省自然科学基金(批准号Z9910006)资助项目.
摘要 用不同的方法分别合成了N-苄基化壳聚糖和N,O-苄基化壳聚糖,取代度分别为0.20和0.54。用偏光显微镜测定在甲酸溶液中的液晶临界浓度。这两种聚合物的临界浓度均为11wt%,说明取代度和取代位置都不影响该体系的临界浓度值。
关键词 壳聚糖,苄基化壳聚糖,溶致液晶,临界浓度
人们早已认识到不少天然高分子能呈现溶致液晶性
, 例如DNA/RNA, 多肽和纤维素衍生物等。1982年Ogura等[1]最早报道了壳聚糖及其衍生物的溶致液晶性。此后,Sakurai等[2] , Terbojevich等[3]和Rout等[4]都相继对其液晶性进行了研究。虽然壳聚糖的化学结构与纤维素很相似, 但是由于比纤维素多了一个活泼的氨基, 使其衍生物化途径更为多种多样。 壳聚糖成为通过衍生物结构的分子设计研究结构因素对溶致液晶行为影响的理想天然高分子物。 利用它进行的分子量、取代度和取代基大小等结构因素对液晶临界行为影响的研究已先后报道[5-9] ,但对于取代基位置(在氧上或在氮上)的影响尚未有报道。本文用两种合成方法制备了不同取代位置的苄基壳聚糖,比较了它们的液晶临界浓度。1 实验部分
1.1原料、仪器和测定方法
壳聚糖为厦门第二制药厂产品,用酸碱滴定法测得脱乙酰度为84%,用粘度法测得分子量为7.4×105。其余试剂均为化学纯,甲酸的浓度为98%。
Nicolet avator 360型FTIR仪(美国),KBr压片法测定。Olympus偏光显微镜(日本)。CE 1110 CHNS-O 元素分析仪(意大利)。
利用元素分析的C/N比实验值求取代度(DS),计算公式如下:
参照文献[10]N–烷基壳聚糖的合成方法,将5g壳聚糖溶于200mL 1%醋酸溶液中,加入12mL苯甲醛,室温搅拌反应1h。用0.1mol/L NaOH调pH至4.5, 继续反应1.5h。 慢慢滴加入NaBH4溶液(由4.2g NaBH4与10mLH2O配成),还原1h。然后用稀NaOH调pH为碱性,产物被沉淀。经过滤和分别用乙醇和水洗涤数次,干燥得白色粉末产物约6g。
1.3 O,N-苄基化壳聚糖的制备
参考文献[11]O–苄基化甲壳素的相转移合成法,将0.7g壳聚糖,0.1g十六烷基三甲基溴化铵与60mL蒸馏水于40℃下搅拌成糊状,用砂芯漏斗过滤除去水份。然后加入100mL 0℃的20%NaOH溶液,搅拌回流0.5h,过滤;再加入100mL 40%NaOH溶液,于40℃和N2下搅拌回流12-14h。抽滤后将残渣压干,粉碎滤饼。重复碱化与抽滤三次。将最后一次产物于-20℃下冷冻。解冻后得碱化壳聚糖0.75g。
将1.2g碱化壳聚糖,5 mL 1%的十六烷基三甲基溴化铵溶液(用作分散剂)与30mL 40%NaOH溶液混合,于40℃和N2下搅拌反应30min。加入5.9mL氯化苄,于功率为360W的微波炉中反应8h。冷却后抽滤,产物水洗至中性并检查无氯离子。用丙酮脱水,于40℃真空干燥,得1.51g浅黄色固体产物。
1.4 溶致液晶临界浓度的测定方法
在小称量瓶中配制苄基化壳聚糖的甲酸溶液,浓度间隔为1wt%。密封放置5天后,取少许在两玻片之间压成薄层,20℃于偏光显微镜下观察,以刚出现双折射时的最低浓度为形成液晶相的临界浓度。 2 结果与讨论
2.1产物的结构分析
用氯苄和壳聚糖反应来合成苄基化壳聚糖,反应可能同时发生在 O和N上,因而获得O,N-取代的衍生物。合成方程式和产物结构示意式如下:
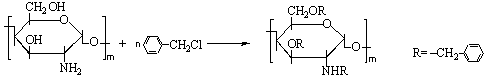
另一方面用如下反应先将壳聚糖转化成壳聚糖的西佛碱,第二步再将西佛碱还原,得到单一的N取代衍生物。合成方程式和产物结构示意式如下:
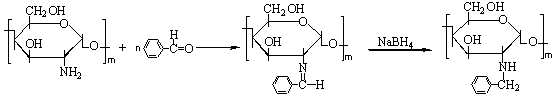
从两者的红外谱图(图1)可见, 都存在约700和740cm-1的单取代苯C-H面外弯曲振动的双峰。此外1600cm-1谱带较强,这是苯环骨架振动和残余-NH2伸缩振动共同作用的结果。图1b 还出现了苯环上C-H伸缩振动的3050cm-1谱带。这些都表明壳聚糖已经发生了苄基化。从O,N-苄基化壳聚糖的NMR谱图(图2)上可以观察到δ=3.39和4.43两个峰, 它们分别归属于Ar-CH2-N<和Ar-CH2-OR的质子[12],表明在O上和N上都有取代。参考苄基化甲壳素的红外定量分析方法[13],若用普通基线法处理红外谱图,以700cm-1为分析谱带,以1650cm-1(酰胺Ⅰ谱带)为内标谱带,所得吸光度比A700/A1650列于表1。表1同时列出元素分析结果。从表1可见O,N-苄基化壳聚糖的取代度是N-苄基化壳聚糖的取代度的2-3倍。
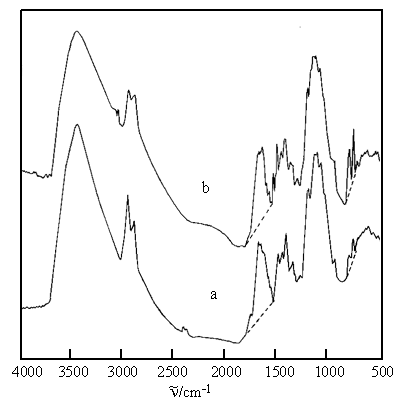
图1 N-苄基化壳聚糖(a)和O,N-苄基化壳聚糖(b)的富立叶红外光谱(基线作法如虚线所示)
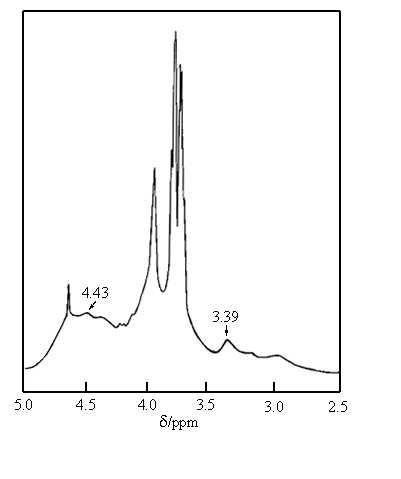
图2 O,N-苄基化壳聚糖的1 H NMR谱图 表1 苄基化壳聚糖的元素分析结果和红外分析结果的比较
衍生物名称 |
取代度 (元素分析) |
A700/A1650 |
N -苄基化壳聚糖 |
0.20 |
0.21 |
O ,N-苄基化壳聚糖 |
0.54 |
0.69 |
苄基化壳聚糖/甲酸溶液的临界浓度值列于表2,表2还列出了未取代之前的壳聚糖原料在同样溶剂中的临界浓度以作比较。
表
2 苄基化壳聚糖/甲酸溶液的溶致液晶临界浓度测定值聚合物名称 |
临界浓度( w/w%) |
取代度 (元素分析) |
壳聚糖 |
5 |
0 |
N -苄基化壳聚糖 |
11 |
0.20 |
O ,N-苄基化壳聚糖 |
11 |
0.54 |
描述刚棒状液晶高分子从各向同性相进入各向异性相的临界体积浓度
V2'主要有Onsager关系式和Flory关系式[14]。Onsager理论给出: V2'=3.3D/L
Flory理论给出: V2'≈6.4D/L
式中D为分子直径,L为分子长度。对于半刚性链,可用库恩链步长或构象保持长度q代替L计算。由于q是链刚性的度量,因而无论Onsager关系式或Flory关系式都说明液晶临界浓度只与链刚性及链直径两种结构因素有关。下面分别从链刚性和链直径两方面来讨论实验结果。
从表2可见,两种苄基化壳聚糖的临界浓度值均高于壳聚糖,原因是苄基取代了原壳聚糖中的氢,破坏了原结构中的分子内或分子间氢键(如图3所示)。这种分子间作用力的削弱引起链刚性减少,从而临界浓度提高。实验表明只需少量取代(如本文中的0.20)就能达到这一目的,而且无论O取代或N取代都可以。
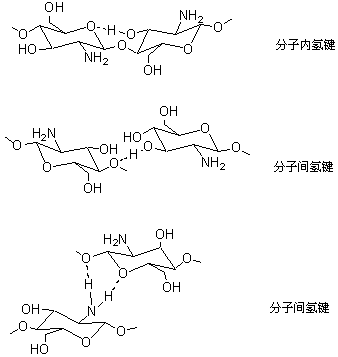
图
3 被取代破坏前的壳聚糖分子内和分子外氢键示意图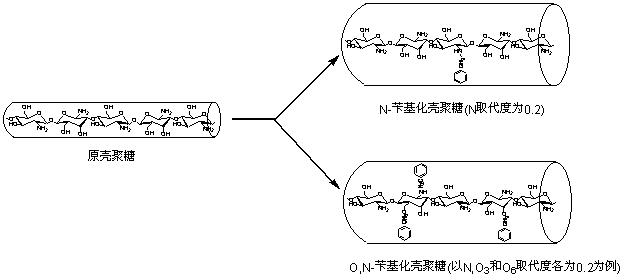
N-苄基化壳聚糖只有一个取代位置,取代度为0.20。O,N-苄基化壳聚糖可能有O3,O6和N三个取代位置,总取代度为0.54,取代度比N-苄基化壳聚糖高得多。实验结果表明两者的临界浓度都是11%。前文[7,8]已经说明了取代度不影响临界浓度,因而本文实验结果说明无论取代发生在N上或O上,取代度并不影响该体系的临界浓度值。这一结果可以用N或O上的苄基化使分子链直径的增加差不多(如图4所示)来解释。
REFERENCES
[1] Ogura K, Kanamato T, Sannan T et al. Chitin Chitosan Proceeding Int Conf 2nd, Tottori,
Japan, 1982, 39.
[2]Sakurai K, Shibano T, Kimura K et al. Sen-i
Gakkaishi, 1985, 41 (9): T-361.
[3]Terbojevich M, Cosani A, Conio G et al. Carhydr.
Res., 1991, 209: 251.
[4]Rout D K, Pulapura S K, Gross R A.
Macromolecules, 1993, 26 (22): 5999.
[5]Wang J W, Dong Y M, Liu H N et al. Chem J Chin
Uni (Gao Deng Xue Xiao Hua Xue Xue Bao), 1999 , 20 (3): 474.
[6]Dong Y M, Wang J W, Wu Z F et al. Acta Polymerica
Sinica (Gao Fen Zi Xue Bao), 1999, (5): 576.
[7]Dong Y M, Wang J W, Mei X F et al. Acta
Polymerica Sinica (Gao Fen Zi Xue Bao), 1999, (6): 668.
[8]Yuan Q, Dong Y M, Wang J W et al. Acta Polymerica
Sinica (Gao Fen Zi Xue Bao), 2000, (1): 5.
[9]Hu Z M, Li R X, Wu D C et al. Acta Polymerica
Sinica (Gao Fen Zi Xue Bao), 2000, (1): 46.
[10]Huang X J, Wang A Q, Yuan G P. Chitin Chemistry
and Application Symposium 2nd. Wuhan, 1999: 199.
[11]Jiang T D. Science Bulletin (Ke Xue Tong Bao),
1984, 29 (13): 792.
[12]Dong Y M. Practical Analysis Techniques for
Polymeric Materials,(Gao Fen Zi Cai Liao Shi Yong Pou Xi ji Shu), Beijing: Chinese
Petroleum Chemistry Press
Zhong Guo Shi Hua Chu Ban She), 1997: 233.
[13]Jiang T, Lu F. Int J Biol Macromol, 1987, (9):
54.
[14]Zhou Q F, Wang X J. Liquid Crystalline Polymers
(Ye Jing Gao Fen Zi), Beijing: Science Press (Ke Xue Chu Ban She) ,1994: 36.