http://www.chemistrymag.org/cji/2001/03a049nc.htm |
Oct. 1,
2001 Vol.3 No.10 P.49 Copyright |
Synthesis and characterization of
complex C60[RuCl2(PPh3)]3
Wu Zhenyi, Cheng Dadian, Yang Sengen,
Zhan Mengxiong
(Department of Chemistry, Xiamen University, Xiamen, 361005)
Abstract A C60[RuCl2(PPh3)]3
has been prepared and characterized by elemental analysis ,FAB-MS, IR , electronic
spectra. and XPS. In addition, its structure has been supposed .
Keywords fullerene Ruthenium complex
C60[RuCl2(PPh3)]3配合物的合成和表征
吴振奕 程大典 林永生 杨森根 詹梦熊(厦门大学化学系 361005 ) 2001年6月18日收稿; 高等学校博士学科点专项科研基金、厦门大学校级自选课题基金资助项目 富勒烯(尤其是C60)独特的结构引起了世界各国化学家及物理学家广泛的兴趣,目前对富勒烯极其化合物的研究范围已迅速扩展[1-3],人们正致力于各类衍生物的结构与性质之间的依赖关系[4,5],以期合成出具有特殊性能的配合物,为富勒烯的实际开发应用奠定基础。富勒烯多金属配合物以其优良的催化性能及光电性能已成为此研究领域的重要组成部分[1-6]。本文合成了C60[RuCl2(PPh3)]3配合物,采用元素分析、质谱、红外光谱、电子光谱及光电子能谱进行鉴定和表征,并推测其结构。 1 实验部分
1.1 C60[RuCl2(PPh3)]3的合成
合成按下列反应进行:
RuCl3+3PPh3
RuCl2(PPh3)3+C60 → C60[RuCl2(PPh3)]3
具体操作如下:二氯·三(三苯基膦)合钌按文献[7]方法合成,产物为乳白色晶体。
称取95.8mg RuCl2(PPh3)3于圆底烧瓶中,利用抽真空装置的高纯氮冲洗装置数次,在保持氮气氛正压的情况下加入20ml甲苯,电磁搅拌使RuCl2(PPh3)3完全溶解,将溶有72mg C60的甲苯溶液300ml倾入分液漏斗中,鼓氮除氧后,将溶液加入烧瓶中,连续搅拌4小时,得到墨绿色溶液,在氮气氛保护下把溶液加热浓缩至20ml,冷却后加入40ml正己烷,有墨绿色沉淀产生,沉淀经正己烷多次洗涤,用甲苯重结晶。真空干燥后得墨绿色粉末,产量92.2mg(以C60计产率45.6%), 产物在氮气氛下保存。与固态相相比,产物的溶液状态更易于被氧化,其甲苯溶液暴露于大气中2 3天后由墨绿色变为棕色。
1.2
产物的表征紫外可见光谱以甲苯为溶剂,在岛津UV 240型紫外可见分光光度计上测得。红外光谱以KBr压片法在Nicolet AVATAR FT-IR360型红外分光光谱仪上测得。采用Carlo Erba 1110型元素分析仪对产物进行元素分析。FAB-MS采用LCQ液相色质联用仪测定。光电子能谱在VG ESCA LAB MK II型能谱仪上测定。 2 结果与讨论
2.1合成反应机理
本文合成过程属于取代反应,与Fagan等人[8]利用C60取代(C2H4)Pt(PPh3)2中C2H4生成C60Pt(PPh3)2的过程相比本反应更易于进行,这是因为本反应中反应物是稳定性较差的非h2型配合物,经取代反应后生成的产物为具有较高稳定性的h2型配合物。反应时C60是以富电子区的C=C双键(6元环与6元环之间)接近RuCl2(PPh3)3的中心金属Ru并提供电子给钌形成s配位键,此时由于RuCl2(PPh3)3中聚集过多的负电荷,拉长并削弱了Ru←PPh3配位键,形成中间过渡态[C60…Ru…PPh3]*,当C60进一步接近Ru时,Ru…PPh3键很快断裂并离解出PPh3,此时C60上的C=C双键上的p*轨道与Ru的d轨道发生重叠,Ru上丰富的d电子反馈到C60的C=C键的p*轨道上,从而削弱并最终打开C=C双键,形成稳定的s-p配位键。
2.2
产物的组成与结构产物的元素分析结果为 C 67.40% H 2.37%, 它与理论值( C 67.64% H 2.22%)基本一致。
从质谱图(图1)可看出,存在质荷比m/z=2022、1951、1920、1819、1760、1724、1376、1345、1296、1285、1273、1166、1136、1058、1034、1013、751、720等一系列峰,其中2022为分子离子峰,720为C60峰,其余峰均为产物在激光作用下裂解与聚合的碎片产生, 这些碎片分别为:C60[RuCl2(PPh3)]2Ru(PPh3)(1951)、(Ph3)C60[RuCl2(PPh3)]2Ru(1920)、(Ph3)C60[RuCl2(PPh3)]2(1919)、C60[RuCl2(PPh3)]2Ru Cl2(1760)、C60[RuCl2(PPh3)]2Ru Cl(1724)、C60Ru (PPh3)2P(1376)、C60Ru (PPh3)2(1345)、(C6H5)C60Ru2Cl(PPh3)(1296)、C60Ru 3(PPh3)(1285)、(2C6H5)C60RuCl(PPh3)(1273)、C60Ru3Cl(PPh)(1166)、(C6H5)C60Ru3Cl(1136)、C60Ru3Cl(1058)、(C6H5)C60Ru3Cl(1034)。
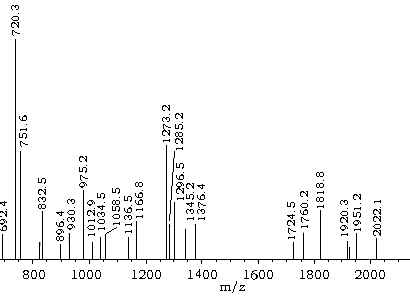
Fig.1 The mass spectroscopy of samples
C60与RuCl2(PPh3)3反应生成C60[RuCl2(PPh3)]3后电子光谱变化十分明显,产物在可见光区有三个吸收峰,分别在400(e=2.17×103L·mol-1·cm-1)、510(e=723L·mol-1·cm-1)及630nm(e=434L·mol-1·cm-1)处,这是由C60分子的HOMO→LUMO跃迁引起的,这三个吸收峰在C60电子光谱中没有出现。这是因为在单纯C60中该跃迁为禁阻跃迁,当C60分子打开C=C双键与Ru形成C60金属配合物后,C60分子由原来的Ih对称性变为D3h对称性,从而使该跃迁由禁阻跃迁变为允许跃迁,证明配合物中C60是以h2形式与金属形成s-p配合物[9]。
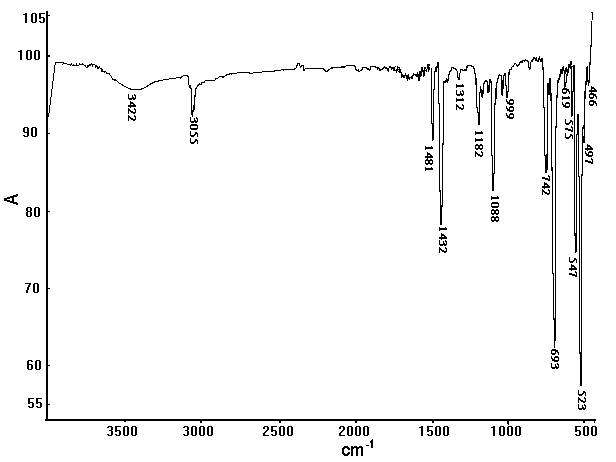
Fig.2 IR Spectra For C60[RuCl2(PPh3)]3
从图2红外光谱也可得到类似的结论。与反应物RuCl2(PPh3)3相比,产物在575cm-1处出现一新的吸收峰,这是产物中C(C60)-Ru振动产生的。产物PPh3苯环上的C-H振动吸收峰出现在3055 cm-1处,与中间物RuCl2(PPh3)3吸收峰(3051cm-1)相比往高波数方向移动了3cm-1,说明在形成配合物后配体苯环上的p电子密度升高,这主要是由于在C60Ru[Cl2(PPh3)]3分子中发生了超共轭作用,使得在C(C60)- Ru-P-C(Ph)-H上电子云密度加大,也即增加了苯环C-H上p电子云密度。另外配位的结果还使反应物RuCl2(PPh3)3在543和518 cm-1处振动吸收频率向高波数方向移动4和5cm-1,而在1314和1189cm-1处吸收峰分别向低波数方向移动2和7cm-1。
 |
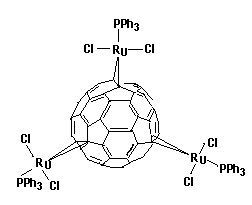 |
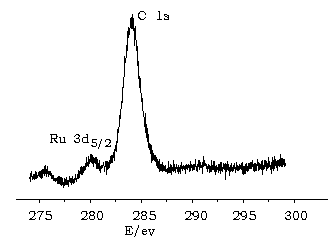
Fig3 XPS for C and Ru of C60Ru[Cl2(PPh3)]3 |
Fig.4 Diagram for structure C60[RuCl2(PPh3)]3 |
由光电子能谱的数据可知,产物中Ru3d5/2结合能为280.3ev,比单质Ru3d5/2结合能高0.3ev,而比两价的Ru(NH3)5(MeCN)Br2低0.4ev,说明产物的中心金属Ru的价态处于0~2价。产物的C1s结合能为283.9ev,与石墨相比低0.4ev,说明产物中的C60的C呈负价态,这主要是因为形成配合物后,金属在接受C60的C=C双键的配位电子对的同时向C60反馈大量电子,从而使金属Ru呈正价态。对产物的Ru3d5/2和C1s的谱峰面积(分别为A C、A Ru )进行积分,求得A C:A Ru≈40:1 ,说明分子中的C原子个数nc和Ru原子个数n Ru的比值约为40:1。
Table 1 Ru3d5/2 and C1s data of compounds| Samples | Binding | Energy |
| Ru3d5/2 | C1s | |
| Ru | 280.0 | |
| Ru(NH3)5(MeCN)Br2 | 280.7 | |
| RuCl4 | 281.7 | |
| WC | 282.6 | |
| C(石墨) | 284.3 | |
| (CH2)n | 284.6 | |
| C60Ru[Cl2(PPh3)]3 | 280.3 | 283.9 |
从以上分析可推测产物的结构如图4,中心金属为五配位,其中两个Cl占据轴向的两个配位位置,Ru与C60以h2形式形成配合物,即C60上的C=C双键(六圆环与六圆环之间)象烯烃那样与Ru以s-p键合,也就是说碳碳双键的两个端点占据两个配位位置。最后一个配位位置被PPh3所占据,三个RuCl2(PPh3)基团均匀分布在C60周围,整个分子基本上呈D3h空间构型。
REFERENCES
[1] Lin Yongsheng,Wu Zhenyi,Zhan Mengxiong et al. Chemistry (Huaxue Tongbao), 1996,
(9): 5.
[2] Muraoka T, Asaji H, Yamamoto Y et al. Chemical Communications, 2000, 3: 199-200.
[3] Zanelo P, Laschi F, Fontani M et al. Journal of Organometallic Chemistry, 2000, 594:
7-1.
[4] Zanello P, Laschi F, Cinquantini A et al. European Journal of Inorganic Chemistry,
2000, (6): 1345-1350.
[5] Song L C, Liu J T, Hu Q M et al. Organometallics, 2000, 19 (9):1643-1647.
[6] Song H J, Lee K P Park, Chang H Y et al. Journal of Organometallic Chemistry, 2000,
599 (1): 49-56.
[7] Hen Shoushan, Zhang Zhengzhi,Wang Xukun et al. Handbook of Synthesis of
Metallo-organic Compounds (Jin Shu You Ji Hua He Wu He Cheng Shou Ce), Beijing:
Chem.Industry Press,1986, 58.
[8] Fagan P J, Calabrese J C, Malone B. Science, 1991, 252: 1160.
[9] Ishii Y, Hoshi H, Hidai M. Chem. Lett., 1994, 4: 801.