http://www.chemistrymag.org/cji/2003/055042pc.htm |
May 1, 2003 Vol.5 No.5 P.42 Copyright |
Liang Ju, Cai Ruxiu, Lin Zhixin, Wang Jun
(College of Chemistry & Molecular
Science, Wuhan University, 430072 Wuhan, China)
Abstract The effect of
peroxynitrite on the chemical oscillating system (LA-Act-BrO3--Mn2+-H2SO4)
was studied based on the APP technique in this paper. The oscillating amplitude changes
linearly with the concentration of peroxynitrite, whereas the period changes irregularly.
The oscillating system is so complicated that we perfected the experimental circumstances
and studied the dynamical mechanism after the injection of peroxynitrite. A new method for
the quantitative determination of peroxynitrite was proposed, which is real time, dynamic,
rapid, and simple.
Keywords chemical oscillating reaction, CSTR, APP, peroxynitrite
(武汉大学化学与分子科学学院 湖北武汉 430072) 2003年3月4日收稿;国家自然科学基金资助项目(NO.20075018) 摘要 本文利用APP技术研究了过氧亚硝酸阴离子对化学振荡反应(LA-Act-BrO3--Mn2+-H2SO4)的影响。发现不同浓度的过氧亚硝酸阴离子与振荡的振幅改变之间有着很好的线性关系,而周期的变化在不同的浓度范围之内有不同的规律。鉴于振荡体系复杂的动力学行为,我们对实验条件进行了优化,并对过氧亚硝酸阴离子加入后的作用机理进行探讨。分析了种种实验现象后,我们提出了一种新的定量检测过氧亚硝酸阴离子的方法,同时解析了相关的非线性表征。本法具有实时﹑动态﹑快速﹑简便的特点。
关键词 化学振荡反应 CSTR APP技术 过氧亚硝酸阴离子
过氧亚硝酸阴离子(ONOO-)在体内是由一氧化氮(NO)和超氧阴离子(O2.-)通过一个扩散控制的反应而形成,因此ONOO-在调节NO和O2.-的二者浓度和生物学效应中起着关键作用,这使得ONOO-成为具有重要生理学功能的中心物质[1]。作为一种强氧化剂,过氧亚硝酸阴离子能够与多种生理物质发生氧化还原反应。有证据显示,在各种细胞的损伤中都伴随着过氧亚硝酸阴离子的形成,如心肌缺血细胞﹑肺损伤细胞﹑炎症细胞﹑癌症细胞甚至包括肝脏细胞等等[2]。
可见,过氧亚硝酸阴离子是直接参与了生物体内的细胞损伤过程,与多种疾病相关联。但是由于过氧亚硝酸阴离子高度活泼的反应性以及在生理条件下的不稳定性,因此在过去的很长一段时间内,对过氧亚硝酸阴离子的检测一直是一件非常困难的问题。到目前为止,对过氧亚硝酸阴离子的检测主要有探针法和印迹法,但这两种方法都不能直接检测过氧亚硝酸阴离子,而且不能提供准确无误的结果来证实过氧亚硝酸阴离子的存在以及对它做定量分析。化学振荡是当化学反应系统处于远离平衡的条件下,由于反应系统中各种非线性过程的相互作用而呈现出的一种极其复杂的动力学行为。因其内部的时空序列形态十分类似于发生在生物体内的生物振荡和生物形态现象,从而引起了广大科学工作者的浓厚兴趣[3-6]。从二十世纪五十年代BZ振荡反应的发现到九十年代CSTR(Continuous-flow stirred tank reactor)和APP技术的引入,化学振荡的研究呈现出了繁荣景象,同时促使振荡反应的应用从无机离子的测定迅速扩大到生物和医药领域[7-9]。CSTR的引入保证了体系远离平衡状态,而生命活体总是处于非平衡非线性的运动状态,从这种意义上说正是模拟生命活体非线性动态的有力工具。1995年以来,APP技术[10]和流动注射(FI)[11]的提出为化学振荡在定量分析方面的应用开辟了新的前景。为此,本文用化学振荡反应结合APP(Analyte Pulse Perturbation Technique)技术提供了实时﹑动态和定量检测过氧亚硝酸阴离子的可能性。 1 实验部分
1.1 过氧亚硝酸阴离子的制备(文献[12]的方法)
用KNO2溶液和硫酸酸化的H2O2反应来合成过氧亚硝酸阴离子:将硫酸酸化的H2O2(25ml含1.5ml 30%的H2O2和0.4ml 98%的H2SO4)快速加入到KNO2溶液中。然后加入强碱性的NaOH溶液(50ml含2.5克NaOH)。加入0.4克MnO2以除去过量的H2O2。产物用0.3M的NaOH溶液稀释,然后放在冰箱中保存。合成液在302nm处检测其紫外吸收确定过氧亚硝酸阴离子的浓度为4-7×10-4mol/L。
1.2 实验试剂
实验中所用的LA﹑Act﹑MnSO4﹑KBrO3及H2SO4均为分析纯,水为经二次蒸馏的离子交换水。LA﹑Act﹑MnSO4﹑KBrO3均用一定浓度的H2SO4溶液按实验要求配制成一定浓度的溶液。
1.3 实验装置及实验步骤
化学振荡在20ml自制的CSTR(连续流动搅拌釜式反应器,continuous-flow stirred tank reactor)中进行,反应液储备在恒温夹套玻璃反应器内与恒温水浴(CS501超级恒温器,重庆银河实验仪器有限公司)相连。试剂由蠕动泵(Masterdlax, Cole-Pammer Instrument)输入CSTR,4条流路分别为反应试剂LA﹑Act﹑MnSO4﹑KBrO3。过氧亚硝酸阴离子直接用微量进样器注入CSTR中与反应体系混合,从而与振荡体系相作用。振荡反应过程电位变化由自制的光亮Pt电极和217型饱和甘汞电极指示,PH3-3C型精密酸度计(上海雷磁仪器厂)和Type3056型垂直式记录仪(四川仪表四厂)指示并记录E-t曲线。实验温度用恒温水浴控制,4条通道均以一定的流速将反应试剂经蠕动泵输入CSTR中,与反应物混合(见图1)。
经一段诱导期后,化学振荡即开始。当振荡周期和振幅稳定后,用微量进样器向CSTR中注入一定量(1-0.01ml)的过氧亚硝酸阴离子溶液,即可观察到振荡体系中振荡参数的变化。
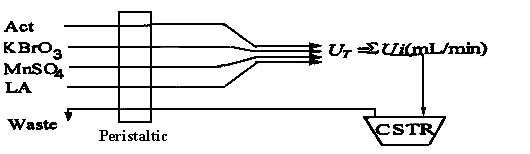
图1 本振荡体系的CSTR流程简图
1.4 具体的实验内容
1.4.1振荡参数的控制实验
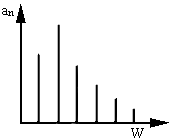
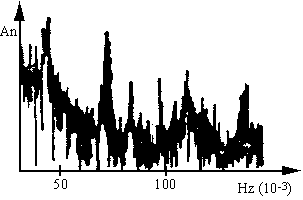
化学振荡体系属于非线性非平衡系统,有着极其复杂的动力学行为。常见的化学振荡是一种规则的周期运动现象,可由其固有频率定量表征。据傅立叶分析,任何形式的周期运动都可以看成是频率为ω 的基频振动和其一系列的泛频振动的叠加。各泛频的振幅an与频率的关系为一分离谱,见图2。但是当化学反应系统的控制参数发生变化时,一种频率的化学振荡可失去稳定性,而产生出具有新的频率的化学振荡。继续改变控制参数,就可以产生一系列更新频率的化学振荡。这种复杂的时空特性现象可以用分岔理论来解释[13]。根据分岔理论,当分岔参数uk的取值逐渐趋于某个极限值u∞时,系统就有可能达到了混沌状态,其功率谱见图3。而正是由于化学振荡体系具有这些复杂的时空行为与生命体系的周期性变化序列(如生物钟)及大脑系统存在的混沌现象有着惊人的相似性,才引起了人们的极大兴趣。实验上所观察到的周期运动,通常可以用极限环描述其在相空间的运动轨迹。我们知道,当稳定的极限环受到扰动时,它能恢复到沿极限环的运动,除非受到足够大的扰动甚至发生各种分岔时,才会跃迁到别的运动轨道,见图4。因此,我们可以利用APP技术对它进行微扰,以达到分析的目的。鉴于此,我们进行了大量的探索实验,找到了使本振荡体系出现稳定周期运动的控制参数范围,这就为我们今后的干扰实验提供了前提保障。参数控制范围见表1。
表1 本振荡体系参数控制范围
温度 |
流速 (mL/mol) |
KBrO3 |
H2SO4 |
LA |
Act |
Mn2+ |
299-307 |
0.34-1.20 |
0.02 -0.05 |
0.3 -1.0 |
0.10 -0.30 |
0.10 -0.30 |
5 ×10-4-5×10-2 |
|
|
| 图2 周期运动状态下振幅an与频率之间的分离谱 | 图3 混沌状态的功率谱 |
1.4.2 实验参数的进一步优化
在此基础上,我们对控制参数进行了进一步的优化,以达到实现最佳分析灵敏度和较快分析速度的目的。实验发现过氧亚硝酸阴离子对振荡体系的影响程度随各个参数所选数值的变化而变化。详细的变化规律见图5。
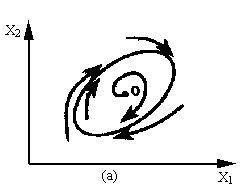
图4 周期运动的极限环描述 |
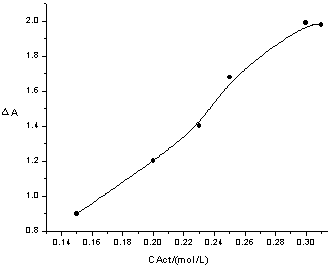 |
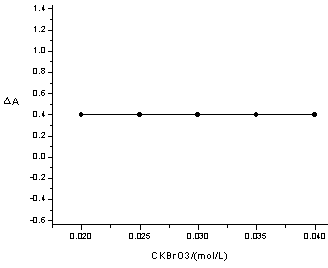
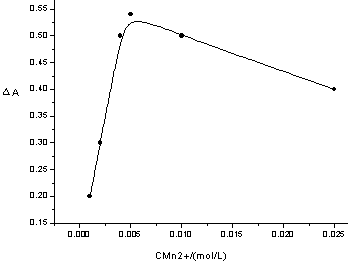
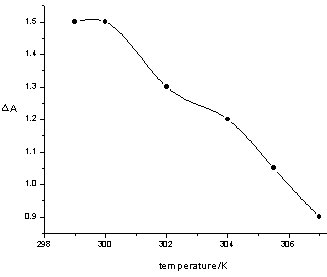
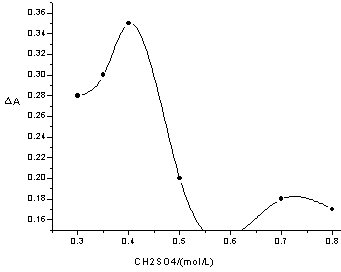
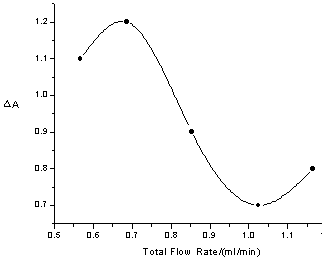
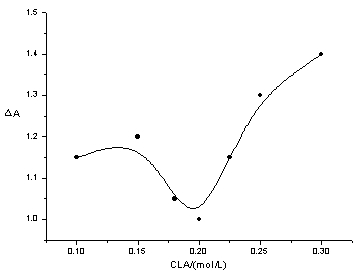
图5 实验中各控制参数的优化图
2.1基本振荡现象
在典型单周期、准双周期和它们的复合态这三种情况下我们考察了过氧亚硝酸阴离子对化学振荡器的微扰。当过氧亚硝酸阴离子微扰后,在不同的实验条件下可观察到不同的微扰现象,过氧亚硝酸阴离子的加入明显地导致振荡振幅的增加,同时伴随振荡周期的增加,微量级的过氧亚硝酸阴离子对振荡反应的影响达到了可以用宏观进行识别的水平(图6)。
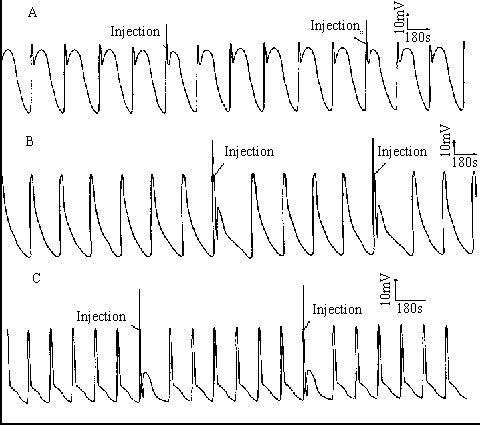
图6 基本振荡现象 (CSTR中 LA-Act-BrO3--Mn2+-H2SO4 振荡体系的典型振荡曲线,箭头指示体系受到微扰的时刻)
A: 典型的准双周期振荡曲线 B: 典型的单周期振荡曲线 C: A和B的混合模式
CH2SO4=0.40mol/L, CLA=0.15mol/L,CMn2+=4×10-3mol/L ,总流速=0.652ml/min
A:T=299K,CKBrO3=0.040mol/L,CAct=0.15mol/L
B:T=301K,CKBrO3=0.025mol./L, CAct=0.15mol/L
C:T=304K,CKBrO3=0.025mol/L,CAct=0.20mol/L 2.2 过氧亚硝酸阴离子的扰动定量关系
根据上面对实验条件的优化,结合分析对灵敏度和分析速度的要求,我们选择T=299K,CKBrO3=0.025mol/L,CH2SO4=0.40mol/L,CLA=0.15mol/L,CAct=0.20mol/L,CMn2+=4×10-3mol/L,总流速0.682mL/min为条件,可以获得较高的灵敏度和较快的分析速度。在此条件下,当振荡周期和振幅稳定后,加入一系列不同量的过氧亚硝酸阴离子(1-0.01ml,C ONOO-=4-7×10-4mol/L),发现不同的过氧亚硝酸阴离子和振幅的变化间有良好的线性关系。回归方程为y=-0.02498+2.69159x,相关系数为0.99561,线性范围为3.73×10-5-6.59×10-7mol/L,检测限达到2.25×10-9mol/L,RSD为0.10505(n=7),测定样品的速度为每小时7-8个样品。线性关系见图7。
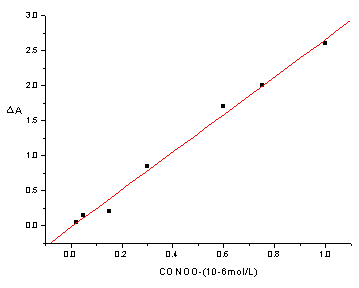
图7过氧亚硝酸阴离子浓度和振幅之间的线性关系 2.3 合成液中H2O2的干扰讨论
由于本实验中所制备的ONOO-溶液中残留有10-6mol/L的H2O2(当ONOO-的浓度为10-4mol/L)。鉴于H2O2对化学振荡体系也有干扰,我们单独研究了H2O2的干扰特征,发现H2O2对振荡体系的影响仅表现在周期的增大 [14],而合成液对振荡反应的影响不仅有周期的增大,更重要更明显的表现在振幅的增大上,当CONOO- =3.73×10-5-7.46×10-6mol/L时,振荡周期和振幅均发生明显的变化,但当CONOO- =3.73×10-6mol/L时,振荡振幅仍有明显的改变,但周期的变化已不明显,究其原因,我们认为当浓度低于10-6mol/L时,H2O2的干扰已不明显而主要表现为ONOO-的干扰。另外,我们知道过氧亚硝酸阴离子的氧化性比H2O2高出许多,对氧化还原体系应是优先反应物。但为了确保实验的准确性,我们以振幅的变化为依据来进行结果的分析。这一点也反映了本检测方法有一定的选择性。
2.4 反应机理的探讨
根据FKN机理,本振荡体系的反应机理应包括以下四个主要步骤(图8):
A ① Br-+BrO3-+2H+→ HBrO2+HOBr
② Br-+ HBrO2+H+ →2HOBr
③ 3(Br-+HOBr + H+→Br2+H2O)
BrO3-+5Br-+6H+→ 3Br2+3H2O B ①2HBrO2 →HOBr+BrO3-+H+
②2(HBrO2+BrO3-+H+ →2BrO2.+H2O)
③4(BrO2.+Mn2++H+ → Mn3++HBrO2)
BrO3-+4Mn2++5H+ → 4Mn3++HOBr+2H2O
C Mn3++CH3CHOHCOOH → Mn2++oxidative product
D Br2+CH3COCH3 → BrCH2COCH3+Br-+H+
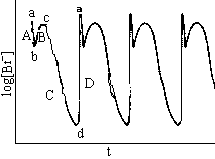
图8 振荡体系的机理描述
在转折点a.b.c.和d处,反应过程中的主要反应步骤发生了切换[13]。由于我们是选择在D向A的切换点处进样,ONOO-作为一种强氧化剂,可以和HBrO2共同竞争Br-,从而使过程D继续占优势反应的地位,导致振幅的增加,即过程D向过程A的切换时间延长。
REFERENCES
[1] Pryor W A et al. J.Am Physiol, 1995, 268 (5): 699-722.
[2] Ischiropoulos H. Biophys, 1998, 356: 1-11.
[3] Field R J, Burger M. Oscillations and Travelling Waves in Chemical Systems. New York: Wiley, 1985.
[4] Gray P, Scott S K. Chemical Oscillation and Instabilities Non Linear Chemical Kinetics. Oxford: Clarendon Press, 1990.
[5] Nicolis G, Prigogine I. Self-organization in Nonequilibrium Systems, New Work: Wiley, 1977.
[6] Field R J, Koros E, Noyes R M. J.Am.Chem.Soc., 1972, 94: 8649.
[7] Gan N Q, An C J, Liu Y, Cai R X. Analyst, 1998, 123: 2395.
[8] Echols R T, Carroll M K, Tyson J F. Anal. Proc., 1995, 32: 3.
[9] Jimenez-Prieto R, Silva M, Perez-Bendito D. Anal. Chem., 1995, 67: 729.
[11] Echols R T, Carroll M K, Tyson J F. Anal. Proc., 1995, 32: 3.
[10] Jimenez-Prieto R , Silva M, Perez-Bendito D. Analyst, 1998, 123: 1R.
[11] Dr Henry, Papee M, Dr Gianna et al. Nature, 1964, 204: 142.
[12] Xi H W, Nonlinear Science (Fei Xianxing Kexue), The Publish of Chinese technology (Zhongguo Kexue Jishu Chubanshe), 1999.
[13] Zhang K, Cai R X, Ma W H et al. Chemical Journal of Chinese Universities (Gaodeng Xuexiao Huaxue Xue bao), 2000, 3: 377.