http://www.chemistrymag.org/cji/2003/059069nc.htm |
Aug. 1, 2003 Vol.5 No.9 P.69 Copyright |
(College of Chemistry and Chemical Engineering; #College of Environment Science and Engineering, DongHua University, Shanghai, 250001)
Abstract The determination of protein using tetrabromofluorescein as spectrographic probe was studied in this paper. The analytical system is very simplicity, Beer's law is obeyed at the range of 0.11-60.0mg/ml protein. The relative standard deviation was 1.26%(15.0
mg/ml BSA , n=10). Sandell's sensitivity is 0.094mg/cm2。 Furthermore, the method has been applied to the determination of protein in serum sample with satisfactory results. The recovery of the method is 96.75-104.5%.Keywords Protein,Tetrabromofluorescein,Molecular absorption spectrometry, spectrographic probe
用四溴荧光素作光谱探针测定血清蛋白的研究
王琼娥 庄惠生#(东华大学化学化工学院; #东华大学环境科学与工程学院,上海200051)
2003年3月14日收到; 国家自然科学基金资助项目(20277005),福建省自然科学基金资助项目(C0110005)和东华大学科技发展基金资助项目
摘要 本文研究了四溴荧光素作为光谱探针用于测定牛血清白蛋白和人血清蛋白的分析方法。BSA浓度在0.11~60.0mg.ml-1范围符合比尔定律;精密度高,测定浓度为15.0mg.ml-1 BSA溶液10次,求得相对标准偏差为1.26%。灵敏度较高,桑德尔灵敏度为0.094mg.cm-2。可直接用于血清样品中蛋白质的测定,测得质量控制血清样品中蛋白质含量为11.8± 0.80 g/L,与标准值12.3 g/L吻合;回收率在96.5%~104.5%之间,结果满意。关键词 蛋白质, 四溴荧光素, 分子吸收光谱
蛋白质与某些生色剂(如溴甲酚绿[1]、溴酚蓝[2]、铬天青S[3,4])可以在酸性条件下发生作用导致颜色变化,以此类阴离子染料作为传感媒介的分析方法已广泛应用于生物样品和临床分析中的蛋白质测量,但未见文献报道过利用阳离子染料作光谱探针测定蛋白质的研究。
四溴荧光素(水溶性)是一种阳离子染料,又名四溴萤光素,可作生物染色剂、吸附指示剂和色谱分析试剂。本文研究了四溴荧光素作为光谱探针与牛血清白蛋白和人血清蛋白质相互作用的性质。在pH=2.2的柠檬酸-磷酸氢二钠的缓冲溶液中,四溴荧光素的最大吸收波长为514nm,当它与牛血清白蛋白结合时,结合物的最大吸收波长为530nm,对比度为
1 试验部分
1.1 仪器与试剂
721分光光度计(上海第三分析仪器厂);牛血清白蛋白(简称BSA)标准溶液:准确称取0.1250g牛血清白蛋白(中国科学院上海生物化学研究所),用0.9%NaCl(0.9gNaCl 溶于100ml水中)溶液配制至250ml,即配成500 mg.cm-1 BSA溶液,置于5℃左右冰箱中保存。使用时稀释至所需的浓度。质量控制血清(临床实验室用,卫生部上海生物制品研究所和卫生部临床诊断试剂中心)冻干。置于5℃左右冰箱中保存。四溴荧光素溶液:准确称取0.2500g四溴荧光素,溶于少量水中,移入500ml容量瓶中,用水定容,摇匀,即配成500mg.cm-1 四溴荧光素溶液,使用时,用水逐级稀释至所需浓度。掩蔽剂EDTA溶液:称取5.010g EDTA溶于水中,移入500ml容量瓶中,用水定容,即配成mg.cm-1 EDTA溶液,可根据需要,稀至其它低浓度。缓冲溶液:准确称取21.014g柠檬酸溶于水中,移入1L容量瓶中,加水至刻度,摇匀,浓度为0.1mol.L-1。准确称取磷酸氢二钠3.5181g溶于水,移入500ml容量瓶,加水至刻度,摇匀,即配成0.2 mol.L-1磷酸氢二钠溶液,使用时按所需不同pH值,移取不同量的柠檬酸溶液,磷酸氢二钠溶液,混合均匀,得到不同pH的缓冲溶液。试验所用试剂均为分析纯,试验用水均为二次蒸馏水。
1.2 试验方法
在25 ml容量瓶中,依次加入500mg.ml-1四溴荧光素溶液1.0ml, 100mg.ml-1 BSA 溶液2.5 ml,用pH=2.2柠檬酸一磷酸氢二钠缓冲溶液定容至25 ml。以试剂空白(在25 ml容量瓶中,依次加入500mg.ml-1四溴荧光素溶液1.0ml, 0.9%NaCl溶液2.5ml,用pH=2.2柠檬酸一磷酸氢二钠缓冲溶液定容至25 ml)为参比(测定四溴荧光素溶液的吸收光谱时用水为参比),用721型分光光度计,仪器灵敏度为2档,比色皿厚度为1cm,测其吸光度。
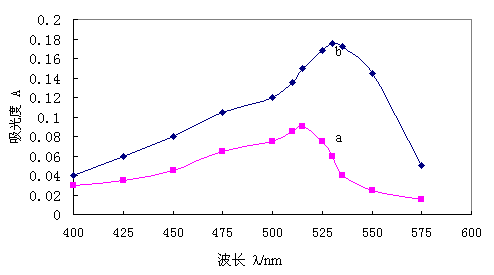
图1 吸收光谱
a pH=2.2, 5mg.ml-1 四溴荧光素; b pH=2.2, 5mg.ml-1四溴荧光素+10mg.ml-1 BSA 2 结果与讨论
2.1 吸收光谱
在pH 2.2的柠檬酸一磷酸氢二钠缓冲溶液中,测定四溴荧光素和四溴荧光素-BSA的吸收光谱见图1。由图1可知四溴荧光素的吸收峰lmax为514nm,四溴荧光素与BSA结合后,最大吸收峰lmax为530nm,可见四溴荧光素与蛋白质有相互作用,结合物吸收光谱产生红移,对比度为Dl=16nm。在波长534nm处四溴荧光素-BSA与四溴荧光素的吸光度差值DA最大,为了降低背景影响,提高测定的灵敏度,本文最佳测定波长选择为534nm。
2.2 介质与酸度
本文选择柠檬酸一磷酸氢二钠缓冲溶液为反应介质。在柠檬酸一磷酸氢二钠缓冲溶液中,随着pH增大,吸光度显著增大,当pH为2.0~2.4间,吸光度达峰值且变化较小,pH再增大,吸光度呈下降趋势,因而选择柠檬酸一磷酸氢二钠缓冲溶液的pH为2.2。
2.3 显色剂用量
随着四溴荧光素加入量的增加,吸光度显著增大,当四溴荧光素用量为0.8~1.4ml,吸光度达到峰值且变化较小,故选择显色剂四溴荧光素用量为1.0ml。
2.4 稳定性试验
试验结果表明,在柠檬酸一磷酸氢二钠缓冲溶液介质中,BSA与四溴荧光素迅速反应形成结合物,吸收光谱产生红移,结合物稳定性较好,在6小时之内,结合物的吸光度基本不变,超过6小时后,吸光度呈缓慢下降趋势,因而在实验中,溶液配好后至6小时之内测定,对测定结果基本无影响。
2.5 干扰与掩蔽试验
在有掩蔽剂EDTA存在条件下,测定浓度为10mg.ml-1 BSA溶液,相对误差小于10 % 时,以下共存离子无干扰:200倍的Ca2+、NH4+,150倍Ba2+、K+,100倍的Ni2+,70倍的乳酸、SO42-,50倍的L-苯丙酸、Mg2+,40倍的NO2-、Pb2+,30倍的Zn2+、Mn2+、Co2+、氨基乙酸,20倍的抗坏血酸、核黄素、草酸、Cr3+,10倍的Fe3+。
2.6 工作曲线
BSA浓度从0.11~60mg.ml-1符合比耳定律,标准曲线见图2。
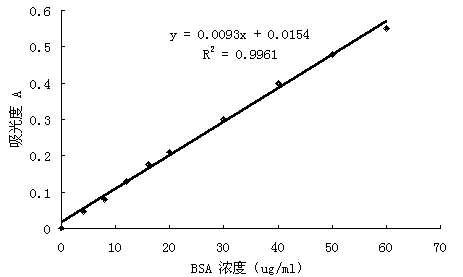
图2 工作曲线
2.7 精密度、桑德尔灵敏度和检测限
2.8 分析应用
2.8.1 质量控制血清中蛋白质含量的测定
用所拟定的实验方法测定质量控制血清中蛋白质含量。该血清中各组分的含量如下:K+,0.90 mol.L-1; Na+,26.9 mol.L-1; Cl-,18.5 mol.L-1; P,8.1mg.L-1; Ca2+,23.4 mg.L-1; 尿酸,14 mg.L-1;葡萄糖,1.19 g.L-1;肌酐,14.7 mg.L-1;总蛋白,12.3 g.L-1。按照说明书,每瓶(蛋白质质量为36.9 mg)加入3.00ml水,使其溶解。移取1.00ml,用水稀释至100ml,用作工作液。用标准加入法测定,取7支比色管,依次编号为1、2a、2b、2c、3、4、5(1号管为空白,2a、2b和2c为平行样)。首先于各管中加一定体积一定浓度的四溴荧光素溶液,然后向2a、2b、2c、3、4、5各管中加入2.0 ml 质控血清工作液,再于3、4、5各管中加入BSA标准溶液(100mg.ml-1 BSA)2.0、4.0和6.0ml,用pH=2.2的柠檬酸一磷酸氢二钠缓冲溶液定容至25ml,以1号管溶液为参比在534nm处测定吸光度值,以吸光度值对BSA标准溶液浓度作图,得一直线,延长此直线与横轴相交,交点的绝对值即为所求蛋白质含量。测得上述质量控制血清样品中蛋白质含量为11.8± 0.80 g/L。与标准值12.3 g/L吻合。
2.8.2 回收试验
取上述质量控制血清工作溶液2.0 ml(蛋白质质量为0.246 mg),加入不同量的BSA,按实验方法测定,测定结果见表1,由表1可知,回收率在96.75~104.5%。
表1 回收率测定结果
| 牛血清白蛋白 | 回收率(%) | |
| 加入量 | 测得量 | |
| 0 0.1330 0.1990 0.2660 |
0.2460 0.3901 0.4502 0.5041 |
|
REFERENCES
[1] Wei Y J, Li K A, Tong S Y. Analytical Chemistry (Fenxi Huaxue), 1996, 24 (4): 387.
[2] Sun H M. Chinese Journal of Clinical Laboratory Science (Linchuang Jianyan Zazhi), 1994, 12 (1): 16.
[3] Wei Y J, Li K A, Tong S Y. Acta Chimica Sinica (Huaxue Xuebao), 1995, 53: 83
[4] Zhuang H S, Duan J P, Wang Q E et al. Chemistry (Huaxue Tongbao), 1999,Supp: 289.