http://www.chemistrymag.org/cji/2005/076041rc.htm |
Jun. 1, 2005 Vol.7 No.6 P.41 Copyright |
Qin Ming, Feng XizengЈ¬Wang
LikaiЈ¬Jia Yunfang
(College of Life Science, Nankai University, Tianjin 300071, China)
Abstracts: Recently, as a new tool, microfludic devices have been widely used in
tissue engineering. This review focuses on new developments of microfluidic technology in
tissue engineering, pointing out the advantages and prospects of these concepts for future
application. Firstly, microfludic technology is a new method of cell patterning and
cultivation, including microfluidic patterning, topographical control over cell, and
bioreactors. Secondly, it was shown that microfluidic technology has been applied in many
branches of tissue engineering, such as basal lamina, vascular tissue, liver, bone,
cartilage, neurons and local delivery. Hence, it is necessary to review the development of
microfluidic technology in tissue engineering.
Keyword microfluidics device, tissue engineering, patterning cell, Topographical
control.
ОўБчМејјКхФЪЧйЦҜ№ӨіМЦРөДУҰУГ
ЗШГчЈ¬·лПІФцЈ¬НхБўҝӯ, јЦЬҝ·јЈЁДПҝӘҙуС§ЙъГьҝЖѧѧФә МмҪт300071Ј©
ХӘТӘ
ҪьДкАҙЈ¬ОўБчМејјКхЧчОӘТ»ЦЦРВөДјјКхКЦ¶ОФЪЧйЦҜ№ӨіМБмУтөГөҪБЛРн¶аУҰУГЎЈұҫОДЧЫКцҪьДкАҙОўБчМејјКхФЪЧйЦҜ№ӨіМЦРөДУҰУГЗйҝцЈ¬КЧПИЈ¬ОўБчМејјКхКЗТ»ЦЦРВөДПё°ы№М¶ЁәНЕаСшјјКхЈ¬°ьАЁОўБчМе№М¶ЁПё°ыЎўҝЙҝШЦЖНШЖЛҪб№№өДПё°ыәНЙъОп·ҙУҰЖчөИ·Ҫ·ЁЈ»ЖдҙОЈ¬ЧчОӘТ»ЦЦРВөДПё°ы№М¶ЁәНЕаСшјјКхЈ¬ОўБчМејјКхТСФЪЧйЦҜ№ӨіМөДРн¶а·ЦБмУтөГөҪУҰУГЈ¬АэИз»щ°еЎўСӘ№ЬЧйЦҜЎўёОЎў№ЗЎўИн№ЗЎўЙсҫӯПё°ыәН¶ЁО»ҙ«өЭөИЈ¬Іў¶ФЖдСРҫҝУҰУГөДЗ°ҫ°ҪшРРХ№НыЎЈ№ШјьҙК ОўБчМеЖчјю, ЧйЦҜ№ӨіМ, Пё°ы№М¶Ё,ҝЙҝШНШЖЛҪб№№ЎЈ 2005Дк5ФВ12ИХКХёе; МмҪтКРҝЖјј·ўХ№јЖ»®УҰУГ»щҙЎСРҫҝЦШөгПоДҝЧКЦъҝОМвЈ¬ҪМУэІҝБфС§»Ш№ъИЛФұҝЖСРЖф¶Ҝҫӯ·СЧКЦъПоДҝЎЈ 1. ТэСФ
ЧйЦҜ№ӨіМЈЁTissue Engineering, TEЈ©КЗЧЫәПУҰУГ№ӨіМС§УлЙъГьҝЖС§өД»щұҫФӯАнЎў»щұҫАнВЫәН»щұҫјјКхПаҪбәПЈ¬СРҫҝІў·ўПЦҝЙУГУЪЧйЦҜ»тЖч№Щ№ҰДЬРЮёҙУлЦШҪЁөДЙъОпМжҙъЖ·өД»щҙЎУҰУГС§ҝЖ[1]ЎЈHubell J[2] ёЕАЁБЛЙъОп»оРФІДБПЦЖұёјјКхј°ПаУҰөДұнХч·Ҫ·ЁЎЈЛжЧЕЖдЛыС§ҝЖөД·ўХ№Ј¬ЧйЦҜ№ӨіМБмУтФЪ»щУЪОўГЧ/ДЙГЧ№№ФмөДРВјјКхәН·Ҫ·ЁөИ·ҪГжТІөГөҪБЛ·ўХ№Ј¬ИзТФ№ЗН·әНИн№ЗЧйЦҜОӘ»щҙЎөДРДФајЎИвәНЖдЛыёҙФУҪб№№өИөДјјКхәН·Ҫ·Ё[3]ЎЈ
ФЪ¶юК®КАјНҫЕК®ДкҙъЈ¬ManzәНWidmer[4]КЧПИМбіцБЛОўБчҝШРҫЖ¬ЈЁmTASЈ©өДёЕДоЈ¬ЛьКЗТ»ЦЦёЯ¶ИјҜіЙ»ҜәНОўРН»ҜөД·ЦОцјјКх·Ҫ·ЁЈ¬ДҝЗ°ТІұ»іЖОӘРҫЖ¬КөСйКТЈЁlab on a chipЈ©[5]ЎЈУлҙ«Ні·ЦОцјјКх·Ҫ·ЁПаұИЈ¬ЖдҫЯУРҝмЛЩЎўҪЪКЎЎў·ҪұгөИМШөгЈ¬ТСұ»№г·әУҰУГУЪЙъОпЎў»ҜС§өИёчёцБмУтЎЈ¶шОўБчМејјКхФЪЧйЦҜ№ӨіМБмУтТІҪ«·ў»УИХТжЦШТӘөДЧчУГЈ¬ТтҙЛЈ¬ұҫОДёЕКцОўБчМејјКхФЪЧйЦҜ№ӨіМЦРөД»щҙЎУлУҰУГөДСРҫҝҪшХ№ЎЈ 2 ОўЗшУтҝЙҝШөДПё°ы№М¶ЁәНЙъіӨјјКх
2.1 Пё°ыөДҝЙҝШРФ№М¶ЁјјКх
УҰУГОўБчМејјКхҝЙФЪ»щөЧұнГжКөПЦІ»Н¬өДПё°ыНј°ёЈ¬ХвЦЦПё°ы№М¶ЁјјКхФЪЧйЦҜ№ӨіМәН»щҙЎПё°ыЙъОпС§СРҫҝБмУтК®·ЦЦШТӘЎЈОўБчМеЖчјюУЙҫЯУРТ»¶ЁҝЧөАҪб№№өДPDMSәН»щөЧОпЦК№№іЙЈ¬НЁ№эОўБчұГ»төзУҫҪ«БчМеҙ«өЭЦБөЧОпЙПөДДіТ»ПЮ¶ЁЗшУтЈ¬ҪшТ»ІҪҪ«Пё°ыХіБ¬»тРьёЎФЪөЧОпөДМШ¶ЁЗшУтЙП[6]ЎЈөұБҪМх»т¶аМхІгБчТәМеҪбәПҪшИлТ»МхҝЧөАКұЈ¬»мәПБчТАИ»»ҘПаЖҪРРБч¶ҜЈ¬ҪцФЪБчМеДЪұнГж·ўЙъұнГжА©ЙўЈ¬АыУГФЪОўҝЧөАЦРІъЙъәНО¬іЦІ»Н¬ИЬТәЖҪРРБч¶ҜөДДЬБҰЈ¬ҝЙ№М¶ЁПё°ыәНДЈДвПё°ыЦЬО§Оў»·ҫі[7]ЎЈTakayama SөИИЛ[8] НЁ№эҪ«БЪҪьТ»ёцПё°ыөДБҪёцБчМеөДДЪұнГж№М¶ЁЈ¬УГУЪСРҫҝСЗПё°ыҙҰАнЈЁИзНј1ЛщКҫЈ©Ј¬¶шҪ«БҪЦЦІ»Н¬өДИҫБП»тТ©ОпУҰУГУЪПаН¬Пё°ыөДІ»Н¬ЗшУтЈ»¶ФУЪІ»ТЧёҪЧЕФЪ№ММеөЧОпұнГжөДПё°ыЈ¬ҝЙУГУЪФЪҝЙҝШМхјюПВРОіЙЧФУЙРьёЎөДЎўҫ«ПёОИ¶ЁөДИэО¬Ҫб№№СӘ№ЬНј°ёЎЈ
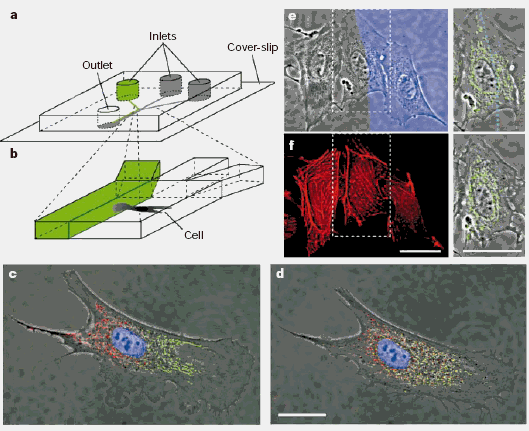
Нј1 УҰУГ¶аЦШІгБчөДөҘТ»ЕЈСӘЗеГ«Пё№ЬДЪЖӨПё°ыІ»Н¬ЗшУт·Ц»ҜНј[8]ЎЈЈЁa, bЈ©КөСйЧ°ЦГ№№іЙНјЈ»ЈЁbЈ© ИлҝЪҝЧөАУлЦчҝЧөАҪбәПҙҰҫЦІҝНјЎЈЈЁcЈ© Т»ІаУГMitotracker Green FMЈ¬БнТ»ІаУГMitotracker Red CM-H2XrosҙҰАнәуөДөҘПё°ыУ«№вНјЖ¬ЈЁХыёцПё°ыУГDNAБ¬ҪУИҫБПHoechst 33342ҙҰАнЈ©ЈЁdЈ©УлcЦРПаН¬өДПё°ыҙҰАн2.5РЎКұЈ¬ПЯБЈМеәмВМБҪІҝ·ЦДЪ»мәПЎЈЈЁeЈ©УГlatrunculin AҙҰАнөДІҝ·ЦөҘПё°ыЎЈА¶Й«ЗшУтұнГчә¬УРlatrunculin AөДЕаСшТәБч¶ҜЎЈУТұЯЈ¬ЦРјдПё°ыәНЛьөДПЯБЈМе·ЕҙуНјЈЁВМЙ«Ј©ЎЈЈЁfЈ©ПаН¬өДПё°ыУГlatrunculin A ҙҰАн10minәуБўјҙУГPhalloidinЁCAlexaұкјЗЎЈЦРјдөДПё°ыЈ¬ҪцІҝ·ЦО»УЪә¬УРlatrunculin AөДБчМеЦРЈ¬ұнГчПЮЦЖУлҙЛЗшУтөДјЎ¶Ҝө°°ЧОўЛҝЦР¶ПЎЈlatrunculin AЈәәмәЈГЮөДёЯ¶ҫҙу»·ДЪхҘЎЈ
Fig.1 Differential manipulation of regions of a single bovine capillary endothelial cell using multiple laminar flows. (a, b) Experimental set-up; (b) shows a close-up of the point at which the inlet channels combine into one main channel. (C) Fluorescence images of a single cell after treatment of its right pole with Mitotracker Green FM and its left pole with Mitotracker Red CM-H2XRos. The entire cell is treated with the DNA-binding dye Hoechst 33342. (d) Image of the same cell as in c but taken 2.5 h later, showing intermixing of the red and green subpopulations of mitochondria. (e) Treatment of a portion of a single cell with latrunculin A. The blue region (Dextran-70,000 Cascade Blue stain) reveals the flow of medium containing latrunculin A. Right, enlarged view of the middle cell and its mitochondria (green). (f) PhalloidinЁCAlexa 594-labelled image of the same cell immediately after 10 min of treatment with latrunculin A. The cell in the middle, which was only partly in the stream containing latrunculin, shows disruption of actin microfilaments that is limited to this region (scale bars, 25 mm). Further details are available from the authors. Feng X ZөИИЛ[9]УҰУГОўБчМејјКхПИҪ«Т»ҝ№№М¶ЁУЪҫӯ»ҜС§РЮКОөД»оРФ»щөЧІДБПұнГжЈ¬ҪшТ»ІҪҪ«У«№вұкјЗөД¶юҝ№УлИЛЦұіҰ°©Пё°ыЈЁCaCOЈӯ2Ј©БӘҪУЈ¬НЁ№эҝ№МејдөДҪбәПЧчУГҪ«Пё°ы№М¶ЁУЪОўҝЧөАөДТә-№МұнГжЙПЈ¬Ҫш¶шҝЙУҰУГУЪБЩҙІЦЧБцөДХп¶П·ЦОцСРҫҝЎЈChiu D T өИИЛ[10]НЁ№эКэІгұнГжРФЦКІ»Н¬өДОўБчМеІгЈ¬ҝЙРОіЙУЙІ»Н¬ЦЦАаПё°ыЧйіЙөДИэО¬Пё°ыЙъіӨөДНј°ёЈ¬ХвЦЦИэО¬Нј°ёјјКхҝЙУГФЪДЪЖӨПё°ыБЩҪьЗшУт№М¶ЁЦЧБцПё°ыЈ¬ІўҝЙДЈ·ВЦЧБцСӘ№ЬЧйіЙөДҝХјдЦШЕЕЎЈ
2.2Пё°ыөДНШЖЛҪб№№өДҝШЦЖРФЙъіӨ
ЧйЦҜ№ӨіМСРҫҝөДәЛРДЦ®Т»КЗИзәОСЎФсәПККөД·Ҫ·ЁЈ¬№№ҪЁМШ¶ЁҪб№№өДЙъОпІДБПЦ§јЬЈ¬ЗТК№Т»¶ЁКэБҝөДПё°ыФЪЦ§јЬЦР·ўУэЙъіӨЎЈН¬КұЈ¬ИЛ№ӨЦЖФмөДЧйЦҜҪб№№УҰҫЯУРБјәГөДҝЙҝШЦЖөДОўҪб№№Ј¬ІўФЪТ»¶ЁөДКұјдДЪДЬ№»О¬іЦПё°ыөДЙъіӨРОМ¬Ўў·Ц»ҜәН№ҰДЬ[11]ЎЈИЛ№ӨЧйЦҜҪб№№өДТ»ёцЦШТӘМШХчКЗҝЙёҙЦЖМеДЪҝХјдҪб№№УлұИАэЈ¬ТФұг°пЦъО¬іЦПё°ыМеДЪөДФӯКјПФРОЎЈУҰУГОўБчМејјКхЈ¬УРҝЙДЬҪ«ОўҪб№№ЦІИлМеДЪЈ¬ҝЙТФУҰУГУЪГвТЯ·ЦАлЎўПё°ыДЪПтЙъіӨәНТ©Опҙ«өЭөИСРҫҝ[12]ЎЈSinghvi R өИИЛ[13]ЧЫКцБЛРн¶аҝЙҝШЦЖПё°ыәНЧйЦҜНШЖЛҪб№№өДСРҫҝіЙ№ыЎЈDeutsch өИИЛ[14]ұЁөАБЛЕаСшөЧОпұнГжөДИэО¬ҝХјдҪб№№ҝЙ¶ФМеНвРДјЎ¶ЁО»ІъЙъәЬҙуөДУ°ПмЈЁјыНј2Ј©ЎЈ
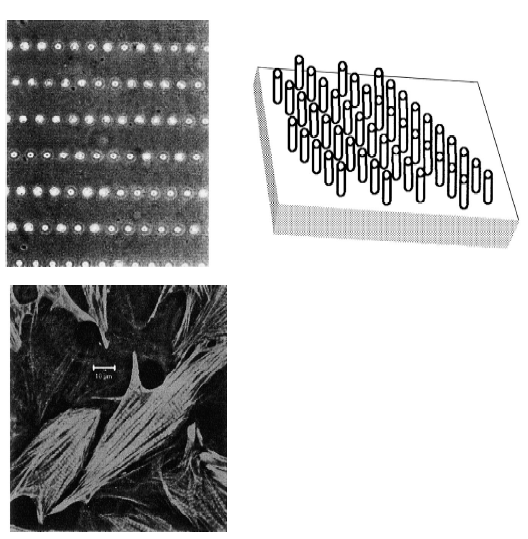
Нј2 ҝЙУГАҙЦЖФмОўҪб№№өДОў¶ӨЈ¬ОўҪб№№ҝЙУ°ПмПё°ыёҪКфәНРОМ¬[15]
Fig.2 Micropegs can be used create microarchitectures which direct cell attachment and morphology
Den BraberE өИИЛ[15]ұЁөАБЛОўЧйЦҜөДИэО¬Ҫб№№¶ФПё°ыХіәПУРәЬҙуөДУ°ПмЎЈVan
Kooten өИИЛ[16]ұЁөАDNAВЦАӘКЬОўЧйЦҜҪб№№өДУ°ПмЈ»ЖдЛьИзПё°ыФЪҝЙҝШЦЖөД¶юО¬»тИэО¬РтБРЦРЦШЕЕ¶ФПё°ы·Ц»ҜЎўО¬іЦәН№ҰДЬіЦҫГРФУРБјәГөДР§№ыЈ»¶шНШЖЛҪб№№ДЬУ°ПмәНТэөјПё°ыөДТЖЦІЙъіӨ·ҪПт[17]ЎЈ
2.3 ЙъОп·ҙУҰЖч
ЕаСшёЯГЬ¶ИөДПё°ыКЗЧйЦҜ№ӨіМОӘҙпөҪЙъАн№ҰДЬөДБнТ»ёцЦШТӘИООсЈ¬ОӘҙЛұШРлИ·ұЈНЁ№эЕаСш»щМṩОИ¶ЁөДУӘСшОпЦКәНСхЖшЈ¬Іўј°КұЕЕіцҙъР»ОпЎЈөЪТ»ҙъУҰУГУЪПё°ыЕаСшөДЙъОп·ҙУҰЖчөДЙијЖәЬјтөҘЈ¬ҪцДЬПтҫЫјҜЧйЦҜұГҪшУӘСшТәЈ»¶шУҰУГУЪЕаСшСӘ№ЬәНИн№ЗЧйЦҜөДөЪ¶юҙъЙъОп·ҙУҰЖчҝЙІъЙъВц¶ҜБчЈ¬К№ЧйЦҜКЬөҪС№ЛхЎўјфЗРБҰәНЕаСш»щөДУ°ПмЎЈХвЦЦУ°ПмҙуҙуёДҪшБЛИЛ№ӨСӘ№ЬЎўИн№ЗЧйЦҜәНРДјЎөД»ъРөРФЦК[18]ЎЈФЪҙ«НіөДПё°ыЕаСшМеПөЦРәЬДСКөПЦід·ЦөДСӯ»·[19]Ј¬¶шОўБчМеҪб№№ҝЙИЭТЧөШМṩ΢іЯ¶ИөДҝЙҝШБчМеСӯ»·Ј¬ДҝЗ°ТСҫӯіцПЦТ»Р©УҰУГУЪПё°ыЕаСшөД¶юО¬ОўБчМеЖчјю[20]ЎЈө«¶аІгОўБчМеҪб№№ИФІ»¶ајы[21]ЎЈLeclerc
EөИИЛ[21a]ұЁөАБЛТ»ЦЦТФҫЫ¶юјЧ»щ№иСхНйЈЁPDMSЈ©ОӘ»щөЧөД¶аІгОўБчМеЖчјюЈ¬ҝЙУГУЪІёИй¶ҜОпПё°ыөД№аЧў·ЁЕаСшЈ¬УГУЪёЯГЬ¶ИЕаСшПё°ыөДУРСхөД¶аІгЖчјюЎЈVozzi
өИИЛ[21b]УҰУГЙъОпҝЙҪөҪвөДҫЫИйЛб-ТТҪ»хҘЈЁpoly(DL-lactide-co-glycolide),PGLAЈ©ІДБПЦЖФміцТ»ЦЦИэО¬¶аІгөДЧФЧйЧ°Ц§јЬУГУЪЙъОпЧйЦҜ№ӨіМСРҫҝЦРЎЈGu
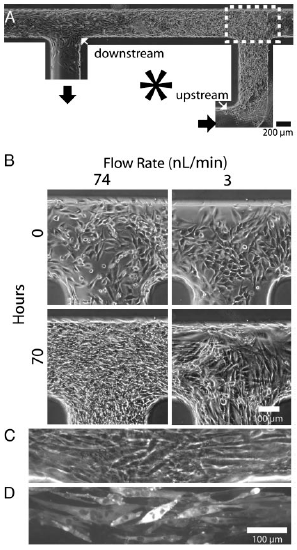
WөИИЛ[22]УҰУГ¶аёцҝЙҝШЦЖТЖ¶ҜөДС№өзТэПЯҫ«И·ҝШЦЖөҜРФМеГ«Пё№ЬНшВзДЪІҝТәМеөДБч¶Ҝ·Ҫ·ЁЈ¬УҰУГёГ·Ҫ·ЁҝЙФЪОўБчМеРҫЖ¬ЙП»®·ЦәНО¬іЦC2C12КуіЙјЎПё°ыөДФцЦіУл·Ц»ҜЈЁИзНј3ЛщКҫЈ©ЎЈ
Нј3
Fig.3 On-chip cell culture. (A) A typical cell culture loop at a flow rate of 15nl/min. (B) C2C12 cells cultured in channels circulated with cell culture media at different flow rates. (C) Phase-contrast images of muscle differentiated and undifferentiated cells aligned in the movement of flow. (D) Fluorescent micrograph of the same differentiated cells stained for the myosin heavy chain. Positive staining and multinucleated cells indicated differentiation.
3 Пё°ы№М¶ЁәНЕаСшјјКхөДУҰУГ
»щ°еФЪёчЦЦЧйЦҜЦРҫщ°зСЭЧЕЦШТӘҪЗЙ«Ј¬ФЪЙцРЎЗтЦР»щ°еҙУЧгПё°ыЦР·ЦАлДЪЖӨПё°ыЈ¬ІўЗТКЗТ»ёцБ¬ҪУСӘҪ¬Пё°ыөД°лНёДӨЈ»ФЪЖӨ·фұнГж»щ°еКЗҙУЖӨПВҪбөЮМеЛШ·ЦАлПё°ыөДТ»ёцХП°ӯОпЎЈЛдИ»№М¶Ё¶аҝЧөДәЈГаЎўЕЭДӯәНДЈҫЯҝЙУГУЪ№№Фм°ыНвИэО¬ҫШХуөДАаЛЖОпЈ¬ө«ҪцПЮУГУЪЦЖФм»щ°еЎЈТ»ЦЦОў№№Фм·Ҫ·ЁҝЙУГУЪЦЖФмҫЯУРёҙФУНШЖЛҪб№№МШХчөД»щ°еАаЛЖОп[23]Ј¬ХвЦЦұіј№әНҝЧөАөДКФСйСщЖ·УлМмИ»»щ°еЦР·ўПЦөДіҰМЧөюәЬАаЛЖЈ¬ҝЙТФНЁ№эјӨ№вҝМКҙҫЫхЈСЗ°·СЪДӨРҫЖ¬¶шөГөҪЈ»ёәРФёҙЦЖРҫЖ¬УГPDMSЦЖіЙЈ¬ХвР©ёҙЦЖЖ·УГАҙЧчОӘҪәФӯ»тДэҪәөДұЎДӨІъЖ·ЈЁ21mmЈ©өДДЈ°еЈ¬¶шХвР©Ҫб№№¶АМШөД»щ°еАаЛЖОпәЬҝЙДЬУРЦъУЪҪвКННШЖЛҪб№№¶ФЙПЖӨПё°ыФцЦіУл·Ц»ҜөДУ°ПмЎЈ
3.2 СӘ№ЬЧйЦҜ
ИЛ№ӨЧйЦҜФЪМеНвГ»УРСӘТәО¬іЦПөНіЈ¬¶шПЮЦЖИЛ№ӨЧйЦҜіЯҙзҙуРЎөДТ»ёцЦчТӘОКМвКЗСхЖшФЪәЬ¶МҫаАлДЪҫНТСҫӯәДЙўЈ¬ІўГ»УРұ»ЧйЦҜАыУГЎЈТЖЦІМеДЪәуЈ¬ИЛ№ӨЧйЦҜөДПё°ы»бФЪјёРЎКұДЪәДҫЎУРПЮөДСхЖшЈ¬ө«КЗҙ«өЭСхЖшәНУӘСшОпЦКөДРВЙъСӘ№ЬФтРиТӘКэМмөДЙъіӨКұјдЎЈЧоҪьТСЦЖФміцТ»ЦЦРВөДОўБчМеНшВзЈ¬ЖдҝЙУГУЪРОіЙёЯ¶ИНіТ»өДҝЙДЈ·ВҙуіЯ¶ИЙъАнРФЦКЈЁАэИзЧЬБчЛЩЈ©өДБч¶ҜДЈКҪЈ¬ЖдДЈ·ВР§№ыУлДЈ·ВРЎіЯ¶ИПЦПуАаЛЖЈ¬АэИзГ«Пё№ЬТәМеЛЩВКЎЈҪьЛЖУЪДҝұкЖч№ЩСӘТәБч¶ҜРРОӘөДТәМе¶ҜБҰС§ДЈРНҝЙЧчОӘ№вҝМСЪДӨөД»щҙЎЈ»ХвР©СЪДӨҝЙТФУГАҙДЈ·ВСӘ№ЬНшВзЎЈҫЫәПОпұЎДӨФЪЦэДЈАпҪҪЦэЈ¬Іўұ»јҜіЙУГУЪРОіЙәсөДИэО¬Ц§јЬЈ¬Ц§јЬҝЙУГУЪПё°ыЕаСшА©ФцЎЈДҝЗ°К№УГТФҫЫТТП©әНҫЫТТҙјЛбөД№ІҫЫОпОӘ»щІДөД·ЗҪөҪвРФЙъОпПаИЭРФДЈ°е»тХЯҝЙҪөҪвЙъОпДЈ°еЈ¬ҪшРРПё°ыЕаСшКөСйСРҫҝЈ¬Ҫб№ыұнГчЙПЖӨПё°ыФЪОўБчМеҝЧөААпөГөҪіЙ№ҰөДОьёҪУлА©ФцЈ¬ІўҝЙ№№ҪЁҪПОӘНкХыөДИэО¬Ҫб№№Ј¬ЖдЦР°ьә¬НкХыЖч№ЩЛщТӘЗуөДСӘ№ЬМе»эәНПё°ыГЬ¶И[24]ЎЈSadhana SөИИЛ[25]УҰУГОўБчМе№М¶ЁјјКхЈ¬ТФИЛЖкҙшҫІВцДЪЖӨПё°ыЧчОӘДЈРНПөНі№№ҪЁПё°ыјдЦКМеПөЈ¬ІўСРҫҝБЛҫЫТТ¶юҙјЈЁPEGЈ©ұЎІгО¬іЦИэО¬Пё°ыНј°ёНкХыРФөДР§ВКЎЈКөСйҪб№ыұнГчЈ¬УлҝЙҝШ№иөЧОпПаұИЈ¬ҪбәПPEGөДөЧОпёДҪшБЛПё°ыНј°ёөДНкХыРФЈ¬¶Ф№№ҪЁСӘ№ЬЧйЦҜ№ӨіМҫЯУРТ»¶ЁөДІОҝјјЫЦөЈЁИзНј4ЛщКҫЈ©ЎЈ
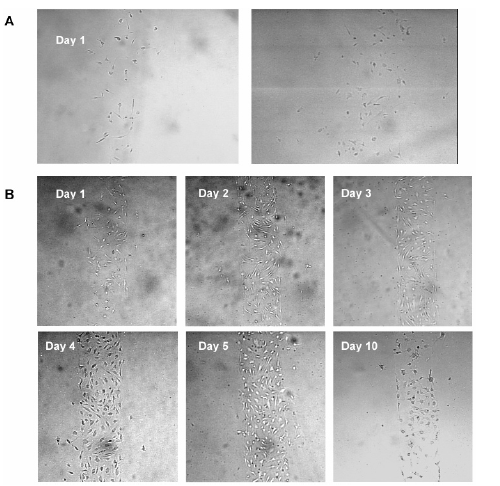
Нј4 A №иЖ¬ЈәЕаСш1Јӯ2МмөДПё°ыЎЈ B.УлPEGҪбәПөД№иЖ¬ЈәЕаСш1Јӯ5МмәН10МмөДПё°ыНјЎЈҫӯ№э10МмЕаСшЈ¬УЙУЪФЪҝЧөАДЪ№э·ЦҫЫјҜөјЦВПё°ыөтНц
[25]ЎЈFig.4 (A) Control silicon: pictures of cells cultured for 1-2 days. After 3 days, we had to take two frames to add images up to get the compliance multifactor; (B) PEG conjugated silicon: pictures of cells cultured for 1-5 days and day 10. After 10-day culture, cells apoptosized due to the overconfluency in the channel area.
3.3 ёОФа
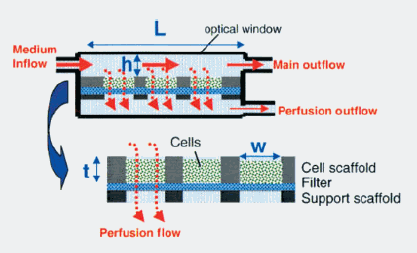
Нј5 Ц§јЬәН·ҙУҰЖчКҫТвНјЈәҝЧөАҝн300mmЈ»Ц§јЬәс235mmЈ»ЙПІҝ·ҙУҰІЫёЯ¶И805mmЈЁҙу·ҙУҰЖчЈ©Ј¬725mmЈЁРЎ·ҙУҰЖчЈ©,Бч¶ҜҝЧөАіӨ400mm[28]ЎЈ
Fig.5 Schematic of scaffold and reactor housing. Dimensions: channel width (w)=300mm;scaffold thicknessЈЁtЈ©ЈҪ235mmЈ»height of upper reactor chamber (h)=805mm(macroreactor), 725mm(millireactor), length of flow path from first to last channel(L)=400mm.
3.4№ЗН·
3.5Ин№ЗЧйЦҜ
ФЪЧйЦҜ№ӨіМБмУт¶ФЦ§іЦ№ШҪЪИн№ЗЧйЦҜФЩЙъөДөЧОпҪшРРБЛҙуБҝСРҫҝЎЈФЪРВИн№ЗЧйЦҜЦРЈ¬МШұрКЗ»щУЪПё°ыөД№ӨіМЈ¬О¬іЦИн№З»щТтөДПФРН·ЗіЈЦШТӘЎЈФЪә¬УРҙуБҝИн№ЗПё°ыөДөҘПё°ыІгәНЙъОп·ҙУҰЖчЦРЈ¬Н¬Пё°ыРьёЎЕаСшТәЦРТ»СщЈ¬Пё°ы·Ц»ҜНЁіЈНЁ№эПЮЦЖПё°ыЙўІјКөПЦ[30]ЎЈОўНј°ёРЮКОјјКхТІҝЙУГУЪ№№ФмЦ§јЬЈ¬МШұрККУГУЪЙијЖЦ§іЦИн№ЗРОіЙөДЦ§јЬЎЈТ»ЦЦОўНј°ёРЮКОөД¶аҝЧ¶аҫЫМЗЦ§јЬТСұ»УГУЪҙЩҪшёЯГЬ¶ИИн№ЗПё°ыЕаСшЎўХіБ¬әНЙъОпәПіЙЈ»ЖдЦ§јЬРОМ¬әНІъЙъҪәФӯЦКўтөДДЬБҰЈ¬ККУГУЪХвР©Ц§јЬөДПё°ыІўҝЙО¬іЦИн№ЗПё°ыПФРН[31]ЎЈ
3.6ЙсҫӯПё°ы
ФЪПё°ыЙъОпҙ«ёРЖчөҪЧйЦҜ№ӨіМөДУҰУГ·ўХ№ЦРЈ¬ҝШЦЖЙсҫӯПё°ы¶ЁО»әНЙъіӨЖрЧЕЦШТӘЧчУГЎЈУҰУГОўөзј«ХуБРјЗВјМеНвЙсҫӯПё°ыөД°ыјдРЕәЕәЬ№г·әЈ¬ХвР©ЙиұёК№УГІЈБ§»тХЯ№иЧчОӘөЧОпЈ¬УГҪрЎўІ¬»точОэСх»ҜОпЦЖіЙөДөзј«№№ФмФЪөЧОпЙПЎЈК№УГХвЦЦПөНіЈ¬ҝЙТФјЗВјҙУЙъОпІъөзОпЦКөД¶аО»өгІъЙъөДЛІјдРЕәЕ[32]ЎЈЦ»УРөұТ»ёцЙсҫӯПё°ыЦұҪУО»УЪөзј«ЙП·ҪКұЈ¬ІЕДЬІъЙъУГУЪРЕәЕјЗВјөДПё°ыәНөзј«јдід·ЦөзсоәПЎЈОӘБЛІЩЧчЙсҫӯПё°ыЙъіӨЈ¬ҝЙТФУҰУГ№вКҙҝМјјКхФЪЙиұёөЧОпұнГжІъЙъ¶ЁПтҪб№№ЈЁНШЖЛҪб№№»т»ҜС§Ҫб№№Ј©[33]ЎЈЧоҪь·ўГчБЛТ»ЦЦОўБчМеЦЖЧчөД¶аҝЧЙсҫӯПё°ыЕаСшЙиұёЈ¬ҝЙТФУҰУГУЪЙсҫӯПөНіөДҝЖС§СРҫҝ[33]ЎЈУлұкЧјЕаСш·Ҫ·ЁәНІЩЧчІ»Н¬ЙсҫӯОў»·ҫіөДЖдЛыҙ«Ні·Ҫ·ЁПаұИЈ¬АыУГОўНј°ёјјКхЦёөјЙсҫӯёҪКфО»өгәНЙсҫӯН»ФціӨЗгПтөДДЬБҰЈ¬ФЪЕаСшЗшУлБчМе·ЦАлЗшУтҪбәПЈ¬ПФКҫіцҫЮҙуУЕФҪРФЎЈLeclerca E өИИЛ[34]УҰУГҫЫхЈСЗ°·РЮКОөДЖҪГжІЈБ§өЧОпұнГжЙПОьёҪ№М¶ЁЙПPC12Пё°ыЈ¬ІўНЁ№эҝШЦЖОўҝЧөАөДҝн¶ИЈ¬ҙУ¶шҝШЦЖЙсҫӯН»ЙъіӨ·ҪПтәНЙсҫӯФӘөДЙъіӨҪб№№ЈЁИзНј6ЛщКҫЈ©ЎЈ
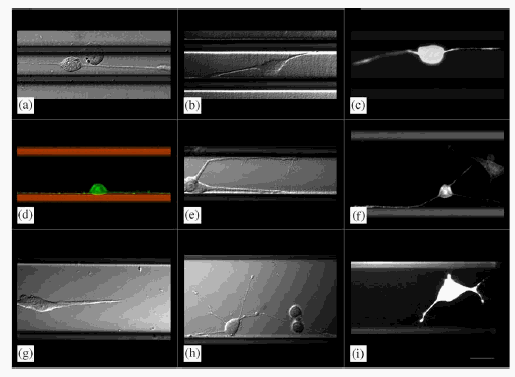
Нј6 PC12Пё°ыЙсҫӯН»ФЪОўҝЧөАЦРЙъіӨ
[34]ЎЈФЪә¬УРЙсҫӯЙъіӨТтЧУөДЕаСш»щЦРЕаСш3МмЈ¬Пё°ыұ»ВМЙ«Пё°ыКҫЧЩОпұкјЗЎЈЙсҫӯН»ЦұҪУУГDICЈЁaЈ¬bЈ¬eЈ¬gЈ¬hЈ©»тХЯУ«№вПФОўҫөЈЁcЈ¬dЈ¬fЈ¬IЈ©»сөГЎЈЙсҫӯН»ФЪПВБРҝн¶ИөДОўҝЧөАЦРФціӨөДөдРНХХЖ¬Јә20mmЈЁaЈ©Ј¬30mmЈЁbЈ¬cЈ©Ј¬40mmЈЁdЈ¬eЈ©Ј¬50mmЈЁfЈ¬gЈ¬IЈ©әН60mmЈЁhЈ©ЎЈұИАэіЯҙъұн20mmЎЈFig.6 PC12 cell neurite growth in microchannels. After 3 days of culture in NGF containing medium, cells were labeled with CellTracker Green. Neurites were directly imaged using DIC (a, b, e, g, h) or fluorescence microscopy (c, d, f, i). Representative images of neurite growth in microchannels with the following widths: 20 mm (a), 30 mm (b,c), 40 mm (d, e), 50 mm (f, g, i), and 60 mm (h). The scale bar represents 20 mm.
3.7»оРФОпЦКөД¶ЁО»ҙ«өЭ
ОўРНИЛФмЖч№ЩҝЙҫ«И·ҙ«өЭ»ҜС§ҪйЦКҪшИлЧйЦҜЦё¶ЁЗшУтЙхЦБПё°ыДЪІҝЎЈУГУЪҙ«өЭөД№иОўМҪХләНОўЧўЙдХлХуБРҝЙУГёчПтН¬ТмРФ·Ё№№Фм
ҙУЙПКцөДЧЫКцЦРҝЙТФҝҙіцЈ¬ОўБчМејјКхФЪЧйЦҜ№ӨіМБмУтөДУҰУГИЎөГәЬҙуөДҪшХ№Ј¬МШұрКЗФЪСӘ№ЬЎў№ЗН·әНИн№ЗЧйЦҜөИ·ҪГжТСөГөҪРн¶аІъЖ·Ј¬Изұн1[38]ЎЈ ұн1 Іҝ·ЦЧйЦҜ№ӨіМІъЖ·ј°ЕаСшЦЬЖЪ
Table 1 Stages of development in selected examples of tissue engineering
ЧйЦҜ |
ИЛ№ӨәПіЙЧйЦҜ |
ЕаСшҪЧ¶О |
У°ПмКФјБ |
СӘ№Ь [39] |
ИЛАаұнЖӨОўВц№ЬДЪЖӨ УГИэО¬ҪәФӯЦКҫШХуҙУЕЯМҘёЙПё°ы»сөГFLK1+Пё°ы УГИэО¬ҪәФӯЎўПЛО¬ФӯҫШХу»сөГөДBCLЈӯ2ИЛАаЖкҙшСӘ№ЬДЪЖӨПё°ы |
·ЦЙўПё°ыЈЁ1МмЈ©Ј»РОіЙ№ЬЧҙҪб№№ЈЁ5МмЈ©Ј»РОіЙ№ҰДЬРФОўВц№ЬЈЁ7МмЈ© ДэҫЫЈЁ0МмЈ©Ј»Пё°ыЕЕБРЈЁ3МмЈ©Ј»¶аПё°ы№№іЙ№ЬЧҙҪб№№ЈЁ5МмЈ© ЎЎ Пё°ыУРРтҪш№ЬЈЁ1МмЈ©Ј»СӘ№ЬҪб№№әНёҙФУ¶аПё°ыЗҪРОіЙЈЁ31Јӯ60МмЈ© |
Јӯ ЎЎ VEGF ЎЎ Јӯ |
№ЗН· [40] |
ФЪPLA-dx-PEG№ІҫЫОпҫШХуөД rhBMP2 TGF-b 1МхјюПВЕаСшөД№ЗЦКПё°ы |
2mm№ЗИұПЭРЮёҙЈЁ2Јӯ4ЦЬЈ©
|
TGF-b 1 rhBMP2 |
Ин№З [41] |
ПЛО¬ө°°ЧҫШХуЦРЕаСшөДЧФУЙөДәНЦ¬ЦКМе°ьЧ°өДTGF-b 1 |
јдТ¶Пё°ыТЖЦІИлҫШХуЈЁКэМмЈ©Ј»Пё°ы·Ц»ҜРОіЙіЙКмИн№ЗПё°ыЈЁКэЦЬЈ© |
TGF-b 1 |
НвО§Йсҫӯ [42] |
К№УГЙъОп»оРФ¶алДөДПЛО¬ө°°ЧҫШХу |
ЙсҫӯЦбН»ФЩЙъ |
Јӯ |
ЦРСлЙсҫӯПөНіЧйЦҜ [43] |
ДФПё°ыҫЫјҜОп·ЦЙўөДPLGAОўЗт |
ЙсҫӯЙъіӨТтЧУФЪЧйЦҜЦРКН·ЕәН»эАЫЈЁјёРЎКұФЪЈӯјёМмЈ©;·Ц»ҜЈЁКэМмЈ© |
NGF |
РШПЩЖч№Щ [44] |
ФЪНҝУРогІгөДИэО¬МјҫШХуЦРЕаСшөДРШПЩ»щЦКПё°ы |
ҫШХуЙП»щЦКІгУРРтЕЕБРЈЁ14МмЈ©Ј»УлСӘәмЛШПё°ыБӘәПЕаСшТФІъЙъTПё°ыЈЁ14МмЈ© |
TGF-b 1 |
ұнЦРЈәBCLЈӯ2Ј¬BЈӯПё°ыБЬ°НБцЈӯ2ө°°ЧЈ»rhBMP2Ј¬ЦШЧйИЛАа№ЗіЙРОЛШө°°Ч2Ј»FLK1+Ј¬Пё°ыұнҙпFLK1ЈЁVEGFКЬМеЦ®Т»Ј©Ј»PLGAЈ¬ҫЫЈЁұыҪ»хҘЈӯcoЈӯТТ¶юҙјЈ©Ј»PLLAЈ¬ҫЫLРНИйЛбЈ»TGF-b 1Ј¬ЧӘ»»ЙъіӨТтЧУ-b 1;VEGF,СӘ№ЬДЪЖӨЙъіӨТтЧУЎЈ
4 ҪбВЫј°Х№Ны
[1] Langer R, Vacanti J. Science, 1993, 260: 920-926.
[2] Hubell J. Curr Opin Biotechnol. 1999, 10: 123-129.
[3] Marler J, Upton J, Langer R et al. Adv Drug Delivery Rev, 1998, 33: 165-182.
[4] (a) Manz A, Graber N, Widmer H M et al. Sens. Actuators, B, Chem., 1990, 1: 244; (b) Manz A, Fettinger J C, Verpoorte E et al. Trends Anal. Chem., 1991, 10: 144.
[5] Fang Z L. Microfluidic chips for analytical chemistry. Beijing: Science Publication Co., 2003.
[6] (a) Folch A, Ayon A, Hurtado O et al. J Biomech. Eng., 1999, 121:28-34 (b) Folch A, Toner M. Biotechnol Prog, 1998, 14: 388-392.
[7] (a) Takayama S, McDonald J, Ostuni E et al. Proc Natl Acad Sci USA, 1999, 96: 5545-5548 (b) Takayama S, Ostuni E, Qian X, et al. Adv. Mater., 2001, 13: 570-574.
[8] Takayama S, Ostuni E, LeDuc, et al. Nature, 2001, 411: 1016.
[9] Feng X Z, Haswell S J, Watts P. Current topics in medicinal chemistry, 2004, 4 (7): 707-727.
[10] Chiu D T, Jeon N L, Huang S, et al. Proc Natl Acad Sci, 2000, 97: 2408-2413.
[11] Singhvi R, Stephanopoulos G, Wang D. 1994, 43: 764-771.
[12] Desai T. Med Eng Phys, 2000, 22: 595-606.
[13] Deutsch J, Motlagh D, Russell B. J Biomed Mater Res., 2000: 53-57.
[14] Braber E D, Ruijter J, Ginsel L et al. J Biomed Mater Res, 1998, 40 (2): 291-300.
[15] Kooten T V, Whitesides J, Recum A. J Biomed Mater Res.: 1998, 43: 1-14.
[16] Singhvi R, Kumar A, Lopez G et al. Science, 1994, 264: 696-698.
[17] Kapur R, Calvert J, Rudolph A. J Biomech Eng, 1999, 121: 65-72.
[18] (a) Flemming R, Murphy C, Abrams G. Biomaterials, 1999, 20 (6): 573-588 (b) Dalby M, Riehle M, Yarwood S et al. Exp Cell Res, 2003, 284: 274-282.
[19] Grodzinsky A, Levenston M, Jin E et al. Annu Rev Biomed Eng, 2000, 2: 691.
[20] (a) Leclerc E, Sakai Y, Fujii T. MicroTAS, 2002: 826-827 (b) Vozzi G, Flaim C, Ahluwalia A et al. Biomaterials, 2003, 24: 2533-2540.
[21] Andersson H, van den Berg A. Sens Actuators B, 2003, 92 (3): 315-325.
[22] Gu W, Zhu X Y, Futai N et al. PNAS, 2004, 101 (45): 15861ЁC15866.
[23] (a) Leclerc E, Sakai Y, Fujii T. Transducers, 2003: 415-418 (b) Vozzi G, Flaim C, Ahluwalia A, et al. Biomaterials, 2003, 24: 2533-2540.
[24] Pins G, Toner M, Morgan J. FASEB, 2000, 14: 593-602.
[25] Sharma S, Tan W, Tejal A et al. Bioconjugate Chem., 2005, 16 (1):18-22.
[26] Borenstein J, Terai H, King K et al. Biomed Microdev., 2002, 4 (3): 167-175.
[27] LeCluyse E, Bullock P, Parkinson A. Adv Drug Delivery Rev., 1996, 22:133-186.
[28] (a) Tilles A, Berthiaume F, Yarmush M. J Hepatobiliary Pancreat Surg, 2002, 9: 686-696 (b) Bathia S, Balis U, Yarmush M et al. Biotechnol Prog., 1998, 14: 378-387; (c) Powers M, Domansky K, Kaazempur-Mofrad M. Biotech Bioeng, 2002, 78 (3): 257-269.
[29] Holy C, Fialkov J, Davies J et al. J Biomed Mater Res., 2003, 65A (4):447-453.
[30] Petersen E, Fishbein K, McFarland A et al. Magn Reson Med, 2000, 44: 367-372; (b) Potter K, Butler J, Horton W et al. Arthritis Rheum, 2000, 43: 1580-1590 (c) Freed L, Martin I, Vunjak-Novakovic G, Clin Orthop, 1999, 367: 46-58.
[31] Petersen E, Spencer R, McFarland E. Biotech Bioeng, 2002, 78(7): 802-805.
[32] Bove M, Martinoia S, Verreschi G. Biosens Bioelectron, 1998, 13: 601-612 (b) Egert U, Schlosshauser B, Fennrich S et al. Brain Res., 1998, 2: 229-242; (c) Thiebaud P, Beuret C, Koudelka-Hep M et al. Biosens Bioelectron, 1999, 14: 61-65 (d) Sprösser C, Denyer M, Britland S et al. Phys Rev, 1999, E60: 2171-2176.
[33] Taylor A, Rhee S, Tu C et al. Langmuir, 2003, 19: 1551-1556; (b) Kleinfeld D, Kahler K Hockberger P. J Neurosci, 1988, 11:4098-4120; (c) Oliva A, James C, Kingman C. et al. Neurochem Res, 2003, 11: 1639-1648.
[34] Leclerca E, Furukawab K.S, Miyatab F et al. Biomaterials, 2004, 25: 4683-4690.
[35] McAllister D V, Allen M G, Prausnitz M R. Annu Rev Biomed Eng, 2000, 2: 289-313.
[36] Chun K, Hashiguchi G, Toshiyoshi H et al. J Appl Phys, 1999, 38: 279-281.
[37] Chen J, Wise K D. IEEE Trans Biomed Eng, 1997, 44: 760-769.
[38] Saltzman W M, Olbricht W. Nat Reviews, 2002, 1: 177-186.
[39] (a) Nor J. E., Peters M C, Christensen J B et al. Lab. Invest, 2001, 81:453-463;(b)Yamashita J,ЎЎITOH H, HIRASHIMA M et al. Nature,2000, 408: 92-96; (c) Schechner J S, Nath A K, Zheng L et al. PNAS,2000, 97: 9191-9196.
[40] (a) Saito N, Okada T , Horiuchi H et al. Nature Biotechnol, 2001, 19: 332-335; (b) Kale S., Biermann S, Edwards C et al. Nature Biotechnol, 2000, 18: 954-958.
[41] Hunziker E B. Osteoarthritis Cartilage, 2001, 9: 22-32.
[42] Schense J C, Bloch J, Aebischer P et al. Nature Biotechnol, 2000, 18: 415-419.
[43] Mahoney M J, Saltzman W M. Nature Biotechnol, 2001, 19: 934-939.
[44] Poznansky M C, Evans R H , Foxall R B et al. Nature Biotechnol, 2000, 18: 729-734.
[45] Andersson H, Van den Berg A. Lab Chip, 2004, 4: 98-103.
[46] Grikscheit T, Ochoa E, Ramsanahie A et al. Ann Surg, 2003, 238, 35-41.
ЎЎ