http://www.chemistrymag.org/cji/2005/07a070pe.htm |
Oct. 12, 2005 Vol.7 No.10 P.70 Copyright |
Wu Xianhua, Zhong Yihui, Zhang Xin, Huang Qiling
(Department of Chemistry, Kunming Teacher's College, Kunming, 650031, China)
Abstract The determination of phenols in main stream smoke by rapid column high performance liquid chromatography was studied. The phenols were collected by Cambridge filter, and were extracted from Cambridge filter with 1% sodium hydroxide solution. Thereafter, the phenols were separated on a ZORBAX Stable Bound (4.6×50 mm, 1.8 m m) rapid column with methanol (containing 0.5% of acetic acid) and 0.05 mol/L potassium dihydrogen phosphates gradient elution as mobile phase at a flow-rate of 2.0 m/min. The key phenols can be separated completely with in 2 min. This method was applied to the determination of phenols in main stream smoke with satisfactory results.
Keywords rapid column High performance liquid chromatography; phenols; main stream smoke 用快速分离柱高效液相色谱法测定卷烟主流烟气中的酚
吴献花,仲一卉,章 新,黄齐林
(玉溪师范学院化学与环境科学系,玉溪 653100) 摘要 研究了用快速分离柱高效液相色谱法测定卷烟主流烟气中的酚类物质,卷烟主流烟气中的酚用剑桥滤片捕集,然后用1%的氢氧化钠溶液振荡浸取,浸取液用C18固相萃取小柱预分离,然后调pH到弱酸性,以甲醇(内含0.5%的醋酸)和0.05 mol/L的磷酸二氢钾缓冲溶液梯度洗脱为流动相,ZORBAX Stable Bound (4.6× 50 mm, 1.8 mm) 快速分离柱分离检测,卷烟主流烟气中的主要酚在2.0 min 内可达到基线分离。所建立的方法可用于卷烟主流烟气中酚的测定。
关键词 高效液相色谱;酚;主流烟气 1 引 言
简单酚类化合物是卷烟主流烟气中的一类重要有害成分,卷烟主流烟气中的简单酚主要有苯酚,苯二酚,甲基苯酚等,它们不但有较难闻的气味,很难被掩盖,对卷烟感观评吸产生不良影响;而且还对皮肤及呼吸道黏膜有强烈的刺激作用和致癌作用 [1,2];因此准确测定卷烟主流烟气中酚类物质对于降低卷烟中的有害成分,提高卷烟的抽吸品质十分重要。酚类物质的测定主要有分光光度法、气相色谱法和液相色谱法等。用分光光度法只能近似测定酚的总量,用气相色谱法直接测定时苯二酚易拖尾,一般需要采用衍生化的方法,高效液相色谱为测定酚类物质最常用的方法,但是传统高效液相色谱法测定酚类物质一般分析时间较长,通常超过20 min [3-6]。我们研究了用ZORBAX Stable Bound (4.6×50 mm, 1.8 mm) 快速分离柱液相色谱法测定卷烟主流烟气中的酚类物质的方法,常见酚类可在2.0 min 内可达到基线分离,取得了满意的结果。
2 实验部分
2.1 仪器与试剂
1100高效液相色谱仪(美国安捷伦公司);包括 1100 四元泵,1100荧光检测器,Chemical Station 色谱工作站。甲醇:高效液相色谱专用(美国Fisher公司生产);蒸馏水:每升水中加入1g硫酸铜,用石英亚沸蒸馏器重蒸,并用Millipore-Q50超纯水仪(Millipore公司)处理,电阻≥18 MW.cm;磷酸二氢钾为色谱纯(瑞士 Fluka 公司生产);苯酚、邻苯二酚、间苯二酚、对苯二酚、邻甲酚、间甲酚、对甲酚(含量≥ 99%;瑞士Fluka公司生产)。
2.2色谱条件
色谱柱为ZORBAX Stable Bound (4.6×50 mm, 1.8 m m)快速分离柱;流动相为甲醇(内含0.5%的醋酸)和0.05 mol/L的磷酸二氢钾缓冲溶液梯度洗脱;流速为2.0 mL/min;梯度变化为:A 甲醇,B 0.05 mol/L的磷酸二氢钾缓冲溶液,按:0 min (A 10% + B 90%),2 min (A 60% + B 40%)。用程序波长荧光检测器检测, 以酚类物质的最大激发波长和发射波长编写荧光检测器的程序,波长变化如下:0 - 0.6 min (激发波长304 nm, 发射波长338 nm),0.6 - 1.0 min (激发波长280 nm, 发射波长325 nm),1.0 - 1.5 min (激发波长257 nm, 发射波长330 nm), 1.5 min -结束 (激发波长285 nm, 发射波长310 nm)。在该条件下标样和烟气样品的色谱图见图1。
固相萃取柱为Waters Sep-Pak-C18固相萃取小柱(1cc/30mg,30 mm);小柱使用前先用5 mL的乙醇活化,然后用水洗净。
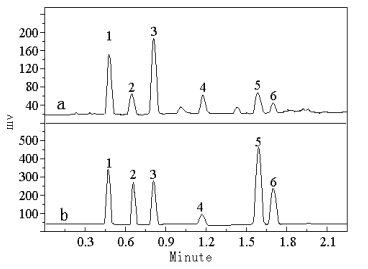
图1 烟气样品(a)和标样(b)色谱图
Fig.1 The chromatogram of tobacco smoke sample (a) and standard sample (b)
1.对苯二酚(hydroquinone);2.间苯二酚(resorcinol) ;3.邻苯二酚(catechol);4.苯酚(phenol);5.间甲酚和对甲酚(m-cresol and p-cresol);6.邻甲酚(o-cresol)
2.3 实验方法
取卷烟样品1条,在GB/T 16447规定的条件下进行,挑选平均重量± 0.02 g和平均吸阻± 49 Pa的卷烟,在YC/T 29规定的条件下用吸烟机进行抽吸,每次测定选20支烟抽吸,并用剑桥滤片收集主流烟气总粒相物,烟吸完后把剑桥滤片和夹持器一起称重。然后把滤片放在锥形瓶内。清扫夹持器的棉球也一并放入瓶中;再准确加入35 mL 1%的氢氧化钠,盖好塞子。用振荡器振荡浸取35 min,过滤,滤液以20 mL/min的流速通过Water Sep-Pak C18固相萃取小柱,过柱后的溶液用醋酸调pH值至2-4之间,准确定容到50 mL。取1 mL溶液用0.45mm聚丙烯薄膜针头过滤器过滤,进样20 mL分析。
3 结果与讨论
3.1样品前处理
酚类物质在碱性介质中有较好的溶解度,因此实验选用1%的氢氧化钠提取剑桥滤片上捕集的酚类物质。实验了振荡浸取,超声振荡浸取,加热回流提取对酚溶出率的影响,结果表明三种方法对酚溶出率无明显影响,因此实验选用较为便捷的振荡浸取。用35 mL的1%氢氧化钠溶液振荡浸取30 min以上可使剑桥滤片上捕集的酚完全浸出,实验选用35 mL的氢氧化钠溶液浸取35min。
卷烟主流烟气中的成分非常复杂,除酚外,还含有芳胺、芳烃和多环芳烃、脂、醛、酮、醚等化合物,这些物质的存在会干扰酚类物质的测定,而且由于其疏水性比酚强,在酚类物质分离的流动相条件下不能被洗脱,在色谱柱上积累而影响柱效。我们根据酚类物质在碱性条件下(pH> 12.5)易电离,电离后以阴离子形态存在,亲水性很强,在反相柱上没有保留的特点,采用固相萃取对样品进行预分离。
样品在pH>12.5条件下通过C18小柱,酚类物质在小柱上没有保留,但芳胺、芳烃和多环芳烃、脂、醛、酮、醚等物质均有较强保留。这样可预分离除去大部分的芳胺、芳烃和多环芳烃、脂、醛、酮、醚等共存物。由于C18材料在碱性条件下不稳定,如果碱性太强,会使柱材料缓慢分解而破坏,碱性弱又会造成酚类物质损失,实验表明,pH低于12.5时,酚类物质的损失趋于明显,而pH高于13.5以上小柱使用寿命很短,因此实验选择用1%的氢氧化钠浸取液直接过柱。
3.2 分离条件的选择
用甲醇-水作流动相,几种酚不能获得很好的分离,而且峰拖尾严重。这是因为酚羟基易产生电离,在固定相表面有双重的保留机制。改用甲醇(内含0.5%的醋酸)和0.05 mol/L的磷酸二氢钾缓冲溶液作流动相可使酚的电离被抑制,成为中性分子在反相条件下的疏水缔合物,可使分离效果和峰型得到较大改善。实验表明用梯度洗脱,当梯度变化为:A 甲醇,B 0.05 mol/L的磷酸二氢钾缓冲溶液,按:0 min (A 10% + B 90%),2 min (A 60% + B 40%)时有较好的分离效果且分离时间短,因此实验选用该梯度条件。
3.3组分的定性及检测波长的选择
样品中各组分均由其保留时间及荧光检测扫描所得的激发光谱图和发射光谱图对照确认,由于各酚最大激发波长和发射波长有差异,为了达到最佳灵敏度,实验采用程序波长检测。波长变化为:0-0.6 min (激发波长304 nm, 发射波长338 nm),0.6-1.0 min (激发波长280 nm, 发射波长325 nm),1.0 - 1.5 min (激发波长257 nm, 发射波长330 nm), 1.5 min - 结束 (激发波长285 nm, 发射波长310 nm)。
3.4工作曲线与检测限
分别配制浓度为1.0mg/mL、5.0mg/mL、20mg/mL、40mg/mL和80mg/mL的酚标准溶液,进样后根据不同浓度的峰面积,计算出回归方程,根据信燥比S/N=3计算检测限,结果见表1。 表1 工作曲线及检测限
Table 1 calibration curves and limits of detection
组分 |
回归方程 |
相关系数 |
检测限 (ng/L) |
对苯二酚(hydroquinone) |
A=2.15×106 C + 1562 |
0.9999 |
2.5 |
间苯二酚(resorcinol) |
A=1.65×105 C + 2818 |
0.9999 |
2.2 |
邻苯二酚(catechol) |
A=1.87×105 C + 1562 |
0.99997 |
2.3 |
苯酚 (phenol) |
A=3.09×104 C + 622 |
0.9999 |
10 |
间甲酚和对甲酚 |
A=3.64×105 C + 1872 |
0.9998 |
1.5 |
邻甲酚 (o-cresol) |
A=1.58×105 C + 1675 |
0.9999 |
3.2 |
3.5方法精密度及回收率
相同卷烟吸两份,其中之一加入已知量酚类物质的标样,另一份不加,在相同条件下连续平行测定5次,通过加标样品测出量减去未加标样品测出量再除以标准加入量计算回收率,根据五次平行测定的结果计算相对标准偏差。结果见表2。
表2 方法精密度及回收率
Table 2 Method Precision and Recovery
组分Compounds |
加入量 |
测出量 |
回收率 |
RSD%(n=5) |
对苯二酚(hydroquinone) |
10 |
9.6 |
96 |
2.6 |
间苯二酚(resorcinol) |
10 |
9.5 |
95 |
3.1 |
邻苯二酚(catechol) |
10 |
10.4 |
104 |
2.8 |
苯酚 (phenol) |
10 |
9.7 |
97 |
3.3 |
间甲酚和对甲酚 |
10 |
10.2 |
102 |
3.5 |
邻甲酚 (o-cresol) |
10 |
9.5 |
95 |
2.9 |
3.6 样品分析
样品按2.3实验方法处理,并按选定色谱条件测定,结果见表3。
表3 卷烟样品分析结果
Table 3 Determination
Results of the Samples
样品 |
测定值Found (mg) |
|||||
对苯二酚(hydroquinone) |
间苯二酚(resorcinol) |
邻苯二酚(catechol) |
苯酚 (phenol) |
间甲酚和对甲酚 |
邻甲酚
|
|
样品-1 (Sample-1) |
8.76 |
4.86 |
15.6 |
10.2 |
1.95 |
1.11 |
样品-2 (Sample-2) |
8.98 |
3.27 |
14.3 |
8.97 |
2.31 |
0.987 |
样品-3 (Sample-3) |
9.64 |
3.16 |
16.8 |
9.26 |
2.18 |
1.26 |
样品-4 (Sample-4) |
10.2 |
3.92 |
16.2 |
12.2 |
2.22 |
1.23 |
4
结论本方法采用1%的氢氧化钠溶液浸取,固相萃取预分离,快速分离柱高效液相色谱法测定卷烟主流烟气中的酚,样品中的主要酚在2.0 min 内可达到基线分离,和常规液相色谱法相比大大缩短了分析时间,而且样品前处理步骤简便快速,便于批量处理。本方法的建立为卷烟主流烟气中酚类物质的快速准确测定提供了方法。
REFERENCES
[1] Li Hanchao,Wang Shuxian. Tobacco,Smoking Chemistry and Analysis. Zhengzhou:Henan Science and Technology Press. 1991, 105
[2] Zhang Huailing,Ge Cuiying. Tobacco Analysis and
Inspection. Zhengzhou: Henan Science and Technology Press. 1994, 252-253
[3] Risner M, Charles H. Journal of Liquid Chromatography. 1993, 16 (18): 4117-4140
[4] Smith C J, Hansch,C. Food and Chemical Toxicology, 2000,38 (7): 637-646
[5] Snook M E. Fresenius' Journal of Analalytical Chemistry. 1991, 339 (3): 199-200
[6] Deutsch L J. CORESTA. 1987, 26 (4): 19-23