http://www.chemistrymag.org/cji/2006/085033pc.htm |
May 1, 2006 Vol.8 No.5 P.33 Copyright |
Yu Jiemei, Wang Xikui, GuoWeilin, Wang
Jingang
(School of Chemistry and Chemical Engineering, Jinan University, Jinan 250022, China)
Abstract AgCl colloid was obtained by using AgNO3 reacted with
NaCl in aqueous solution and then sensitized with UV light illumination. The
photocatalytic degradation of p-nitrophenol in aqueous was realized by near UV light or
sun light illumination with AgCl catalysis. The degradation kinetics of p-nitrophenol was
found to be first-order and the degradation rate coefficient is -0.0337. The degradation
rate of p-nitrophenol was increase with increasing of AgCl concentration and decreased
with increasing of the initial concentration of p-nitrophenol. It was also found that AgCl
was stable during the experiments and can be reused.
Keywords silver chloride,p-nitrophenol
, photocatalytic degradation, catalyzer
氯化银光催化降解对硝基苯酚的研究
于洁玫,王西奎,国伟林,王金刚(济南大学化学化工学院,山东 济南,250022)
2006年3月2日收稿;山东省自然科学基金重点资助项目
(编号Z200B01 ) 摘要 在水溶液中,AgNO3与NaCl反应生成胶体状AgCl沉淀,经紫外光灯照射后得到AgCl催化剂。以AgCl为催化剂,研究了水中对硝基苯酚在近紫外光照射下的光催化降解。结果表明对硝基苯酚在近紫外光或阳光照射下可有效降解,其降解动力学为表观一级反应。AgCl催化剂可重复使用,在相同条件下,p-NP的降解速率随着AgCl催化剂用量的增加而加快,随p-NP浓度的增加而下降。关键词 AgCl,对硝基苯酚,光催化降解,催化剂 1972年Fujishima与Hongda[1]在《Nature》上发表关于在TiO2电极上光解水的论文后,半导体光催化技术引起了科学家的广泛注意,其中半导体光催化剂的选择与优化成为研究热点之一。TiO2因为它价格便宜、稳定性好、可以重复利用等优点成为最常用的光催化剂[2]。但是TiO2光催波剂仅能利用长小于387.5nm的紫外光,对太阳光的利用效率低,而目前实验室中多采用人工光源,能耗大。因此,需要研究开发光能利用率高的新型光催化剂。
AgCl是重要的感光材料,近年来G Calzaferri等[3,4]发现利用AgCl包埋电极,在近紫外光光照射下可将水分解为氧气, 其机理与TiO2光催化分解水类似。汤斌[5-7]等报道以AgCl为光催化剂,在近紫外光光照射下可分解有机色素,杀灭微生物。因此AgCl光催化性能应该引起人们的重视。
1 实验部分
722E型可见分光光度计(上海光谱仪器有限公司),300W高压汞灯(自制) ,JD-3型光照度计(上海市嘉定学联仪表场),对硝基苯酚 (分析纯,上海华东试剂工业供销公司经销),AgNO3(分析纯,国药集团化学试剂有限公司),TiO2(分析纯,北京益利精细化学品有限公司)。
1.2实验方法
1.2.1AgCl催化剂的制备
取适量0.4molL-1的AgNO3水溶液,加入稍过量的NaCl溶液,生成白色絮状AgCl沉淀,过滤,以二次水洗涤后作为催化剂。将该AgCl催化剂在紫外光灯下照射30s,AgCl迅速变为灰褐色,用二次水洗涤,作为光敏化AgCl催化剂。
1.2.2 对硝基苯酚的光催化降解
取适量一定浓度的对硝基苯酚(p-nitrophenol, p-NP)水溶液置于250ml烧杯中,加入一定量的AgCl催化剂,在电磁搅拌器的搅拌下用高压汞灯照射,同时用玻璃滤光片滤除波长360nm以下的紫外光。每间隔5min,取一定体积的反应液高速离心一分钟(1.5×105转/分),然后取上层清液在400nm波长处用1cm比色皿测其吸光度,以试剂空白为参比。
1.2.3 对硝基苯酚光催化降解率的计算
在实验条件下(pH 5.5,浓度0-10 m mol·L-1),p-NP吸光度A与浓度C符合比尔定律,呈良好的线形关系,则p-NP的光降解率P可以用下式表示:
其中A0为p-NP的初始吸光度,Ai为不同时刻的吸光度
2 结果与讨论
取适量2.0 m molL-1的p-NP水溶液,在不加入任何催化剂的条件下分别用高压汞灯UV直接照射(光强E=5.18×104lx)、通过玻璃滤光片滤除波长小于360nm短波的近紫外光照射(E=4.34×104lx)和置于黑暗处(E=0lx),进行空白实验,结果如图1。可见p-NP在无光照时十分稳定,但在紫外光直接照射下可发生一定程度的光解,120分钟降解率接近45%。而以通过玻璃滤光片滤除波长小于360nm短波的近紫外光照射,p-NP亦无变化。说明在无催化剂存在的条件下,p-NP在波长大于360nm的近紫外光照射下不发生降解。为消除UV照射造成的直接光解,在以下实验中除特别说明者外,均采用近紫外光照射,光强E=4.34×104lx。
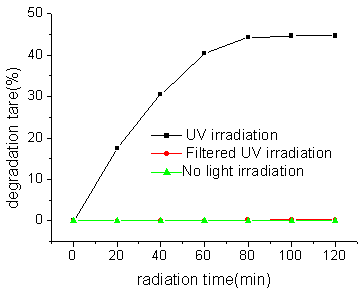
图1 不同光线照射下p-NP的直接光解 2.2 AgCl催化对硝基苯酚的光降解
取适量2.0 m molL-1的p-NP水溶液,加入2.0 m mol的AgCl,分别以紫外光滤光(E=5.18×104lx) 和以玻璃滤光片滤除波长小于360nm短波的近紫外光照射(E=4.34×104lx),同时进行不加任何光照的对比实验,结果如图2。可见在AgCl存在下,如不加以光照,p-NP不发生降解,而在以近紫外光照射下,p-NP浓度迅速下降。说明在AgCl催化和近紫外光照射下,p-NP发生了显著的降解,即光催化降解反应。由图可见,p-NP浓度随降解时间的增加而呈指数性降低,以反应物浓度的对数对降解时间作图,可得直线(图3),符合一级反应速率方程,其降解速率常数(k1)为-0.0337( r=0.995)。
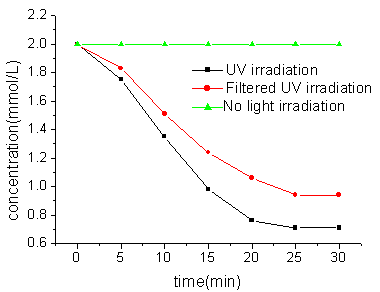
图2 不同光照条件下p-NP浓度与时间关系曲线
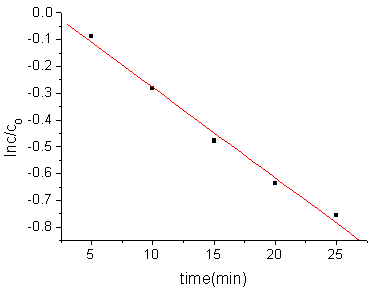
图3 p-NP光催化降解动力学曲线
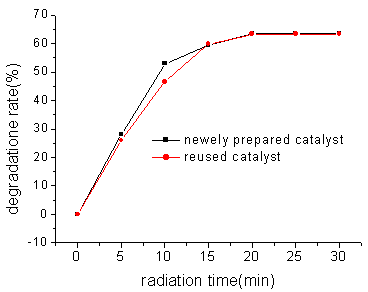
图4 AgCl重复催化降解p-NP
2.3 催化剂的影响
在光催化降解反应中,固体催化剂应保持稳定,并能够重复使用。但是,我们知道AgCl本身不够稳定,在光照下易分解产生Ag原子簇。为了检验AgCl催化剂的重复使用效果,在催化反应结束后,我们将AgCl过滤分离,充分洗涤后,重复进行p-NP的光降解实验,结果如图4。从图可以看出,在光催化降解实验中使用过的AgCl依旧具有很好的光催化活性,其催化效果与新制备的AgCl催化剂几乎完全相同。
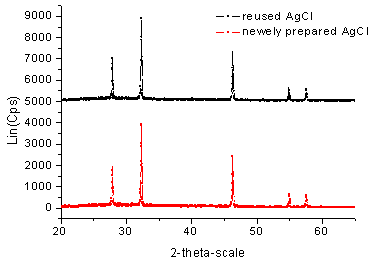
图5 催化反应前后AgCl的XRD衍射图
为进一步考察光照对AgCl催化性能的影响,我们将新制备的AgCl胶体置紫外光灯下照射30s,AgCl迅速变为灰褐色,用二次水洗涤后,进行p-NP的光降解实验,结果如图6。可见经紫外光照射后的AgCl催化效果优于未处理的AgCl胶体,即光照可以使AgCl敏化。其原因可能是由于AgCl在光照下产生了少量的银原子簇,进而降低了其禁带宽度,提高了光利用效率。在AgCl中,Ag+的5s轨道是空的,能量较高,称为空带或导带,Cl-的3p带的能量比Ag+的5s带低,称为价带,两者之差为禁带宽度。与AgCl半导体的带隙位置比较可以发现,银原子簇的空轨道的能量水平线在AgCl的导带之下(图7),银原子簇的存在,能使电子从AgCl的价带转移到银原子簇的能量水平线中,这种跃迁所需要的能量比AgCl价-导带之间跃迁所需要的能量少,使AgCl可以更有效的利用光源,提高了自身的活性[4]。
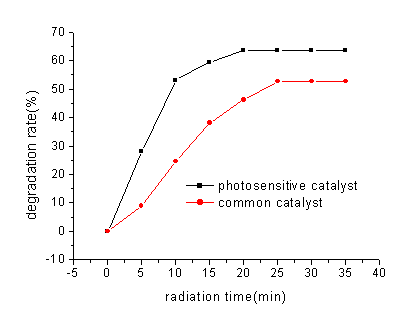
图6 催化剂光敏化对p-NP降解效果的影响
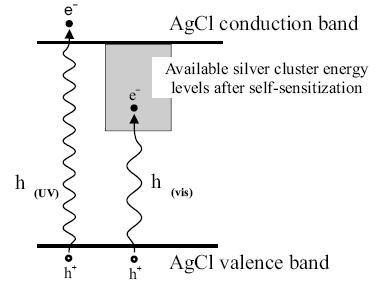
图7 AgCl/银簇带隙位置示意图 2.4催化剂的用量对降解的影响
为了考察催化剂用量对降解实验的影响,我们固定对硝基苯酚的浓度为2.0 mmol L-1,分别加入不同浓度的AgCl催化剂,按前述方法进行其降解,结果如图8。可以看出,随着催化剂用量的增大,对硝基苯酚降解速度明显提高。
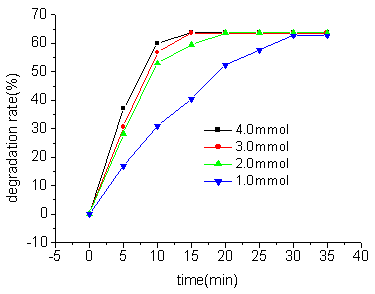
图8 催化剂的用量对p-NP光降解率的影响
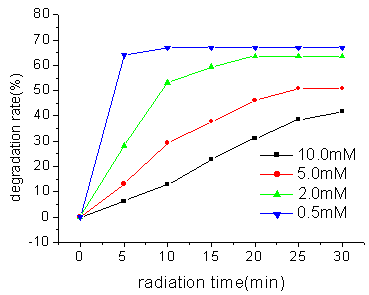
图9 p-NP浓度对光催化降解效果的影响
2.5 p-NP
的浓度对降解的影响固定催化剂的用量(2.0mmol L-1),分别分别加入不同浓度的对硝基苯酚,按前述方法进行降解,结果如图9。由图可知,随着对硝基苯酚浓度的增大,其降解率逐渐降低。
2.6 照射光源对降解的影响
为了考察不同光线对对硝基苯酚降解效果的影响,我们分别考察了近紫外光(E=4.34×104lx)、太阳光(E=4.16×104lx)、室内自然光(E=4.33×102lx)及无光(E=0lx)时p-NP的降解效果,结果如图10。
可见对硝基苯酚在AgCl催化下,以室内自然光照降解非常微弱,无光照时则不降解。而在近紫外光和阳光照射下,可快速降解,且两者差别不大。说明以AgCl作为催化剂,可以利用阳光降解对硝基苯酚,而不是只能利用紫外光。
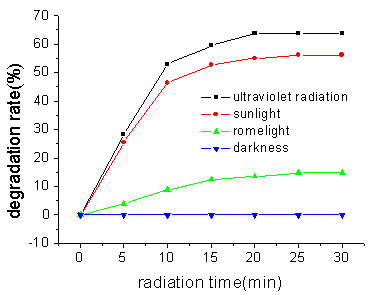
图10 不同光线对p-NP光催化降解效果的影响
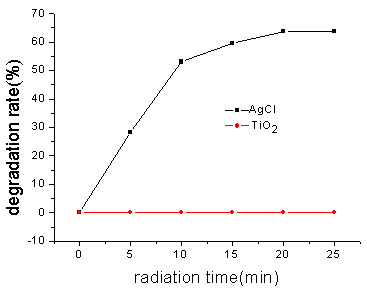
图11 AgCl与TiO2对对硝基苯酚光催化降解效果比较
2.7 AgCl与TiO2光催化降解效果比较
TiO2以其无毒、催化活性高、稳定性好、价廉易得等特点受到人们的重视,是一种应用最广泛的光催化剂,但是由于其禁带宽度较大,在光降解反应中只能利用紫外光。而AgCl在滤除短波的近紫外光照射或太阳光照射下仍然表现出良好的光催化降解效果。图11为相同条件下与TiO2光催化降解对硝基苯酚的实验结果比较,可见在滤除短波的近紫外光照射(E=4.34×104lx)下,对硝基苯酚在AgCl催化下可迅速降解,而同样条件下TiO2光催化降解效果极不明显。
3 结论
[1]A. Fujishima, K. Honda. Nature, 1972, 238(5358): 37-38
[2] Akira Fujishima, Tata N. Rao, Donald A. Tryk. Titanium dioxide photocatalysis. Journal of Photochemisty and Photobiology C: Photochemisty Reviews 1 (2000): 1-21
[3] Martin Lanz,Gion Calzaferri, Photocatalytic oxidation of water to O2 on AgCl coated electrodes, J. Photochem. Photobiolog. A: chemistry, 1997,109:87-89
[4] Martin Lanz,David Schuch, Gion Calzaferri,Photocatalytic oxidation of water to O2 on AgCl coated electrodes,J. Photochem. Photobiolog. A: chemistry, 1999, 120:105-107
[5]Tang B, Zhang QQ. The University of Science and Technology of China Journal(Zhongguo Kexuejishu Daxue Xuebao), 32(6), 2002, 12: 743-747
[6]Song CF, Zhang QQ, Tang B. Journal of Anhui University of Technology and Science(Anhui Gongcheng Keji Xueyuan Xuebao) , 18(1), 2003, 3: 23-25
[7]Zhang Q Q, Tang B. Journal of Nanjing University of Science and Technology (Nanjin Ligong Daxue Xuebao) , 28(5): 2004, 4: 547-551