http:///www.chemistrymag.org//cji/2008/101004pc.htm |
Jan. 1,
2008 Vol.10 No.1 P.4 Copyright |
Shi Huijie, Shi Xianfa
(Chemistry Department of Tongji University, Shanghai 200092
Keywords enzyme mimic, calixarene, cleavage of DNA, molecular recognition
–¬–Ќ±≠ЈЉћю—№…ъќп”лDNA„ч”√–‘÷ µƒ—–Њњ
Јїџљ№£ђ ©ѕ№Ј®
(ЌђЉ√іу—Іїѓ—Іѕµ …ѕЇ£ 200092)
’™“™ ±Њќƒ≤…”√„ѕЌвµќґ®ЇЌ’≥ґ»≤в ‘µƒЈљЈ®—–ЊњЅЋ–¬–Ќ±≠ЈЉћю—№…ъќпUC”лCT-DNAµƒѕаї•„ч”√£ђљбєыЈҐѕ÷£ЇUCњ…“‘“‘Њ≠µд≤е»лµƒƒ£ љ”лDNA„ч”√£ђ≤Ґ”лDNA–ќ≥…1£Ї1µƒ≥ђЈ÷„”їѓЇѕќп£їќ“√«Ќ∆≤вњ…ƒ№ «UC÷–µƒЉоїщƒта„а§≤е»лµљЅЋDNAµƒЉоїщґ‘÷–Љд£ђ∆рµљЅЋ ґ±рDNAµƒ„ч”√°£Ќђ ±£ђќ“√«≤…”√«н÷ђћ«ƒэљЇµз”ЊµƒЈљЈ®£ђ—–ЊњЅЋpBR322 DNAµƒґѕЅ—«йњц£ђљбєыЈҐѕ÷£Ї‘Џќ¬ґ»37
oCћхЉюѕ¬£ђUCµƒіж‘Џґ‘H2O2ґѕЅ—pBR322 DNA∆рµљЅЋ≥ђЈ÷„”іяїѓµƒ„ч”√£ђ єDNAі”±’їЈ≥ђ¬Ё–эµƒForm I –Ќ„™±дќ™»±њћµƒForm II–Ќ°£єЎЉьі ƒ£ƒв√Є£ђ±≠ЈЉћю£ђDNAґѕЅ—£ђЈ÷„” ґ±р
1 Є≈“™
ЇЋЋбґѕЅ—”лїщ“т÷Ў„йЉЉ х «Ј÷„”…ъќп—ІЇЌїщ“тє§≥ћ—ІµƒЇЋ–ƒЉЉ х£ђ∆д÷–ґ‘DNAЇЌRNAµƒґ®ќї«–Єо”÷ «Є√ЉЉ хµƒєЎЉь°£»Ћ√« ‘ЌЉЌ®єэїѓ—ІµƒЈљЈ®Їѕ≥…ƒ№єїґ®µг«–ЄоDNAµƒЈ÷„”Љфµґїт’я√Єµƒƒ£–Ќќп£ђЌ®єэDNAµƒґ®µг«–Єоїт’я—хїѓґѕЅ—£ђЋЃљвґѕЅ—µ»£ђ—∞’“іҐіж‘ЏDNAЈ÷„”÷–µƒ“≈іЂ–≈ѕҐ£ђЅЋљв…ъ√ьµƒ∞¬√Ў£ђќ™“љ÷ќЄч÷÷“≈іЂ≤°£ђ÷„Ѕцµ»љ®ЅҐјн¬џµƒїщі°°£
љьƒкјі£ђƒ£ƒв√Єµƒ—–Њњ“ї÷± «»Ћ√«єЎ„Ґµƒљєµг°£±≠ЈЉћю„чќ™“ї÷÷”≈–гµƒЈ÷„”∆љћ®“≤єгЈЇ”√”Џƒ£ƒв√Єµƒ—–Њњ÷–°£±≠ЈЉћю «“ї÷÷»Ћє§Їѕ≥…µƒ”…»°іъ±љЈ”ќІ≥…µƒїЈ„і≥ђЈ÷„” №ћеїѓЇѕќп[1]°£±≠ЈЉћюЉ∞∆д—№…ъќпµƒЈ÷„”Њя”–іу–°њ…µчµƒ иЋЃњ’«ї£ђњ…“‘љ”ƒ… ґ±ріу–°Їѕ µƒ–°Ј÷„”£ђЌђ ±…ѕѕ¬—Ўњ…“‘љш––їѓ—І–ё ќ£ђ“э»л≤їЌђµƒєўƒ№Ќ≈„чќ™їо–‘ќїµг°£“тіЋ£ђ±≠ЈЉћюЉ∞∆д—№…ъќпњ…“‘Ќђ ±ћбє© иЋЃїЈЊ≥ЇЌїо–‘ќїµг£ђі”ґш є∆д‘Џ…ъќпіуЈ÷„”£ђ»зµ∞∞„÷ £ђЇЋ№’Љ∞ЇЋ№’ЋбµƒіяїѓґѕЅ—÷–Њя”–єгЈЇµƒ”¶”√«∞Њ∞[2-7]°£ƒњ«∞£ђ±≠ЈЉћю—№…ъќпµƒƒ£ƒв√Є—–Њњ÷ч“™ « №»ЋћеƒЏ√Єµƒљбєєµƒ∆фЈҐ£ђ‘Џ±≠ЈЉћюµƒє«Љ№…ѕ“э»лЄч÷÷љр ф≈дЇѕќпЈ÷„”£ђ є∆д„чќ™іяїѓЈі”¶µƒїо–‘ќїµг£ђљшґш—–Њњ∆дґ‘DNAїт’я∆дƒ£–ЌќпµƒіяїѓЋЃљв„ч”√µ»µ»[8-11]°£±≠ЈЉћю±Њ…н”…”Џ»±…ў ґ±рїщЌ≈£ђ≤їƒ№єї ґ±р÷Єґ®µƒЇЋ№’Ћбїт’яDNAЈ÷„”£ђі”ґшѕё÷∆ЅЋЋь√«DNAЇЌЇЋ№’Ћбґ®µг«–Єо÷–µƒ”¶”√£ђ“тіЋ±Њќƒ„ч’я≥Ґ ‘љЂ”–їъ–°Ј÷„”“э»лµљ±≠ЈЉћюµƒє«Љ№µ±÷–£ђ є∆дƒ№єї ґ±рDNAЈ÷„”£ђљшґшіяїѓDNAµƒґѕЅ—°£’вЈљ√жµƒє§„чїєЇ№…ў”–±®µј[12]°£
„ч’я≤…”√Ј÷„”…иЉ∆µƒЈљЈ®£ђ“‘±≠ЈЉћюќ™Ј÷„”∆љћ®£ђ“‘ƒта„ৄчќ™«±‘Џ°∞ ґ±р„”°±£ђ…иЉ∆Їѕ≥…ЅЋЇђ”–ƒта„а§їщЌ≈µƒ—№…ъќпUC£®5-(Uracil-N1-acetamido)-25, 26, 27, 28-tetrahydroxycalix[4]arene£ђЉі£Ї5-(ƒта„а§-N1-““х£∞±їщ)-25, 26, 27, 28-4-ф«їщ±≠[4]ЈЉћю£©£ђ≤ҐЌ®єэ÷ ∆„ЇЌLBƒ§µƒЈљЈ®—–ЊњЅЋUCґ‘ЇЋ№’ЇЌЉоїщµƒ—°‘с–‘ ґ±р£ђљбєы÷§√чUCњ…“‘і”ґа÷÷їмЇѕµƒЉоїщЇЌЇЋ№’µƒ»№“Ї÷–£ђ—°‘с–‘µƒ ґ±р≥цѕўа—я ЇЌѕў№’£®Їѕ≥…¬ЈѕяЉ∞Ј÷„”љбєєЉыЌЉ1£©°£’в≤њЈ÷µƒє§„ч“—Њ≠±®µјєэ[13]°£‘Џ±Њќƒ÷–£ђќ“√«≤…”√„ѕЌвЇЌ’≥ґ»µƒЈљЈ®—–ЊњЅЋUC”лDNAµƒ„ч”√£ђ≤Ґ≤…”√«н÷ђћ«ƒэљЇµз”ЊµƒЈљЈ®ґ‘UCіяїѓpBR322 DNAµƒґѕЅ—„ч”√љш––ЅЋ≥х≤љћљЋч£ђѕ£Ќыƒ№єїќ™њ™ЈҐ≥ц“ї÷÷–¬–Ќµƒƒ№єїґ®µг«–ЄоDNAµƒƒ£ƒв√Є ‘ЉЅµмґ®“їґ®µƒїщі°°£
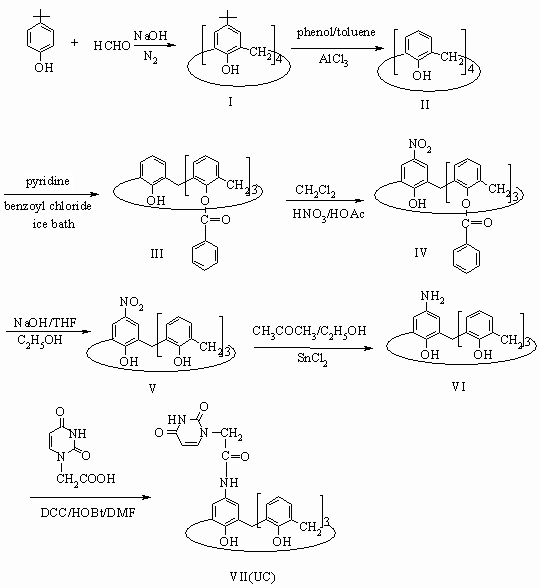
ЌЉ1 UCµƒЇѕ≥…¬ЈѕяЉ∞Ј÷„”љбєєЌЉ
Fig.1 The structure and synthesis route of UC
2 µ—й≤њЈ÷
2.1 “«∆чЉ∞ ‘ЉЅ
Lambda Bio 40 UV/VIS–Ќ „ѕЌвњ…Љыєв∆„“«£®√јєъPEєЂЋЊ£©;ќЏ ѕ’≥ґ»Љ∆£®√ЂѕЄє№ƒЏЊґ0.57mm£ђ…ѕЇ£…кЅҐ≤£ЅІ“«∆ч”–ѕёєЂЋЊ£©;DYY-11–Ќµз”Њ“«£®±±Њ©Ѕщ“ї“«∆ч≥І£©;JY02G–ЌƒэљЇ≥…ѕс“«£®±±Њ©Њэ“вґЂЈљµз”Њ…и±Є”–ѕёєЂЋЊ£©;–°≈£–ЎѕўDNA£®CT-DNA£©єЇ„‘sigmaєЂЋЊ£ђpBR322 DNAєЇ„‘FermentasєЂЋЊ°£
∆дЋыЋщ”– є”√µƒ ‘ЉЅЊщќ™ – џЈ÷ќціњїт…ъќп ‘ЉЅ£ђќіЊ≠„Ґ√чЊщќіљш––і¶јн°£
2.2 »№“Їµƒ≈д÷√
2.2.1 їЇ≥е“Їµƒ≈д÷√
Ћщ”–»№“Їµƒ≈д÷√Њщ є”√TrisїЇ≥е“Ї°£
TrisїЇ≥е“Ї1£ЇЇђ”–5 ´ 10-3mol°Ѕ L-1 TrisЇЌ0.05mol°Ѕ L-1 NaCl£ђ”√—ќЋбµчљЏЋбґ» єpH = 7.2°£UC”лDNAµƒѕаї•„ч”√µƒ„ѕЌвЇЌ’≥ґ» µ—йЊщ‘ЏіЋїЇ≥е»№“Ї÷–љш––°£UCѕ»”√≤ї≥ђєэ10£•µƒDMSO»№љв£ђ‘ў”√іЋTirsїЇ≥е“Їґ®»Ё°£
TrisїЇ≥е»№“Ї2. Їђ”–0.05 mol°Ѕ L-1Tris£ђ0.018 mol°Ѕ L-1 NaCl£ђ”√—ќЋбµчљЏЋбґ» є»№“ЇpH = 7.2°£іЋµз”ЊїЇ≥е“Ї÷ї ”√”Џµз”ЊЈі”¶“Їµƒ≈д÷∆°£
TBEµз”ЊїЇ≥е“Їµƒ≈д÷√ „ѕ»љЂ10.8 g Tris£ђ5.5 g H3BO3ЇЌ0.9 g EDTA»№љв”Џ1000 mLЋЃ÷–£ђ≈д≥… TBEµƒ≈рЋб»№“Ї£ђ≈®ґ»ќ™0.089 mol°Ѕ L-1 Tris£ђ0.089 mol°Ѕ L-1 H3BO3 ЇЌ2 ´ 10-3 mol°Ѕ L-1 EDTA£®pH = 8.3£©°£
2.2.2 UC»№“Їµƒ≈д÷√
ЊЂ»Ј≥∆Ѕњ“їґ®ЅњµƒUC£ђ”√TrisїЇ≥е“Ї1≈д÷√≥…≈®ґ»ќ™4´ 10-5 mol°Ѕ L-1µƒ»№“Ї£ђ”√”Џ„ѕЌвЇЌ’≥ґ»µƒ—–Њњ µ—й°£
ЊЂ»Ј≥∆Ѕњ“їґ®ЅњµƒUC£ђ”√TrisїЇ≥е“Ї2≈д÷√≥…≈®ґ»ќ™1´ 10-4 mol°Ѕ L-1µƒ»№“Ї£ђ”√”Џ«н÷ђћ«ƒэљЇµз”Њµƒ—–Њњ µ—й°£
2.2.3 DNA»№“Їµƒ≈д÷√Љ∞≈®ґ»µƒ»Јґ®
≥∆»° Ѕњµƒ–°≈£–ЎѕўDNA»№”ЏTrisїЇ≥е»№“Ї (pH =7.2)÷–£ђ≥й¬Ћ£ђљЂЋщµ√µљµƒ¬Ћ“Ї∞і–и“™ѕ° Ќ÷Ѕ“їґ®≈®ґ»°£≤вЅњDNA»№“Ї‘Џ260 nmЇЌ280 nmі¶µƒќьєвґ»÷µ£ђ»зєыA260 / A280 = 1.8-1.9£ђЋµ√чїщ±Њ…ѕ≤їЇђµ∞∞„÷ £ђ≤ї–и“™‘ўљш“ї≤љі¶јн°£–°≈£–ЎѕўDNAµƒ≈®ґ»“‘Љоїщґ‘µƒƒ¶ґы≈®ґ»Љ∆£ђ≤вЅњDNA‘Џ260 nmі¶µƒќьєвґ»£ђ»їЇуЄщЊЁDNA‘Џ260 nmі¶µƒƒ¶ґыќьєвѕµ э6600 L°Ѕ mol-1cm-1јі»Јґ®DNAµƒ≈®ґ»°£
[DNA]=K°Ѕ A260/6600
Kќ™ѕ° Ќµƒ±ґ э°£≤вЅњDNAќьєвґ» ±£ђ»зDNA≈®ґ»єэЄя£ђњ…µЉ÷¬ќьєвґ»≤вЅњ≤ї„Љ£ђ“ї∞㔶ѕ° ЌµљA‘Џ0.5-1÷ЃЉдљѕќ™Їѕ °£≈д÷∆Ї√µƒDNAіҐ±Є“Ї”¶‘Џ4 oCќ¬ґ»ѕ¬±£іж£ђ≤Ґ”Џ4ћмƒЏ є”√°£
2.2.4 DNA’≥ґ»µƒ≤вґ®
DNA»№“Їµƒ’≥ґ»”√ќЏ ѕ’≥ґ»Љ∆≤вґ®£ђ≤вґ® ±љЂ»№“Їµƒќ¬ґ»Їгґ®‘Џ30 °ј 0.1oC°£±£≥÷DNA≈®ґ»≤ї±д£®[DNA]=2.5´ 10-4mol°Ѕ L-1£©£ђЄƒ±д[UC]/[DNA]µƒ±»јэ£®[UC]/[DNA]= 0.03£ђ0.06£ђ0.09£ђ0.12£©£ђ≤вµ√≤їЌђUC≈®ґ»ѕ¬DNAµƒѕаґ‘’≥ґ»°£≤в ‘“Їµƒѕаґ‘’≥ґ»∞ієЂ љh = (t ®C t0) / t0Љ∆Ћг£ђ∆д÷–t0ќ™їЇ≥е“ЇЅчЊ≠√ЂѕЄє№Ћщ–иµƒ ±Љд£ђtќ™DNA»№“Ї£®Їђ≈®ґ»≤їµ»µƒUC£©ЅчЊ≠√ЂѕЄє№Ћщ–иµƒ ±Љд°£“‘(h / h0)1/3ґ‘љбЇѕ±»¬ r (r = [UC] / [DNA])„чЌЉ°£h0ќ™ќіЉ”UC ±DNA»№“Їµƒѕаґ‘’≥ґ»°£
2.2.5 «н÷ђћ«ƒэљЇµз”Њ µ—й
0.8%µƒ«н÷ђћ«ƒэљЇµз”Њ£ђpH = 8.3µƒTris-H3BO3-EDTAїЇ≥е»№“Ї„чќ™µзЉЂїЇ≥е»№“Ї£ђдеЈ”јґ»№“Ї„чќ™µз”Њєэ≥ћ÷–µƒ÷Є Њ±к÷Њ£ђѕтЇђ”–pBR 322 DNA µƒ»№“Ї÷–Љ”»л“їѕµЅ–≤їЌђћеїэµƒїѓЇѕќпUC»№“Ї£ђїмЇѕЊщ‘»£ђ єЈі”¶“Їµƒ÷’ћеїэ±£≥÷‘Џ10 mL°£љЂ÷∆±ЄЇ√µƒµз”ЊЈі”¶“Ї‘Џ37°г CЇгќ¬12–° ±£ђ»їЇуљЂіЋµз”ЊЈі”¶“Ї÷√”ЏTBEµз”ЊїЇ≥е“Ї÷–£ђ‘Џ60V£ђ60mAµƒЇг—єЇгЅчћхЉюѕ¬µз”Њ“їґќ ±ЉдЇу£ђ“‘деїѓ““ґІќ™ѕ‘…ЂЉЅ£ђ„оЇу”√JY02G–ЌƒэљЇ≥…ѕс“«Ј÷ќцљбєы≈ƒ…г’’∆ђ°£
3 µ—йљбєыЉ∞ћ÷¬џ
3.1 „ѕЌвєв∆„Ј®—–ЊњUC”лCT-DNA
„ѕЌвєв∆„Ј® «“ї÷÷”––Іµƒ—–ЊњЈ÷„”Љд„ч”√µƒЈљЈ®°£µ±–°Ј÷„””лDNA„ч”√ ±£ђїѓЇѕќпЋщі¶µƒїЈЊ≥ №µљDNAіж‘Џµƒ”∞ѕм£ђЈ÷„”µƒ„ѕЌвќь ’Јеїб≥цѕ÷ѕа”¶µƒћЎ’ч±дїѓ£®∞ьј®Їм“∆°Ґјґ“∆їт’я‘ц…Ђ°ҐЉх…Ђ–І”¶£©[14,15]°£
“‘TrisїЇ≥е“Ї1ќ™≤ќ±»£ђѕт4´ 10-5mol°Ѕ L-1µƒUC»№“Ї÷–µќЉ”“їґ®ћеїэµƒDNA»№“Ї£ђ єµ√[DNA]/[UC]µƒ±»јэ≤їґѕ‘цЉ”£ђЉ«¬Љ»№“Ї‘Џ260nmі¶µƒќьєвґ»÷µ°£±н1÷–ќ™≤їЌђ[DNA] ±£ђ‘Џ260nmі¶їмЇѕћеѕµµƒ µЉ ≤вµ√µƒќьєвґ»÷µЇЌљЂЅљ’я£®DNAЇЌUC£©Љтµ•їмЇѕ£®±ЋіЋќёѕаї•„ч”√µƒ£©µƒЉ∆Ћгќьєвґ»÷µ£®Љіѕа”¶≈®ґ»µƒDNAЇЌUCЄч„‘µ•ґјµƒќьєвґ»÷µ÷ЃЇЌ£©°£
±н
1 ≤їЌђ[DNA]≈®ґ»ѕ¬їмЇѕћеѕµµƒќьєвґ»÷µ£®260nm£©Table 1 the absorption of the mixture where UC (4°Ѕ10-5mol·L-1) was mixed with different concentration of DNA
[DNA]´ 105 mol°Ѕ L-1 |
0 |
0.975 |
1.949 |
2.924 |
3.899 |
5.848 |
7.797 |
9.947 |
11.730 |
µ≤вќьєвґ»÷µ |
0.23055 |
0.32807 |
0.41489 |
0.52342 |
0.61674 |
0.75269 |
0.88800 |
1.01902 |
1.15011 |
Љ∆Ћгќьєвґ»÷µ |
0.23055 |
0.29412 |
0.35768 |
0.42125 |
0.48481 |
0.61194 |
0.73908 |
0.86621 |
0.99334 |
| DA ( µ≤в-Љ∆Ћг) |
0 |
0.03395 |
0.05721 |
0.10217 |
0.13193 |
0.14075 |
0.14892 |
0.15279 |
0.15677 |
ЄщЊЁ…ѕ±н„чЌЉ£®ЌЉ2£©£ђі”ЌЉ÷–ќ“√«њ…“‘њі≥ц£ђ±£≥÷UC≈®ґ»≤ї±д£ђµ±[DNA]/[UC]°№1 ±£ђЋж„≈DNA≈®ґ»µƒ≤їґѕ‘ціу£ђїмЇѕћеѕµµƒќьєвґ»—ЄЋў‘ціу£ђ≤Ґ«“‘Џ[DNA]/[UC]=1 ±£ђDA /
AUCіпµљЅЋ57%£ђ’вЋµ√чDNA”лUC÷ЃЉд»Ј µЈҐ…ъЅЋ„ч”√£ђ≤Ґ«“…ъ≥…µƒ≤ъќп‘Џ≤вґ®≤®≥§260nmі¶µƒƒ¶ґыќьєвѕµ э±»µ•іњµƒDNAїт’яUCµƒƒ¶ґыќьєвѕµ эґЉіу°£µ±[DNA]/[UC]> 1£ђЋж„≈[DNA]µƒ‘цЉ”£ђќьєвґ»»‘”–“їґ®µƒ‘цЉ”£ђµЂ «±»[DNA]/[UC]< 1 ±“™∆љїЇµƒґа£ђїщ±Њ«ч∆љ°£“‘…ѕљбєыЋµ√ч£ђ‘ЏіЋ µ—йћхЉюѕ¬£ђDNA”лUC”≈ѕ»…ъ≥…1£Ї1µƒ≥ђЈ÷„”їѓЇѕќп£ђ’в”л“‘«∞µƒ±®µјљбєы «ѕаЈыµƒ[13]°£µЂ «‘Ћ”√„ѕЌвµƒЈљЈ®ƒњ«∞…–≤ї„г“‘»Јґ®‘ЏіЋ«йњцѕ¬UC”лDNA„ч”√µƒЊяћеќїµгЉ∞„ч”√ƒ£ љ£ђ”–іэ”Џљш“ї≤љ…о»лµƒ—–Њњ°£
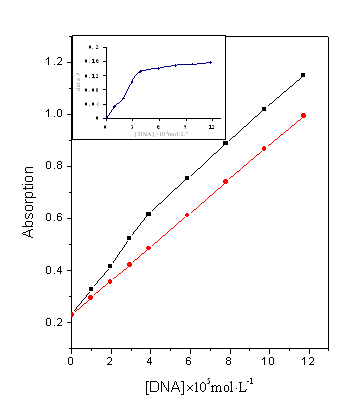
ЌЉ2 ≤їЌђ[DNA]ѕ¬ћеѕµќьєвґ»µƒ±дїѓЌЉ(°ціъ±н µ≤вќьєвґ»÷µ£ї°сіъ±нЉ∆Ћгќьєвґ»÷µ); ≤еЌЉќ™ќьєвґ»±дїѓ÷µґ‘[DNA]µƒ±дїѓ«ъѕя
Fig.2 The variation
of the absorption of the mixture with increasing of the concentration of DNA(°цdenotes the absorption measured;°сdenotes the absorption
calculated); Inserted was the curve of DA
via [DNA]
3.2
’≥ґ»Ј®—–ЊњUC”лCT-DNAµƒѕаї•„ч”√’≥ґ»≤в ‘ «Љм≤в–°Ј÷„”їѓЇѕќп”лDNAљбЇѕƒ£ љµƒ„о”––ІµƒЈљЈ®÷Ѓ“ї£ђ∆дљбєы±»єв∆„ эЊЁЄьЊяЋµЈюЅ¶[16,17]°£µ±–°Ј÷„”їѓЇѕќп“‘Њ≤µз°Ґєµ√жљбЇѕµ»Ј«≤е»лЈљ љ”лDNA„ч”√ ±£ђDNA»№“Їµƒ’≥ґ»ќё√чѕ‘±дїѓ£їµ±–°Ј÷„”їѓЇѕќп“‘Њ≠µд≤е»лЈљ љ”лDNA„ч”√ ±£ђDNAѕаЅЏЉоїщґ‘µƒЊајлїб“т–°Ј÷„”µƒ≤е»лґш±діу£ђµЉ÷¬DNAЋЂ¬Ё–э…м≥§£ђ єDNA»№“Їµƒ’≥ґ»‘цЉ”£ђ≤Ґ«“љбЇѕ«њґ»‘љіу£ђ’≥ґ»µƒ±дїѓ‘љіу£їґшµ±їѓЇѕќп”лDNA“‘≤њЈ÷≤е»лЈљ љ„ч”√ ±£ђ‘тњ…ƒ№ єDNAЋЂ¬Ё–эЈҐ…ъ≈§љб£ђµЉ÷¬DNA»№“Їµƒ’≥ґ»Љх–°°£
±ЊљЏ÷–£ђ„ч’я≤…”√’≥ґ»µƒЈљЈ®≤в ‘ЅЋUCґ‘DNA’≥ґ»µƒ”∞ѕм,≤Ґ”лµд–Ќµƒ“‘≤е»лƒ£ љ”лDNAљбЇѕµƒ≈дЇѕќп[Ru(bpy)2dppz](ClO4)2±»љѕ°£
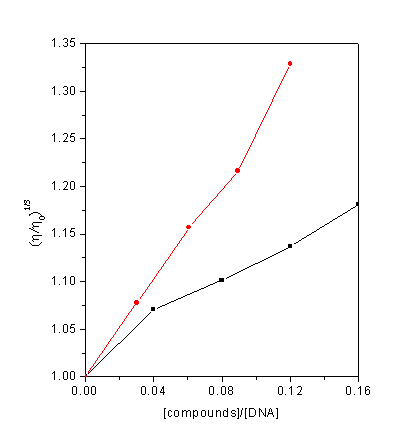
ЌЉ3 ≤їЌђ≈®ґ»µƒUCґ‘DNA»№“Їѕаґ‘’≥ґ»µƒ”∞ѕм: °ц іъ±н≤їЌђ≈®ґ»µƒ[Ru(bpy)2dppz](ClO4)2ґ‘DNA’≥ґ»µƒ”∞ѕм£ї°сіъ±н≤ї”√≈®ґ»µƒUCґ‘DNA’≥ґ»µƒ”∞ѕм
Fig.3 Effect of increasing amounts of UC and [Ru(bpy)2(dppz)]2+ on the relative viscosity of CT-DNA at 30°ј0.01oC. [DNA]=2.5°Ѕ10-4mol·L-1
»зЌЉ3Ћщ Њ£ђќ“√«“‘Њ≠µдµƒ“‘≤е»лƒ£ љљбЇѕDNAµƒ≈дЇѕќп[Ru(bpy)2dppz](ClO4)2„чќ™ґ‘’’£ђЋж„≈UC≈®ґ»µƒ≤їґѕ‘цЉ”£ђDNA»№“Їµƒ’≥ґ»‘ціу£ђ’вЋµ√чUC“‘≤е»лµƒƒ£ љ”лDNAѕаљбЇѕ£ђ≤Ґ«“±»[Ru(bpy)2dppz](ClO4)2µƒ≤е»л«њґ»Єьіу°£ќ“√«Ќ∆≤в’вњ…ƒ№ «UC…ѕµƒЉоїщ£ђЉіƒта„ৄчќ™≤е»лїщЌ≈£ђ≤е»лµљЅЋDNAµƒЉоїщґ‘µ±÷–°£’в÷÷≥ђЈ÷„”„ч”√Ћµ√чUC÷–µƒƒта„а§їщЌ≈»Ј µ∆рµљЅЋ ґ±рDNAµƒ„ч”√£ђ «UC”лDNAљбЇѕ≥…≥ђЈ÷„”їѓЇѕќпµƒљбЇѕќїµг°£µ±»ї£ђUC≤е»лµљDNAЈ÷„”÷–µƒЊяћеќї÷√£ђЉіDNAµƒљ”ƒ…ќїµг…––иљш“ї≤љµƒ»Ј»ѕ°£
3.3 UCґ‘DNAґѕЅ—„ч”√µƒ—–Њњ
«н÷ђћ«ƒэљЇµз”Њ µ—йњ…“‘”√јі—–Њњ–°Ј÷„”їѓЇѕќпґ‘DNAµƒґѕЅ—„ч”√°£‘ЏƒэљЇµз”Њ÷–Њя”–≤їЌђЈ÷„”ЅњµƒDNAµƒ«®“∆Ћў¬ «≤їЌђµƒ£ђЈ÷„”Ѕњ‘љ–°£ђ«®“∆Ћў¬ ‘љіу°£÷ Ѕ£DNA÷–іж‘Џ»э÷÷єє–Ќ°£∆д÷–є≤Љџ±’їЈµƒ≥ђ¬Ё–эForm I µƒљбєє„оќ™љф√№£ђ«®“∆Ћў¬ „оіу£ђ„я‘Џ„о«∞√ж°£ѕя–ќµƒForm III „я‘Џ∆діќ°£ґшњ™їЈ»±њћµƒForm II ”…”Џљбєє±»љѕЋ……Ґ£ђ„я‘Џ„оЇу√ж[18]°£
µ±–°Ј÷„”їѓЇѕќп“‘≤е»лƒ£ љ”лDNA„ч”√ ±£ђЌщЌщїбµЉ÷¬DNAЈ÷„”µƒљв–эЇЌґѕЅ—£ђ≤ъ…ъ≤їЌђєє–ЌµƒDNAЈ÷„”£ђ‘ЏƒэљЇµз”Њ÷–ЊЌїб≥цѕ÷≤їЌђµƒћхіш°£
‘Џ«∞√жє§„чµƒїщі°…ѕ£ђ„ч’я „ѕ»—–ЊњЅЋ≤їЌђ≈®ґ»µƒUCґ‘DNAµƒ„ч”√£ђЈҐѕ÷‘Џ÷ї”–UCЇЌpBR322 DNAіж‘ЏµƒћхЉюѕ¬£ђ37oCѕ¬Їгќ¬12–° ±£ђ≤Ґ√ї”–ЈҐѕ÷pBR322 DNAЈҐ…ъґѕЅ—£®µз”ЊЌЉіЋі¶ќіЅ–≥ц£©°£µЂ «µ±ѕтЈі”¶“Ї÷–Љ”»л“їґ®ЅњµƒH2O2 ±£ђDNAЈҐ…ъЅЋґѕЅ—°£»зЌЉ4Ћщ Њ£ђµ±÷ї”–DNAїтDNA+H2O2іж‘Џ ±£ђDNA≤Ґ√ї”–ЈҐ…ъґѕЅ—£їґшµ±ѕтµз”ЊЈі”¶“Ї÷–Љ”»лUCЇу£ђDNAЈҐ…ъЅЋґѕЅ—£ђі”Form IѕтForm II„™їѓ£ђ≤Ґ«“Ћж„≈UC≈®ґ»µƒ‘цЉ”£ђ”–ЄьґаµƒForm I –ЌpBR322 DNA„™±дќ™Form II –Ќ»±њћDNA°£’вЋµ√чЅЋUCµƒіж‘Џ£ђґ‘H2O2ґѕЅ—DNA∆рµљЅЋ≥ђЈ÷„”іяїѓ„ч”√£ђґш’в÷÷іяїѓ„ч”√јі„‘”ЏUCґ‘DNAµƒЈ÷„” ґ±р£ђњ…“‘єй фќ™“ї÷÷їщ”ЏЈ÷„” ґ±рµƒ≥ђЈ÷„”іяїѓ„ч”√[19]°£’вЄцљбєыќ™њ™ЈҐ–¬–ЌµƒЇђ”–±≠ЈЉћюїщЌ≈µƒDNAґ®µг«–Єоƒ£ƒв√Є ‘ЉЅћбє©ЅЋјн¬џ÷І≥÷°£

ЌЉ4 ≤їЌђUC≈®ґ»ѕ¬pBR322 DNAµƒґѕЅ—«йњц£їћхЉю£Ї37oC±£ќ¬12–° ±£ї0 DNA£ї1 DNA+3m LH2O2£ї2 DNA+3mL H2O2 +10m LUC£ї3 DNA+3m LH2O2+20m LUC£ї4 DNA+3mL H2O2 +30m LUC£ї5 DNA+3mL H2O2+40mL UC£ї6 DNA+3mL H2O2 +50mL UC
Fig.4 Cleavage of pBR322 DNA in the presence of UC, kept at 37oC for 12 hours. Lane 0: DNA alone; 1 DNA+3mL H2O2£ї2 DNA+3mL H2O2 +10mL UC£ї3 DNA+3mL H2O2+20mL UC£ї4 DNA+3mL H2O2 +30mL UC£ї5 DNA+3mL H2O2+40mL UC£ї6 DNA+3mL H2O2 +50mL UC
4 –°љб
±Њќƒ≤…”√„ѕЌвµќґ®ЇЌ’≥ґ»≤в ‘µƒЈљЈ®—–ЊњЅЋ–¬–Ќ±≠ЈЉћю—№…ъќпUC”лCT-DNAµƒѕаї•„ч”√£ђљбєыЈҐѕ÷£ЇUCњ…“‘“‘Њ≠µд≤е»лµƒƒ£ љ”лDNA„ч”√£ђ≤Ґ”лDNA–ќ≥…1£Ї1µƒ≥ђЈ÷„”їѓЇѕќп£їќ“√«Ќ∆≤вњ…ƒ№ «UC÷–µƒЉоїщƒта„а§≤е»лµљЅЋDNAµƒЉоїщґ‘÷–Љд£ђ∆рµљЅЋ ґ±рDNAµƒ„ч”√°£Ќђ ±£ђќ“√«≤…”√«н÷ђћ«ƒэљЇµз”ЊµƒЈљЈ®£ђ—–ЊњЅЋpBR322 DNAµƒґѕЅ—«йњц£ђљбєыЈҐѕ÷£Ї‘Џќ¬ґ»37oCћхЉюѕ¬£ђUCµƒіж‘Џґ‘H2O2ґѕЅ—pBR322 DNA∆рµљЅЋ≥ђЈ÷„”іяїѓµƒ„ч”√£ђ єDNAі”±’їЈ≥ђ¬Ё–эµƒForm I –Ќ„™±дќ™»±њћµƒForm II–Ќ°£±Њќƒќ™њ™ЈҐ–¬–ЌµƒЇђ”–±≠ЈЉћюїщЌ≈µƒ”√”ЏDNAґ®µг«–Єоµƒƒ£ƒв√Є ‘ЉЅћбє©ЅЋјн¬џµƒ÷І≥÷°£
REFERENCES
[1] Gutsche C. D., Dhawan B., No K. H., et al, J. Am. Chem. Soc., 1981, 103: 3782
[2] RondelezY., Bertho G., and Reinaud O., Angew. Chem. Int. Ed., 2002, 41, 1044
[3] Cao Y. D., Zheng Q. Y., Chen C. F., Hu H. M., Huang Z. T., Inorg. Chim. Acta, 2004,
357: 316
[4] Rondelez Y., Duprat A., and Reinaud O., J. Am. Chem. Soc., 2002, 124: 1334
[5] Seneque O., Rager M. N., Giorgi M.,and Reinaud O., J. Am. Chem. Soc., 2000, 122: 6183
[6] Sénèque O., Rager M. N., Giorgi M.,et al, J. Am. Chem. Soc. 2001,
123: 8442
[7] Goto K., Murakami Y., Ueoka R., J. Mol. Catal. B: Enzymatic, 2001, 11: 985
[8] Molenveld P., Engbersen J. F. J., Kooijman H., J. Am. Chem. Soc. 1998, 120:
6726
[9] Rondelez Y., Bertho G., Reinaud O., Angew. Chem. Int. Ed. 2002, 41(6): 1044
[10] Sénèque O., Rager M. N., Giorgi M., et al, J. Am. Chem. Soc. 2005, 127:
14833
[11] Bukhaltsev E., Frish L., Cohen Y., et al, Org. Lett., 2005, 7(23): 5123
[12] Ikeda A., Ejima A., Nishiguchi K., et al, Chemistry Letters, 2005, 34(3): 308
[13] Shi H. J., Shi X. F., Yao T.M., et al, Chinese Journal of Chemistry, in press
[14] Baudoin O., Gonnet F., Lehn J. M., et al, Chem. Eur. J. 1999, 5(9): 2762
[15] He Y.B., Xiao Y. J., Meng L. Z., et al, Tetrahedron Letters, 2002, 43: 6249
[16] Satyanarayana S., Dabroniak J.C., Chaires J.B., Biochemistry, 1992, 31: 9319
[17] Satyanarayana S., Dabroniak J.C., Chaires J.B., Biochemistry, 1993, 32: 2573
[18] Barton J. K., Raphael A. L., J. Am. Chem. Soc., 1984, 106: 2466
[19] Lehn J. M., Nobel lecture, Dec. 8, 1987: 462