http://www.chemistrymag.org/cji/2008/103014pc.htm |
Mar. 1,
2008 Vol.10 No.3 P.14 Copyright |
Yang Hui, Yu Zhaoyun, Yang Llili#
(Hebei University Health Science Center Hebei baoding 071000; #Hebei Normal Unicersity College of Chemistry & Material Science Hebei shijiazhuang 050016) Abstract The adsorption behavior and mechanism of copper in chloride system with ion exchange technique were studied. The experimental conditions of anion exchange resin were optimized with dynamic method. Under optimal reaction system, the influences on the ion exchange process including temperature, concentration of Copper and particle radium were investigated by static method. Moving Boundary Model was applied to describe the kinetics of exchange process. The results showed that the dominant procedure was ion diffusion through particles. The apparent activation energy, reaction order, rate constant and total kinetics equation were obtained.
Keywords Copper;Ion exchange resin;Kinetics;Moving Boundary Model
阴离子交换树脂吸附铜的动力学研究
杨慧 于朝云 杨丽莉#
(河北大学医学部,河北 保定071000;#河北师范大学化学学院,河北 石家庄 050016) 摘要 实验采用离子交换法吸附氯盐体系中的铜,用动态法优化了阴离子交换树脂吸附铜的最佳条件。在最佳反应体系下,用静态法研究了温度、溶液浓度和树脂粒径对交换过程的影响,用动边界模型描述交换过程的动力学,确定了离子交换行为的速度控制步骤为颗粒扩散,推算出了交换过程的表观活化能、表观反应级数、速率常数和动力学总方程式。
关键词 铜;阴离子交换树脂;动力学;动边界模型
工业排放污水如有色冶炼,电镀,化工,印染等行业的废水中常含有铜,当水体被含铜废水污染超过1.0 mg/L时可使白色织物着色,超过1.5 mg/L水有异味。较高浓度的铜对生物体有毒,其影响随有机体种类各不相同。海水及软体动物对铜特别敏感,他们的安全浓度小于10 μg/L,排入水体的铜可通过食物链被生物大量富集,人体摄入过量铜会导致腹痛,呕吐,肝硬化。随着工业文明的发展,环境污染的预防和治理已成为人们愈加重视的一大课题。利用离子交换树脂可以有效的去除铜,以达到高度净化的目的,并有利于资源的再生。
本实验采用离子交换法吸附处理氯盐体系中的铜,并研究了络离子在强碱性阴离子交换树脂上的交换动力学。实验证明铜在201×7阴离子交换树脂上的交换动力学符合动边界模型[1-3]。并通过测定温度、浓度和粒径对交换过程的影响,推算出速度控制步骤、表观活化能、表观反应级数、速率常数和动力学总方程[4-5]。 1. 实验部分
1.1 仪器与试剂
WYX-402型原子吸收分光光度计(沈阳分析仪器厂),201×7强碱性阴离子交换树脂(石家庄市有机化工厂),玻璃交换柱:Ф10 mm×250 mm,氯化钠,亚硫酸钠,五水硫酸铜,盐酸(均为分析纯),实验用水均为二次去离子水。
1.2 实验方法
1.2.1 树脂预处理:201×7强碱性阴离子交换树脂用水浸泡24小时,使其充分溶涨,然后用1%~2%的盐酸溶液浸泡24小时,用水洗至中性备用。
1.2.2 动态法研究:处理好的树脂用滤纸吸干水分后称取5 g,采用湿法装柱,柱高6.6 cm。用一定pH值的含一定浓度氯化钠和亚硫酸钠的混合溶液,以2 mL/min的流速通过交换柱至流出液与混合液的pH相同。然后取10 ml与冲洗液同浓度和同pH值的氯化钠和亚硫酸钠的铜溶液以相同流速通过交换柱,最后用相同浓度和pH值的氯化钠和亚硫酸钠混合液冲洗树脂柱,合并流出液,采用原子吸收光谱法检测流出液中Cu的浓度。
1.2.3 静态法研究:201×7强碱性阴离子交换树脂先用水浸泡24小时,使其充分溶涨,然后用1%~2%的盐酸溶液浸泡24小时,再用水洗至中性,最后用2 mol/L的氯化钠溶液饱和,自然风干。实验过程中溶液浓度为0.01574 mol/L,树脂半径为3.855×10-4 m,取1.0 g树脂于锥形瓶中,加入铜和氯化钠、亚硫酸钠的混合溶液50 ml,在最佳工作条件下,恒温震荡30 min,每间隔2 min取出一定体积的溶液,定容后采用原子吸收光谱法检测溶液中Cu的浓度,j次取样时Cu的交换度(F)为:
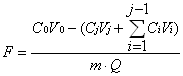 j³ 2 (1)
2. 结果与讨论
j³ 2 (1)
2. 结果与讨论2.1 动态法研究树脂的最佳工作条件
2.1.1 铜(Ⅱ)还原为铜(Ⅰ)的条件选择
实验发现,铜(Ⅱ)较难被阴离子交换树脂吸附,如果还原为铜(Ⅰ)就比较容易被吸附。本实验采用亚硫酸钠为还原剂。
(1) pH值对铜还原的影响:亚硫酸钠还原铜(Ⅱ)和亚硫酸钠的分解反应可分别表示如下:
2Cu2++ Na2SO3 +H2O = 2Cu+ + Na2SO4 + 2H+ (2)
Na2SO3 + 2H+ = SO2 + H2O + 2Na+ (3)
由于式(2)生成氢离子,所以降低氢离子的浓度,即提高溶液pH值有利于反应向生成铜 (Ⅰ)的方向进行;同时式(3)要消耗氢离子,氢离子浓度的降低,导致亚硫酸钠自动分解减少,这样可以减少还原剂的损失。总之,pH值升高,对铜(Ⅱ)的还原有利,从而使分离效果就越好。为避免调节溶液pH值时金属离子发生水解,初始pH值以4.5为宜。
(2)亚硫酸钠用量对铜分离的影响:根据式(2),理论上2 mol铜(Ⅱ)需要1 mol亚硫酸钠进行还原,即1 g铜(Ⅱ)约需要1 g亚硫酸钠,考虑到亚硫酸钠的分解反应,需要过量的亚硫酸钠,用动态法研究了亚硫酸钠对铜吸附率的影响,结果表明,最佳亚硫酸钠用量为铜量的 3倍左右,多于或少于此最佳值都对铜的分离不利。
2.1.2氯离子浓度对铜吸附率的影响
氯离子浓度是影响各配离子浓度的决定性因素,随着氯离子浓度的增加,带负电荷的高配位的配离子浓度CuCl43-增加,从而使树脂的吸附效果提高。但实验发现,氯离子浓度过高时会与铜产生竞争性吸附,反而使铜的吸附率降低。图1为动态法研究氯离子浓度对铜吸附率影响的结果。由图可见,当氯离子浓度为 2 mol/L时,铜(Ⅰ)在树脂上的吸附率最高。
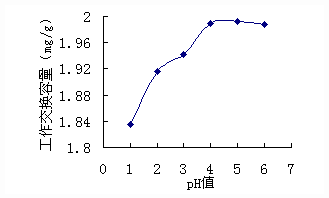
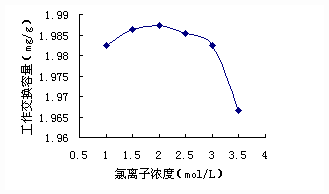
图2 pH值对树脂工作交换容量的影响
2.1.3溶液pH值对铜吸附率的影响
固定氯化钠和Cu2+溶液浓度分别为2 mol/L和0.01574 mol/L。改变溶液pH值,考察溶液pH值对吸附效果的影响。 图2为动态法研究pH值对铜吸附率影响的结果。由图可见,在含2 mol/L氯离子的溶液中,pH=4时铜的吸附率达到最大值。因为在各配离子形式中CuCl43-最容易被树脂吸附
,pH=4时,Cu+与Cl-形成的配阴离子最稳定,pH<4时,其他不易被树脂吸附的配离子浓度增高,从而CuCl43-的浓度降低;pH>4时,由于水解效应,溶液中Cu+浓度下降,从而降低CuCl43-浓度,导致吸附率的下降。
2.2 静态法研究树脂交换过程动力学
2.2.1 温度对树脂交换过程的影响
离子交换过程一般需经历三个步骤:(1)离子由溶液经液膜扩散到树脂表面;(2)离子由树脂表面向树脂内部扩散;(3)离子在树脂内活性基位置发生交换反应;因此离子交换过程受液膜扩散、颗粒扩散和化学反应三个步骤速度的影响,而其中速度最慢的一步是离子交换过程的速度控制步骤。动边界模型的膜扩散、颗粒扩散和化学反应控制方程为[2]:
膜扩散: ![]() (4)
(4)
颗粒扩散:![]() (5)
(5)
化学反应:![]() (6)
(6)
用上述方程对实验数据进行处理,确定反应的速度控制步骤。
实验考察了不同温度下配阴离子的交换动力学,分别用方程(4)-(6)对实验数据进行检验,只有![]() 与t成线性关系,如图3所示。实验结果表明,反应的速度控制步骤为颗粒扩散控制;随着温度升高,扩散速率和交换反应速率均有提高,从而加快了整个过程的交换速率。
与t成线性关系,如图3所示。实验结果表明,反应的速度控制步骤为颗粒扩散控制;随着温度升高,扩散速率和交换反应速率均有提高,从而加快了整个过程的交换速率。
从图3中各直线的斜率可得不同温度下配离子交换过程的表观速率常数k,以![]() 对1/T作图得到图4,结果表明交换过程为吸热反应,将数据进行拟合得出如下方程:
对1/T作图得到图4,结果表明交换过程为吸热反应,将数据进行拟合得出如下方程:
![]() (7)
(7)
根据阿累尼乌斯方程:![]() (8)
(8)
可求得交换过程的表观活化能![]() 为12.84 kJ/mol。
为12.84 kJ/mol。
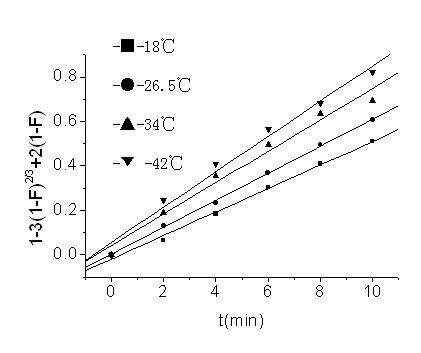
图3 不同温度下对交换模型的检验
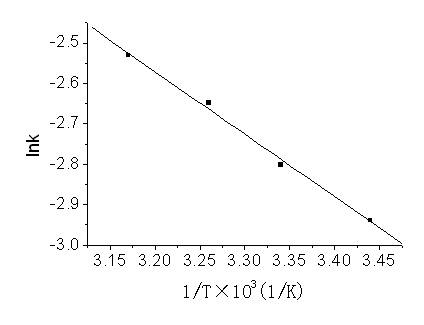
图4 阿累尼乌斯关系图
实验对不同浓度下的交换过程进行了考察,同样用动边界模型对实验结果进行检验,进一步证明了交换过程受颗粒扩散控制,结果见图5,随着溶液浓度的增加,交换过程的交换速率也随之增大。由图5中各直线斜率可得不同浓度交换过程的表观速率常数,实验数据处理结果见表1。
表1 溶液浓度实验数据处理结果
[Cu2+] 浓度mol/L |
lg[Cu2+] |
k´ 103 |
lgk |
线性相关系数 |
0.01259 |
-1.900 |
17.70 |
-1.752 |
0.9928 |
0.01574 |
-1.803 |
24.00 |
-1.620 |
0.9876 |
0.01888 |
-1.724 |
39.79 |
-1.400 |
0.9983 |
根据溶液浓度与表观速率常数的关系: ![]() (9)
(9)
n为表观反应级数,拟合![]() 和
和![]() 可得:
可得: ![]() (10)
(10)
其线性相关系数为0.9796,所以铜配离子交换过程的拟反应级数为1.976。
2.2.3 树脂粒径对交换过程的影响
实验筛选了两种不同粒径的树脂进行动力学实验,实验数据用动边界模型的颗粒扩散控制方程进行处理,结果如图6,![]() 与t成线性关系,实验表明小粒径树脂较大粒径树脂的交换速率快,因为颗粒扩散是控制步骤,对于小粒径树脂,溶液中离子通过树脂表面进入未反应区的路程相应较短,从而相应加快了交换速度。
与t成线性关系,实验表明小粒径树脂较大粒径树脂的交换速率快,因为颗粒扩散是控制步骤,对于小粒径树脂,溶液中离子通过树脂表面进入未反应区的路程相应较短,从而相应加快了交换速度。
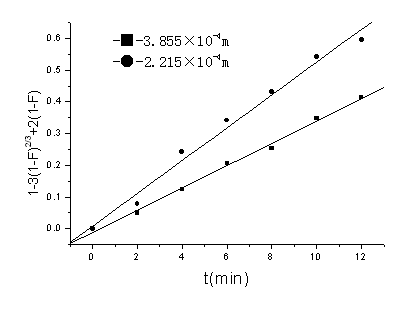
图5 不同浓度下交换过程的模型检验
r:3.855×104 m 温度:16 ℃
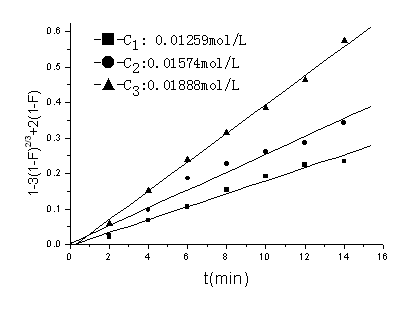
图6 不同粒径下交换过程的模型检验
C0:0.01574 mol/L 温度:17 ℃
通过对温度、溶液浓度和树脂粒径对交换过程影响的实验研究以及得到的表观速率常数,可求得铜配阴离子交换反应的速率常数k0为4.12×10-3,则交换过程的动力学总方程式为:
3 结论
本文主要研究了温度、铜离子浓度和树脂粒径对铜交换过程的影响,发现铜在阴离子交换树脂上的交换过程符合动边界模型,铜在阴离子交换树脂上的交换速率随树脂粒径的减小、温度和浓度的提高而增加,离子交换行为的速度控制步骤为颗粒扩散。
REFERENCES
[1] Tao zuyi.Ion Exchange and Adsorption,1990, 6(3): 232-237
[2] Jang zhixin. Ion Exchange and Adsorption,1989, 5(1): 54-73
[3] Xing zheng,Chen xingqu,Tao zuyi.Acta Chimaca Sinica,1983, 41(11): 1005-1021
[4] Wen yanxuan,Wang lisheng,Jin zuomei etal.Journal of Chemical Engineering of Chinese Unicersities,1999, 13(6): 572-575
[5] Wang yan,Zhou chunshan,Wang xinyan.The Chinese Journal of Process Engineering,2001, 1(4): 356-359