http://www.chemistrymag.org/cji/2008/104016pc.htm |
Apr. 1,
2008 Vol.10 No.4 P.16 Copyright |
Ying
Liyan, Shen Haoyu, Jiang Hailiang, Lin Heng#
(Analysis and Testing Center, Ningbo Institute of Technology,Zhejiang University,Ningbo,Zhejiang
315100; #Biological and Chemical Engineering School,
Ningbo Institute of Technology, Zhejiang University, Ningbo, Zhejiang 315100)
Abstract This paper focuses
on the recent development of using room temperature ionic liquid and H3PO4
as mixed catalyst for alkylation of p-cresol with tert-butyl alcohol. Comparative studies
on the catalytic properties of room temperature ionic liquids,H3PO4,
and their mixed catalyst were carried out under identical reaction conditions. The use of
mixed catalyst was found to be able to enhance the catalytic properties. The conversion of
p-cresol can be achieved 98%, while the selectivity of 2,6-di-tert-butyl-p-cresol can be
achieved to 49%.
Keywords Alkylation, Room temperature ionic liquids, p-cresol ,
tert-butyl alcohol (TBA), H3PO4, mixed catalyst
(浙江大学宁波理工学院分析测试中心 宁波 315100;#浙江大学宁波理工学院生物与化工分院 宁波 315100) 2008年1月22日收稿
摘要 报道了以室温离子液体与H3PO4为混合催化剂协同催化对甲苯酚(p-cresol)和叔丁醇(TBA)烷基化反应的研究,考察了室温离子液体、H3PO4以及室温离子液体与H3PO4混合比例等因素对催化反应的影响,结果表明室温离子液体与H3PO4混合使用能大幅度提高催化性能,对甲苯酚的转化率可达98%,2,6-二叔丁基对甲基苯酚的选择性可达49%。
关键词 烷基化反应、室温离子液体、对甲苯酚、叔丁醇、H3PO4、混合催化剂
2-叔丁基对甲苯酚(简称2-TBC)和2,6-二叔丁基对甲苯酚(简称2,6-DTBC,又称BHT)是对甲苯酚和叔丁醇烷基化反应的主要产物,是生产树脂过程中必需添加的抗氧化剂,并作为杀菌剂、农药、紫外线吸收剂等被广泛应用[1-7]。该反应是典型的Friedel桟rafts烷基化反应,传统的催化剂主要有Lewis酸(如A1C13,BF3)[8]、Brφnsted酸(H2SO4,
H3PO4, HF, HClO4)[9,10]、阳离子交换树脂[11]、沸石[4,5]等。这些催化剂存在着操作苛刻、环境污染、腐蚀、反应时间长、热稳定性差和结垢等缺陷[12-13]。
离子液体,又称室温离子液体(RTIL)或室温熔融盐[14];离子液体的主要优势在于:蒸气压低、液体范围广和热稳定性好等;离子液体也被誉为性能优越的新型反应介质,作为替代常规溶剂在有机反应中的应用方面的研究日趋活跃,如离子液体被直接作为催化剂用于Friedel朇rafts
烷基化反应,催化苯与十二烷反应生成线性烷基苯化合物等[15]。本文以离子液体为催化剂及介质研究了对甲苯酚和叔丁醇烷基化反应,以离子液体、H3PO4以及两者混合物为催化剂对该烷基化反应进行了比较试验,探讨了室温离子液体与H3PO4混合催化剂中离子液体和H3PO4混合比例、反应物比例、反应时间、不同离子液体、混合催化剂加入量等对甲苯酚与叔丁醇烷基化反应的影响。
1.1仪器与试剂
1.1.1 仪器
Agilent 6890N型气相色谱仪配备自动进样器和FID检测器;HP-5 (0.32mm×30m×0.25mm)气相条件:进样口:250oC;检测器:280oC ;N2为载气,流量1 mL/min;柱温:80 oC保持 1.00 min, 20 oC/min的速度上升至150 oC保持2.00 min,25 oC/min上升至280oC保持4 min。
Agilent 6890N/5973N型气质联用仪配备自动进样器;HP-5MS(0.25 mm×30 m×0.25 μm)质谱条件:EI电离源,电离能量70eV,离子源温度230℃,传输线温度280℃,EM为1435V,溶剂延迟2min,质量范围:30~500amu;气相条件:高纯He为载气,流量1 mL/min;柱温:80 oC保持 1.00 min, 20 oC/min的速度上升至150 oC保持2.00 min,25 oC/min上升至280 oC保持4 min。
1.1.2 试剂
对甲苯酚(化学纯,上海化学试剂采购供应五联化工厂);乙醚(分析纯,质量分数≥99.5%,上海化学试剂采购供应五联化工厂);叔丁醇(TBA)(化学纯,上海试剂一厂);H3PO4(化学纯,含量≥85%,上海化学试剂采购供应五联化工厂);[bmim]PF6 1、 [hmim]PF6 2、[omim]PF6 3(见图1)按文献[16]方法合成和提纯;蒸馏水。
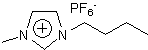

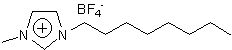
[bmim]PF6 1 [hmim] PF6 2 [omim] PF6 3
图1
离子液体1-3的结构
Fig. 1 Structure of ionic liquids 1-3
1.2 实验步骤
典型反应条件为:10 mL玻璃反应器中加入对甲苯酚1mmol;
n(TBA):n(对甲苯酚)为2:1;0.5mL [bmim]PF6; H3PO4:[bmim]PF6(v/v)比为3:5;
70oC反应4小时后,用乙醚萃取并定容25mL,气质联用仪定性分析各产物,气相色谱进行定量分析,计算转化率和选择性。
2 结果与讨论
2.1
对甲苯酚与叔丁醇烷基化反应产物的组分分析
对甲苯酚1mmol(0.108g),n(TBA):n(对甲苯酚)比为2:1,
0.5mL [bmim]PF6, 70oC反应4小时后,采用气质联用仪定性分析得总离子流图2,确定各产物成分。图2中3.94
min为 对甲苯酚(p-cresol), 4.69 min为对甲基叔丁基醚(CTBE), 6.44 min为2-叔丁基对甲苯酚(2-TBC),
8.13 min为2,6-二叔丁基对甲苯酚(2,6-DTBC)。
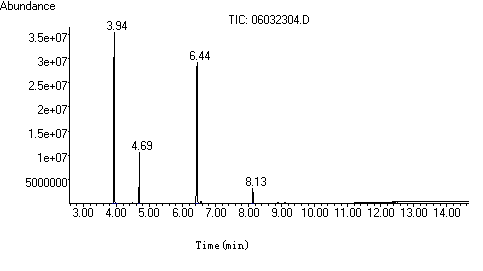
图.2 对甲苯酚与叔丁醇在[bmim]PF6中烷基化反应的总离子流图。条件: 1 mmol 对甲苯酚;n(TBA):n(对甲苯酚)=2:1;0.5
mL[bmim]PF6;70 oC;4h
Fig.2 Total ions chromatography of
Alkylation of p-cresol with tert-butyl alcohol in [bmim]PF6.conditions:
1mmol p-cresol;mole ratio of TBA and
p-cresol=2:1;0.5 mL[bmim]PF6; 70 oC; 4 h.
对甲苯酚1mmol(0.108g),n(TBA):n(对甲苯酚)比为2:1,分别加入催化剂组合1、2、3、4、5(见表1),70oC反应 4小时,考察各种不同催化剂组合的催化活性。离子液体[bmim]PF6呈弱酸性,对烷基化反应有一定的催化活性(对甲苯酚转化率为29%,见表1,Entry 2);H3PO4的催化性能(对甲苯酚转化率为45%,见表1,Entry 1)比离子液体要高,表明对甲苯酚烷基化是一个典型的酸催化反应[4,5]。H3PO4与离子液体[bmim]PF6混合添加后,对甲苯酚的转化率则迅速提高至93%(见表1,Entry 5),可见离子液体不仅具有一定的催化性能外,还是优良的反应介质。与甲苯(对甲苯酚转化率为35%,见表1,Entry 3)、正己烷(对甲苯酚转化率为67%,见表1,Entry 4)相比,对反应物具有更好良好的溶解性能,与H3PO4组合后协同催化烷基化反应,其催化性能的提高不仅仅是两者简单的加和,而是大大促进对甲苯酚转化成产物。
表1 不同催化条件下对对甲苯酚烷基化反应的影响
Entry |
catalyst |
Conversion of p-cresol (%) |
1 |
0.3 mL H3PO4 |
45 |
2 |
0.5 mL[bmim]PF6 |
29 |
3 |
0.5 mL toluene &0.3 mL H3PO4 |
35 |
4 |
0.5 mL hexane &0.3 mL H3PO4 |
67 |
5 |
0.5 mL[bmim]PF6 &0.3 mL H3PO4 |
93 |
conditions: 1 mmol p-cresol;mole ratio of TBA and p-cresol=2:1 ;70 oC;4h.
2.3
离子液体[bmim]PF6和H3PO4混合催化剂对烷基化反应条件的优化2.3.1反应时间对烷基化反应的影响
对甲苯酚1mmol(0.108g),n(TBA):n(对甲苯酚)比为2:1, 0.5mL [bmim]PF6,H3PO4:[bmim]PF6(v/v)为3:5, 70oC条件下考察反应时间对烷基化反应的影响(见图3)。随着反应时间的加长,对甲苯酚的转化率明显提高并达到平台,而2-叔丁基对甲苯酚的选择性逐渐降低,2,6-二叔丁基对甲基苯酚选择性逐渐升高,这表明2,6-二叔丁基对甲基苯酚反应分步进行,先生成2-叔丁基对甲苯酚,再进行6位取代,由于空间位阻的原因,基本没有观察到3、5位取代产物。反应4小时后,反应物的转化率和产物的选择性达到最高值。
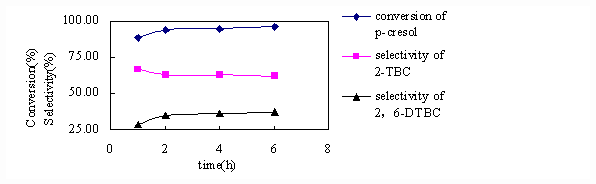
Fig.3 conversion and product selectivity of p-cresol vs reaction time. Conditions: 1 mmol p-cresol;mole ratio of TBA and p-cresol=2:1; 0.5 mL[bmim]PF6;H3PO4:[bmim]PF6(v/v)=3:5; 70 oC.
2.3.2反应物摩尔比对烷基化反应的影响
对甲苯酚1m mol(0.108g),改变TBA物质的量(0.5、1、2、3、4
mmol),0.5mL [bmim]PF6,H3PO4:[bmim]PF6(v/v)为3:5,
70oC反应4小时,研究反应物的摩尔比对烷基化反应转化率和选择性的影响(见图4)。随着TBA物质的量增加,对甲苯酚的转化率出现最大值,2,6-二叔丁基对甲基苯酚的选择性出现最大值后变小,2-叔丁基对甲基苯酚则出现最小值后变大,这可能是TBA物质的量的增加,稀释了混合催化剂的酸性,从而减弱2-叔丁基对甲基苯酚进一步反应生成2,6-二叔丁基对甲基苯酚。当n(TBA):n(对甲苯酚)比为3:1时,2,6-二叔丁基对甲基苯酚的选择性达最高。
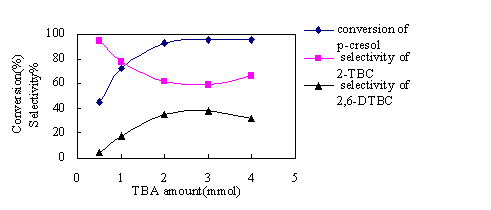
图4 反应物用量对烷基化反应的影响。条件:1
mmol 对甲苯酚; 0.5mL[bmim]PF6;H3PO4:[bmim]PF6(v/v)=3:5;70
oC;4h。
Fig.4 conversion and product
selectivity of p-cresol vs amount of TBA added. Conditions: 1 mmol p-cresol; 0.5
mL[bmim]PF6;H3PO4:[bmim]PF6(v/v)=3:5; 70 oC;
4h.
2.3.3 混合催化剂[bmim]PF6与H3PO4体积比值对烷基化反应的影响
对甲苯酚1mmol(0.108g),n(TBA):n(对甲苯酚)比为3:1,固定[bmim]PF6
0.5 mL,改变H3PO4体积(分别为0.2,0.3,0.4,0.5 mL),考察混合催化剂[bmim]PF6与H3PO4体积比值对烷基化反应转化率和产物选择性的作用(见图5)。结果表明离子液体与H3PO4体积比值对对甲苯酚的转化率变化影响不大;但产物的选择性发生了变化,2-叔丁基对甲苯酚随着磷酸在混合催化剂中的比例增大选择性逐渐降低,而2.6-二叔丁基对甲苯酚的选择性呈上升的趋势,并在离子液体介质与H3PO4体积比值为4:5时达到最大值,可见体系的酸值能够改变产物的选择性,H3PO4的酸性为中强酸,本文中H3PO4的改变量不是很大,对体系来讲酸值改变也比较小,但产物却有新的明显变化,如果使用强的非氧化性酸,产物的选择性可能会发生进一步的变化。
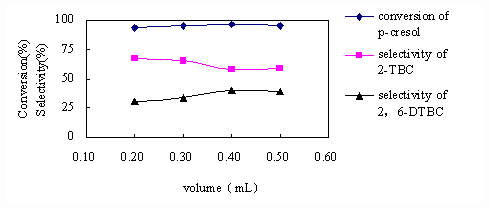
图5 H3PO4添加量对烷基化反应的影响。条件:1 mmol 对甲苯酚;n(TBA):n(对甲苯酚)=3:1;
0.5 mL[bmim]PF6; 70 oC;4h。
Fig.5 conversion and product
selectivity of p-cresol vs amount of H3PO4.Conditions: 1 mmol
p-cresol;mole ratio of TBA and p-cresol=3:1; 0.5 mL
[bmim]PF6; 70 oC 4h.
2.3.4不同离子液体与H3PO4混合对烷基化反应的影响
[bmim]PF6,[hmim]PF6,[omim]PF6
三种离子液体,分别与H3PO4组合成混合催化剂,按上述优化条件:对甲苯酚1mmol(0.108g),n(TBA):n(对甲苯酚)比为3:1,0.5mL
离子液体,H3PO4:离子液体(v/v)为4:5对烷基化反应进行比较,结果表明不同离子液体对甲苯酚的转化率的影响并不明显(见表2),对甲苯酚对离子液体咪唑环上的取代基的烷烃链的长短并不敏感。
Table 2 Alkylation of p-cresol with TBA in different Ionic liquid
Entry |
Ionic liquid |
Conversion of phenol (%) |
Selectivity of 2-TBC (%) |
Selectivity of 2,6-DTBC (%) |
1 |
[bmim]PF6 |
95 |
58 |
39 |
2 |
[hmim] PF6 |
96 |
59 |
38 |
3 |
[omim] PF6 |
95 |
62 |
34 |
Condition: 1 mmol p-cresol;mole ratio of TBA and p-cresol=3:1;H3PO4:[bmim]PF6(v/v)=4:5; 0.5 mL [bmim]PF6; 70 oC; 4h.
2.3.5
混合催化剂加入量对烷基化反应的影响对甲苯酚1mmol(0.108g),n(TBA):n(对甲苯酚)比为3:1,H3PO4:[bmim]PF6(v/v)为4:5,改变混合催化剂的总体积加入量(0.2、0.5、0.9、1.2、1.5mL),研究其对烷基化反应的影响(见图6)。随着混合催化剂的加入量增加,对甲基苯酚的转化率迅速提高,2,6-二叔丁基对甲基苯酚的选择性的增加幅度由大变小,当混合催化剂加入量为1.2mL时对甲苯酚的转化率已基本达到最大平衡值,而2,6-二叔丁基对甲基苯酚的选择性也最好。
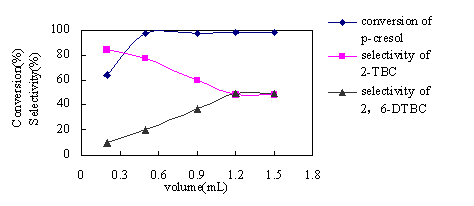
图6 混合催化剂加入量对对甲苯酚与叔丁醇烷基化反应的影响。
条件:1 mmol 对甲苯酚;n(TBA):n(对甲苯酚)=3:1; H3PO4:[bmim]PF6(v/v)=4:5;70 oC;4h。
Fig.6 conversion and product selectivity of p-cresol vs amount of mixed catalyst.
Conditions: 1 mmol p-cresol;mole ratio of TBA and p-cresol=3:1; H3PO4:[bmim]PF6(v/v)=4:5;70 oC; 4h. 3.结论
对甲苯酚与叔丁醇烷基化反应中,离子液体与H3PO4混合催化剂能大大提高H3PO4的催化性能,在70 oC,1 mmol 对甲苯酚;n(TBA):n(对甲苯酚)为3:1; H3PO4:[bmim]PF6(v/v)比为4:5;混合催化剂1.2mL;反应4小时后,对甲苯酚的转化率可达98%,2,6-二叔丁基对甲基苯酚的选择性可达49%。离子液体的合成简便,反应后经乙醚萃取分离,即可与H3PO4混合再次使用,回收方便,在工业化使用中有潜在的使用价值。
REFERENCES
[1] Pospisil J. Poly. Deg. Stab, 1988, 20:181.
[2] Kamalakar G, Komura K, Sugi Y.
Appl.Catal. A: Gen, 2006, 310:155.
[3] Sakthivel A, Badamali S K, Selvam P.
Micropo. Mesop. Mater, 2000, 39: 457.
[4]Krishnan A V, Ojha K, Pradhan N C. Org.
Process Res. Dev, 2002, 6:132.
[5]Zhang K, Zhang H, Xua G, et al.
Appl.Catal. A: Gen, 2001, 207:183.
[6]Sato T, Sekiguchi G, Adschiri T, et al..
Chem. Commun, 2001, 17: 1566.
[7]Sumbramanian S, Mitra A, Satyanarayana C V
V, et al. Appl. Catal. A: Gen, 1997, 159:229.
[8]ivasanker S, Thangaaraj A. J Catal, 1992,
138: 386.
[9] Moon G, Bo¨hringer W, O’Connor C T. Catal. Today, 2004, 97:291.
[10] Shen H Y, A Judeh Z M, Ching C B, et al.
J. Mol. Catal. A: Chem, 2004, 212:301.
[11] Herrmann W A, W B¨ohm V P. J.
Organomet. Chem, 1999, 572: 141.
[12]Kumbar S M, Shanbhag G V, Lefebvre F, et
al. J. Mol. Catal. A: Chem, 2006, 256:324.
[13] Gui J Z, Ban H Y, Cong X H, et al. J.
Mol. Catal. A: Chem, 2005, 225:27.
[14] Welton T. Chem. Rev, 1999, 99: 2071.
[15] DeCastro C, Sauvage E, Valkenberg, et
al. J. Catal, 2000, 196:86.
[16] Owens G S, Abu-omar M M. J. Mol. Catal.
A: Chem, 2002, 187:215.